
常温下,下列各组数据中比值为2:1的是( )
|
科目:高中化学 来源: 题型:
| A、电解熔融的氯化钠,在阴极和阳极上析出产物的物质的量之比 | B、中和体积相同、pH相同的硫酸和盐酸消耗NaOH的物质的量之比 | C、1mol/L氨水与0.5mol/L氨水中的c(OH-)之比 | D、物质的量相同的水和乙醇与足量金属钠反应产生氢气的体积之比 |
科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3溶液中c(Na+)与c(CO32-)之比 |
| B.0.2mol?L-1的CH3COOH溶液与0.1mol?L-1的盐酸中c(H+)之比 |
| C.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比 |
| D.pH=12的Ba(OH)2溶液与pH=12的KOH溶液中溶质的物质的量浓度之比 |
科目:高中化学 来源:不详 题型:单选题
| A.电解熔融的氯化钠,在阴极和阳极上析出产物的物质的量之比 |
| B.中和体积相同、pH相同的硫酸和盐酸消耗NaOH的物质的量之比 |
| C.1mol/L氨水与0.5mol/L氨水中的c(OH-)之比 |
| D.物质的量相同的水和乙醇与足量金属钠反应产生氢气的体积之比 |
科目:高中化学 来源:同步题 题型:填空题
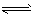 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表: 
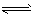 N2(g)+3H2(g)的化学平衡常数的值为___
N2(g)+3H2(g)的化学平衡常数的值为___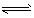 2SO3(g) △H<0某温度下,SO2的平衡转化率(a)与体系总压强(p)的关系如下图所示。根据图示回答下列问题:
2SO3(g) △H<0某温度下,SO2的平衡转化率(a)与体系总压强(p)的关系如下图所示。根据图示回答下列问题: 
科目:高中化学 来源: 题型:阅读理解
图一是煤化工产业链的一部分,试运用所学知识,回答下列问题:
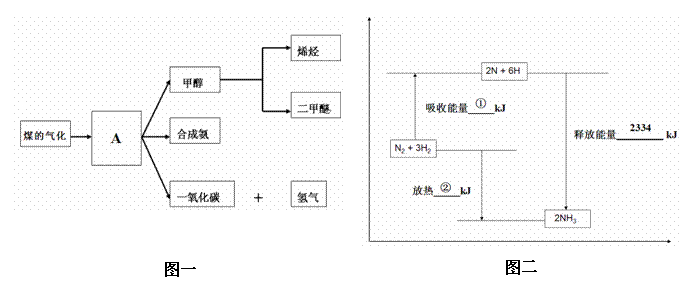
(1)图一中气体A的俗称是_______________
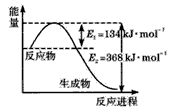
(2)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1mol氮气中的化学键需要吸收946 kJ能量;破坏0.5mol氢气中的H-H键需要吸收218kJ的能量;形成氨分子中1 mol N-H键能够释放389kJ能量。图二表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值,填在下边的横线上。
① kJ ,② kJ
(3)煤化工产业的重要产品之一甲醇,是一种新型的汽车动力燃料,发达国家等一般通过CO和H2化合制备甲醇,该反应的化学方程式为:CO (g) + 2H2(g)![]() CH3OH(g)
CH3OH(g)
①下列描述中能说明上述反应已达平衡的是_______;
A. 容器内气体的平均摩尔质量保持不变
B. 2v(H2)正 = v(CH3OH)逆
C. 容器中气体的压强保持不变
D. 单位时间内生成n molCO的同时生成2n mol H2
②在容积固定的恒温密闭容器中充入CO和H2发生上述反应,反应在第4 min时候达到其限度,此时容器中压强与反应前之比为3︰5,容器内物质的各种物质的量浓度如下表:
| 时间/浓度 | c(CO)(mol/L) | c(H2 )(mol/L) | c(CH3OH)(mol/L) |
| 起始 | 0.200 | 0.300 | 0.000 |
| 第4 min | a | b | c |
则b=__________________
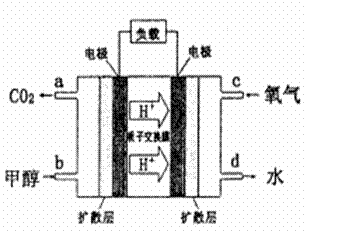
(4)甲醇—空气燃料电池(DMFC)是一种高效能、轻污 染电动汽车的车载电池,其工作原理如下图所示,该燃料电池的电池反应式为2CH3OH (g) + 3O2(g) = 2CO2(g) + 4H2O(l),则负极的电极反应式为______________________,正极附近pH值_______________(填写“增大”、“减小”或者“不变”)
科目:高中化学 来源:2011-2013学年福建省泉州市南安市华侨中学高二(上)期末化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
Ⅰ.800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应CO(g)+H2O(g) H2(g)+CO2(g),反应过程中测定的部分数据见下表:
H2(g)+CO2(g),反应过程中测定的部分数据见下表:
| 反应时间/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | | 0.80 |
| n(H2O)/ mol | 0.60 | | 0.20 | |
| 组别 | 药品1 | 药品2 | 实验现象 |
| I | 0.01 mol/L NaOH溶液 | 0.01 mol/L MgCl2溶液 | 生成白色沉淀 |
| II | 0.01 mol/L氨水 | 0.01 mol/L MgCl2溶液 | 无现象 |
| III | 0.1 mol/L氨水 | 0.1 mol/L MgCl2溶液 | 现象III |
| IV | 0.1 mol/L氨水 | 0.01 mol/L MgCl2溶液 | 生成白色沉淀 |
| V | 0.01 mol/L氨水 | 0.1 mol/L MgCl2溶液 | 无现象 |
 2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。
2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com