
| 已知反应2SO2(g)+O2(g)?2SO3(g)△H<0.现有甲、乙两个容积相同的恒容容器.在500℃和有催化剂存在下,向甲中加入2molSO2和1molO2,向乙中加入2molSO3,并同时发生反应.当两容器中反应分别达到平衡后,维持条件不变,则 ①平衡时甲中SO2的转化率一定等于乙中SO3的分解率 ②从开始反应到平衡,甲中反应放出的热量与乙中反应吸收的热量一定相等 ③平衡时,甲、乙两容器中混合气体平均相对分子质量一定相等 ④从反应开始到刚好建立平衡时所用的时间甲一定等于乙 以上说法中正确的是( )
|
科目:高中化学 来源: 题型:
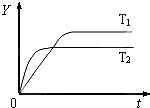 已知反应2SO2(g)+O2(g)?2SO3(g)△H<0,向某体积恒定的密闭容器中按体积比2:1充入SO2和O2,在一定条件下发生反应.下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )
已知反应2SO2(g)+O2(g)?2SO3(g)△H<0,向某体积恒定的密闭容器中按体积比2:1充入SO2和O2,在一定条件下发生反应.下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:单选题
| A.③ | B.①② | C.③④ | D.①②③ |
科目:高中化学 来源: 题型:
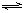 2SO3(g)在某温度达到平衡时,各物质的浓度是[SO2]=0.1mol?L-1、[O2]=0.05mol?L-1、[SO3]=0.9mol?L-1。如果体系温度保持不变,而将体积减少到原来的一半,试通过计算说明平衡移动的方向。
2SO3(g)在某温度达到平衡时,各物质的浓度是[SO2]=0.1mol?L-1、[O2]=0.05mol?L-1、[SO3]=0.9mol?L-1。如果体系温度保持不变,而将体积减少到原来的一半,试通过计算说明平衡移动的方向。科目:高中化学 来源:2012-2013学年湖北省宜昌市长阳一中高二(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源:2012-2013学年黑龙江省大庆实验中学高二(上)期末化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:
 2SO3(g) ΔH=-98.3kJ?mol-1,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )。
2SO3(g) ΔH=-98.3kJ?mol-1,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )。科目:高中化学 来源: 题型:
 2SO3(g)在一密闭容器中进行。已知初始浓度 c0(SO2)=0.4mol?L-1、c0(O2)=1mol?L-1,如达到平衡时有80%的SO2转化为SO3,求平衡时三种气体的浓度和平衡常数。
2SO3(g)在一密闭容器中进行。已知初始浓度 c0(SO2)=0.4mol?L-1、c0(O2)=1mol?L-1,如达到平衡时有80%的SO2转化为SO3,求平衡时三种气体的浓度和平衡常数。科目:高中化学 来源: 题型:
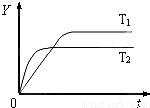
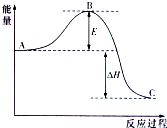 2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.科目:高中化学 来源: 题型:

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com