
下列说法中正确的是( )
|
科目:高中化学 来源:2011年浙江省高考化学模拟试卷(解析版) 题型:选择题
 O2(g)=CO2(g)△H=-283.0kJ?mol-1
O2(g)=CO2(g)△H=-283.0kJ?mol-1科目:高中化学 来源:2011-2012学年浙江省湖州市高二(下)期末化学试卷(解析版) 题型:选择题
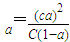 .若加入少量CH3COONa固体,则电离平衡CH3COOH?CH3COO-+H+向左移动,a减小,Ka变小
.若加入少量CH3COONa固体,则电离平衡CH3COOH?CH3COO-+H+向左移动,a减小,Ka变小科目:高中化学 来源:2011年浙江省高考化学试卷(解析版) 题型:选择题
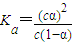 .若加入少量醋酸钠固体,则CH3COOH
.若加入少量醋酸钠固体,则CH3COOH O2(g)═CO2(g);△H=-283.0kJ?mol-1.C(石墨)+O2(g)═CO2(g);△H=-393.5kJ?mol-1.则4Fe(s)+3O2(g)═2Fe2O3(s);△H=-1641.0kJ?mol-1
O2(g)═CO2(g);△H=-283.0kJ?mol-1.C(石墨)+O2(g)═CO2(g);△H=-393.5kJ?mol-1.则4Fe(s)+3O2(g)═2Fe2O3(s);△H=-1641.0kJ?mol-1科目:高中化学 来源:2011年普通高等学校招生全国统一考试化学卷(浙江) 题型:单选题
下列说法不正确的是
A.已知冰的融化热为6.0 kJ·mol  1,冰中氢键键能为20 kJ·mol 1,冰中氢键键能为20 kJ·mol 1 。假设每摩尔冰中有2 mol 氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键 1 。假设每摩尔冰中有2 mol 氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键 |
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为 若加入少量CH3COONa固体,则电离平衡 若加入少量CH3COONa固体,则电离平衡 向左移动,a减小, 向左移动,a减小, 变小 变小 |
C.实验测得环己烷(1)、环己烯(1)和苯(1)的标准燃烧热分别为-3916kJ 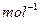 、-3747kJ 、-3747kJ 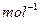 和-3265kJ 和-3265kJ 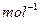 ,可以证明在苯分子中不存在独立的碳碳双键。 ,可以证明在苯分子中不存在独立的碳碳双键。 |
D.已知:  |
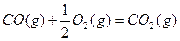
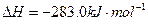

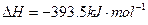
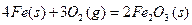

科目:高中化学 来源:不详 题型:单选题
A.已知冰的融化热为6.0 kJ·mol  1,冰中氢键键能为20 kJ·mol 1,冰中氢键键能为20 kJ·mol 1 。假设每摩尔冰中有2 mol 氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键 1 。假设每摩尔冰中有2 mol 氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键 |
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为 若加入少量CH3COONa固体,则电离平衡 若加入少量CH3COONa固体,则电离平衡 向左移动,a减小, 向左移动,a减小, 变小 变小 |
C.实验测得环己烷(1)、环己烯(1)和苯(1)的标准燃烧热分别为-3916kJ  、-3747kJ 、-3747kJ  和-3265kJ 和-3265kJ  ,可以证明在苯分子中不存在独立的碳碳双键。 ,可以证明在苯分子中不存在独立的碳碳双键。 |
D.已知:  |






科目:高中化学 来源: 题型:阅读理解



科目:高中化学 来源: 题型:
| A、已知冰的熔化热为6.0kJ/mol,冰中氢键键能为20kJ/mol,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | ||
B、已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Kα=
| ||
| C、实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916kJ/mol、-3747kJ/mol和-3265kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 | ||
| D、已知: Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g),△H=+489.0kJ/mol. CO(g)+
C(石墨)+O2(g)═CO2(g),△H=-393.5kJ/mol; 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0kJ/mol |
科目:高中化学 来源:不详 题型:填空题
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (K) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
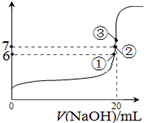
 SO2Cl2(l) △H=–97.3kJ·mol—1
SO2Cl2(l) △H=–97.3kJ·mol—1科目:高中化学 来源:2012-2013学年河南省商丘市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
Ⅰ.电离平衡常数(用K表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
|
化学式 |
HF |
H2CO3 |
HClO |
|
电离平衡常数 (K) |
7.2×10-4 |
K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
(1)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液 ②NaHCO3溶液 ③NaF溶液 ④NaClO溶液。依据数据判断pH由大到小的顺序是______________。
(2)25℃时,在20mL0.1mol·L—1氢氟酸中加入VmL0.1mol·L—1NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是_______。
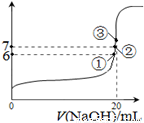
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol·L—1
(3)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH=-akJ·mol—1,
②H+(aq)+OH-(aq)=H2O(l) ΔH=-bkJ·mol—1,
氢氟酸的电离方程式及热效应可表示为________________________。
(4)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H—O—F。HFO与等物质的量的H2O反应得到HF和化合物A,则每生成1molHF转移_______mol电子。
Ⅱ.氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点–54.1℃,沸点69.1℃。氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
SO2(g)+Cl2(g) SO2Cl2(l) △H=–97.3kJ·mol—1
SO2Cl2(l) △H=–97.3kJ·mol—1
(1)试写出常温常压下化学平衡常数K的表达式:K=_________________;
(2)对上述反应,若要使化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是_____(选填编号)。
a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(3)下列描述中能说明上述反应已达平衡的是____________(选填编号)。
a.υ(Cl 2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl 2) : c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(4)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g。若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是________________________。
科目:高中化学 来源:2012届辽宁省葫芦岛一高高二下学期第二次月考化学试卷 题型:填空题
(12分)
为了比较温室效应气体对目前全球增温现象的影响,科学家通常引用“温室效应指数”,以二氧化碳为相对标准。表1有(A)至(I)共九种气体在大气中的体积百分比及其温室效应指数。
结合表中列出的九种气体,试参与回答下列各题:
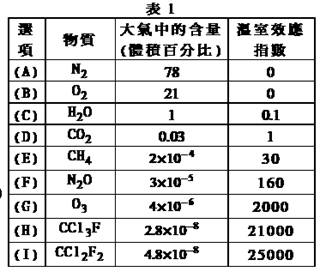
(1)下列由极性键形成的非极性分子是 。
A.N2 B.O2 C.H2O D.CO2 E.CH4
(2)下列说法正确的是 。
A.N2O与CO2, CCl3F与CCl2F2互为等电子体
B.CCl2F2无同分异构体,说明其中碳原子采用sp2方式杂化
C.CCl2F2是目前引起温室效应的主要原因
D.H2O沸点是九种物质中最高的,是因为水分子间能形成氢键
(3)在半导体生产或灭火剂的使用中,会向空气逸散气体如:NF3、CHClFCF3、C3F8,它们虽是微量的,有些确是强温室气体,下列推测正确的是 。
A.由价层电子对互斥理论可确定NF3分子呈平面三角形
B.C3F8在CCl4中的溶解度比水中大
C.CHClFCF3存在手性异构
D.电负性:N<O<F
(4)甲烷晶体的晶胞结构如图,下列有关说法正确的 。

A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个CH4分子有6个紧邻的甲烷分子
C.CH4晶体熔化时需克服共价键
D.可燃冰(8CH4·46H2O)是在低温高压下形成的晶体[来源:学*科*网]
(5)水能与多种过渡金属离子形成络合物,已知某紫红色络合物的组成为CoCl3·5NH3·H2O。其水溶液显弱酸性,加入强碱并加热至沸腾有氨放出,同时产生Co2O3沉淀;加AgNO3于该化合物溶液中,有AgCl沉淀生成,过滤后再加AgNO3溶液于滤液中无变化,但加热至沸腾有AgCl沉淀生成,且其质量为第一次沉淀量的二分之一。则该配合物的化学式最可能为 。
A.[ CoCl2(NH3)4 ]Cl·NH3·H2O B.[ CoCl(NH3)5]Cl2·H2O
C.[ CoCl2(NH3)3(H2O)]Cl·2NH3 D.[ Co(NH3)5(H2O)]Cl3
(6)题(5)中钴离子在基态时核外电子排布式为: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com