
某学生要称取5.4克氯化钠,他在左边托盘上放5克砝码,又把游码移至0.4克处,然后在右盘上加氯化钠至天平平衡.这时托盘上氯化钠的实际质量是( )
|
科目:初中化学 来源:不详 题型:单选题
| A.5.4克 | B.4.6克 | C.5.0克 | D.5.8克 |
科目:初中化学 来源:2012-2013学年福建省泉州市南安市华侨中学九年级(上)第一次月考化学试卷(解析版) 题型:选择题
科目:初中化学 来源:2012-2013学年内蒙古呼伦贝尔市九年级(上)第一次月考化学试卷(解析版) 题型:选择题
科目:初中化学 来源: 题型:单选题
科目:初中化学 来源:汕头市2006-2007学年度初三化学综合测试卷、新人教 题型:013
某学生要称取5.4克氯化钠,他在左边托盘上放5克砝码,又把游码移至0.4克处,然后在右盘上加氯化钠至天平平衡.这时托盘上氯化钠的实际质量是
A.5.4克
B.4.6克
C.5.0克
D.5.8克
科目:初中化学 来源: 题型:阅读理解
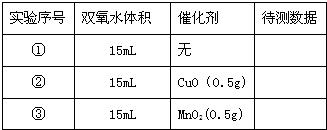
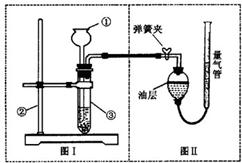
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 实验现象 | 实验结论 |
| ①从甲同学的烧杯中取少量上层清液于试管中,向其中滴加足量 CaCl2 CaCl2 溶液. |
有白色沉淀生成 |
生成白色沉淀的化学方程式为: Na2CO3+CaCl2=CaCO3↓+2NaCl Na2CO3+CaCl2=CaCO3↓+2NaCl . |
| ②过滤,向滤液中滴加无色酚酞试液. | 无明显现象 | 通过实验及分析,样品中不含有: Ca(OH)2、NaOH和CaO Ca(OH)2、NaOH和CaO . |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com