
为了检验某溶液中是否含有Fe3+,可加入KSCN溶液,如果溶液中含有Fe3+,溶液会变成血红色:这主要是因为反应了Fe(SCN)3的缘故,在这个反应过程中,Fe元素的化合价并没有改变,又知在Fe(SCN)3中,C元素化合价为+4,N元素化合价为-3,则S元素的化合价为( )
|
科目:初中化学 来源: 题型:
科目:初中化学 来源:不详 题型:单选题
| A.-2 | B.+2 | C.+4 | D.+6 |
科目:初中化学 来源:2011-2012学年江苏省苏州市吴中区九年级(上)期末化学试卷(解析版) 题型:选择题
科目:初中化学 来源:2012年甘肃省平凉市庄浪县阳川中学中考化学模拟试卷(九)(解析版) 题型:选择题
科目:初中化学 来源: 题型:单选题
科目:初中化学 来源: 题型:探究题
(9分)地球上的金属资源广泛地存在于地壳和海洋中,工业上主要是从含有金属元素并有开采价值的矿石中提炼金属。
(1)赤铁矿在自然界中储藏丰富,其主要成分的化学式是 。
(2)磁铁矿的主要成分是Fe3O4。在Fe3O4中存在两种不同价态的铁离子,其中1/3是Fe2+,2/3是Fe3+。请写出Fe3O4与盐酸反应的化学方程式 。
(3)工业上主要采用高炉炼铁,常用到的原料有铁矿石、焦碳、石灰石和空气。其中,焦碳的作用是 。(仅答一点)
(4)由于铁的氧化物中Fe3O4和FeO均为黑色,实验室用CO还原Fe2O3得到的铁中是否会含有Fe3O4和FeO,某同学设计了下列探究实验。
资料:FeCl3溶液与铁发生的反应是2FeCl3+Fe=3FeCl2,但FeCl3溶液不与Fe3O4、FeO反应;含有Fe3+的盐溶液遇到KSCN溶液时变成红色,利用该反应可检验Fe3+的存在。
【提出问题】CO还原Fe2O3得到黑色产物的成分是什么?
【猜 想】
猜想l:Fe 猜想2:Fe和Fe3O4;
猜想3:Fe和FeO; 猜想4: 。
【实验探究】限选试剂:C0、盐酸、澄清石灰水、KSCN溶液、FeCl3溶液。
| 实验操作 | 实验现象 | 实验结论 |
| Ⅰ取少量黑色产物加入到装有足量FeCl3溶液的烧杯中,充分反应后过滤,对过滤所得固体用蒸馏水洗涤。 | 黑色固体部分溶解。 | 猜想2和4都 不成立。 |
| Ⅱ , 。 | 黑色固体全部溶解,溶液 不变红色。 | |
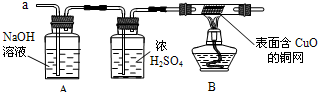
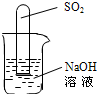
| Ⅲ另取少量黑色产物装入玻璃管中,通入C0,一段时间后加热,并将反应后的气体通入装有一定量的 的烧杯中。 | 。 | 猜想l不成立, 猜想3成立。 |
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 实验结论 |
| Ⅰ取少量黑色产物加入到装有足量FeCl3溶液的烧杯中,充分反应后过滤,对过滤所得固体用蒸馏水洗涤。 | 黑色固体部分溶解。 | 猜想2和4都 不成立。 |
| Ⅱ , 。 | 黑色固体全部溶解,溶液 不变红色。 | |
| Ⅲ另取少量黑色产物装入玻璃管中,通入C0,一段时间后加热,并将反应后的气体通入装有一定量的 的烧杯中。 | 。 | 猜想l不成立, 猜想3成立。 |
科目:初中化学 来源: 题型:解答题
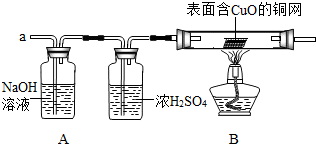
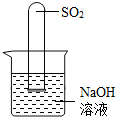 ______.要得到科学严谨的结论,仍利用该装置,补做的实验是______.
______.要得到科学严谨的结论,仍利用该装置,补做的实验是______.| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | ______ | FeCl3溶液可以催化分解H2O2 |
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 | 无明显现象 | ______ |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的______,并把带火星的木条伸入试管 | ______ | ______ |
科目:初中化学 来源:2010年湖南省株洲市攸县一中化学奥赛选拔试卷1(解析版) 题型:解答题
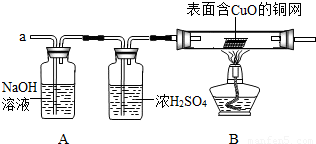
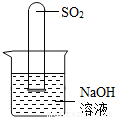 ______.要得到科学严谨的结论,仍利用该装置,补做的实验是______.
______.要得到科学严谨的结论,仍利用该装置,补做的实验是______.| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | ______ | FeCl3溶液可以催化分解H2O2 |
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 | 无明显现象 | ______ |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的______,并把带火星的木条伸入试管 | ______ | ______ |
科目:初中化学 来源: 题型:阅读理解
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | 试管中有大量的气泡产生,伸入的带火星的木条复燃 |
FeCl3溶液可以催化分解H2O2 |
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 | 无明显现象 | 起催化作用的不是Cl- |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的 Fe(NO3)3溶液 ,并把带火星的木条伸入试管 |
试管中有大量气泡产生,带火星的木条复燃 |
起催化作用的是Fe3+ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com