
【题目】现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
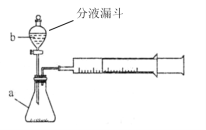
(1)下列方法能检查该装置气密性的是_______。
A.将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B.关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C.关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)甲小组有如下实验设计方案,完成下表。
实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 探究_________对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
(3)甲、乙两小组得出如下图数据。
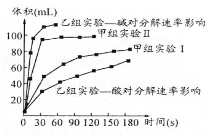
①甲组实验得出的数据可知:浓度越大,H2O2分解速率_________;
②由乙组研究的酸、碱对H2O2分解影响因素的 数据相同条件下, H2O2在_______(填“酸”或“碱”)性环境下放出气体速率较快
【答案】AB 过氧化氢溶液浓度 越快 碱
【解析】
(1)气密性的检验是根据压强原理,可以关闭分液漏斗活塞,将注射器外移看停止用力后看注射器活塞能够复原,也可固定注射器活塞,采用液面差法,也可用升高温度法,故选AB;
(2)由甲组两个实验对比可以看出实验Ⅱ中催化剂与实验Ⅰ中的相同,而过氧化氢浓度不同,因此甲组的实验目的为探究浓度对速率的影响;
(3)①由图象可知在体积-时间图,斜率即可代表化学反应速率,由甲组实验两条曲线可知,甲组实验Ⅱ斜率大,因此H2O2的浓度越大分解速率越快;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析可知碱性越强,放出气体的速率越快,由图可知碱性条件下,H2O2分解的速率较快。


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:
【题目】下图所示为实验室常用的实验装置:
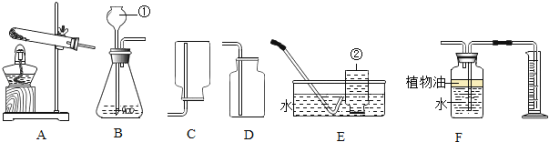
据此回答下列问题:
(1)写出带标号仪器的名称:②_______________;
(2)常温下,实验室制取并收集较纯净氧气选择的装置组合是______(填序号,下同),化学方程式为___________________________________,其基本反应类型是_____________。
(3)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是___________.
(4)某同学在实验室用大理石与一定浓度盐酸制取二氧化碳,发现产生气体的速率太快,请你分析并写出可能的原因_______________________________,实验室检验二氧化碳的反应方程式是____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图表是整理数据、发现其中规律的一种重要工具。1-18号元素原子最外层电子数与原子序数的关系如图。试回答:
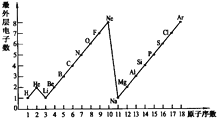
(1)图中和Cl元素化学性质相似的是____;(用元素名称填空)
(2)从图中你可以发现的一条规律是:_____________;
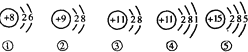
(3)图中属于第二周期的金属原子有_____种;如图是1-18号元素中部分粒子的结构示意图其中②和③两种粒子构成的化合物的化学式是______;⑤的原子核内的中子数比核外电子数多1个,则它的相对原子质量是________。
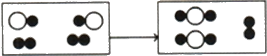
(4)下图为某化学反应的微观模拟图,“○”和“●”分别表示两种不同的原子:由 “![]() ”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的两种反应物中单质与化合物的分子个数比为______,此反应的基本反应类型为_____。
”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的两种反应物中单质与化合物的分子个数比为______,此反应的基本反应类型为_____。
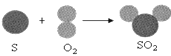
(5)硫与氧气的反应可用下图表示:写出该反应的实验现象_______,设n个氧气分子的质量为32g,则64g氧气与足量硫粉完全反应生成的二氧化硫分子数为________n。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】核电荷数为 1~18 的元素的原子结构示意图等信息如下,请回答下列问题。

(1)原子序数为 11 的元素属于_______(填“金属”或“非金属”)元素,位于第 2 周期第VA 族的元素名称是________。
(2)硅元素和碳元素有相似的化学性质,是因为硅原子和碳原子的__________相同。
(3)一般地说,电子层数相同的原子(稀有气体除外),原子半径随着原子序数的递增而逐渐减小;最外层电子数相同的原子,原子半径随电子层数的增加而增大。请比较:氧原子、钠原子和硫原子的半径由大到小的顺序为____________。
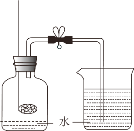
(4)原子序数为 15 的元素组成的单质常用来做“测定空气中氧气的含量”实验(如图所示),实验中该单质发生反应的化学方程式为__________。关于该实验,下列说法正确的是________。
A.该实验可说明氮气不易溶于水
B.燃烧匙中的固体可以换成木炭
C.燃烧匙中的固体量不足会导致测定结果偏小
D.实验过程中弹簧夹未夹紧会导致测定结果偏小
(5)A 物质为奥运火炬常用燃料,纯净物 A 在 B 物质中充分燃烧,发生反应:A+5B ![]() 3C+4D(部分微观示意图如下所示)。
3C+4D(部分微观示意图如下所示)。

①在上述反应中提供氧,具有氧化性的物质为________(填化学式);
②A 物质中各元素的质量比为___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】很多宏观现象都是由微观来揭示本质的,宏观微观建立起了一定联系。我们一起走进微观世界。元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息
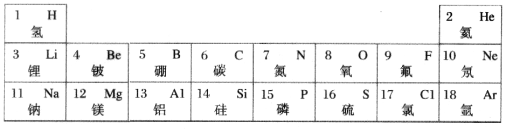
请认真分析表中信息,回答下列问题:
(1)质子数为17的元素名称是_________该元素原子的核外电子层数为_________。
(2)某粒子的结构示意图是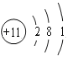 ,该粒子属于____(填金属或非金属)元素,它的最外层电子数为_____,该粒子易_______电子,形成的粒子符号是________。
,该粒子属于____(填金属或非金属)元素,它的最外层电子数为_____,该粒子易_______电子,形成的粒子符号是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人们日常生活中非常熟悉的物质之一,我们应该多角度进行研究。

(一)水的组成——电解水
(1)电解一段时间后,将两极产生的气体的体积与时间的关系绘制成图②所示的平面直角坐标系,回答:
①由图①、②看出,A气体是__(填化学式),B气体在电源的___极。
②0~8min A、B气体的体积比为________。
(2)微观该反应中发生分解的微粒是____。
(3)电解水的化学方程式为__________。
(二)水的净化
小刚收集到一瓶浑浊的长江水,他要模拟自来水厂的净水过程,最终制成自来水。其实验过程如图所示。请回答以下问题。

(4)操作①的名称是_________;该操作中用到的玻璃仪器有烧杯、玻璃棒和_______。
(5)操作②主要是除去水中的异味和色素,应选用的物质是_____。
(6)小刚发现经净化后的D是硬水,日常生活中常用___ 的方法使硬水软化。
(三)水的性质、变化和用途
(7)下列是有关水的性质、变化和用途的描述:
a.通常为无色、无味的液体
b.没有水,人和动物就无法生存
c.水是常用的灭火剂
d.氢气在氧气中能燃烧生成水
e.水可与氧化钙(CaO)反应生成氢氧化钙。
①其中属于水的物理性质的有________(填序号,下同);属于水的化学性质的有________;属于水的用途的有__________。
②写出上文描述中体现水的化学性质的化学方程式____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,A的单质是自然界中密度最小的气体;B、C分别是地壳中含量最多的非金属元素和金属元素;D的单质在空气中燃烧产生大量白烟,在军事上可作烟幕弹;E元素的单质可在B元素形成的单质中燃烧,产生蓝紫色火焰。
(1)用元素符号表示:A______,B_______,D________,E________。
(2)由B、C两种元素形成的化合物的化学式是________。
(3)写出D的单质在空气中燃烧的化学方程式___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是氢气在氯气中燃烧生成氯化氢的微观模拟图,请回答下列问题:
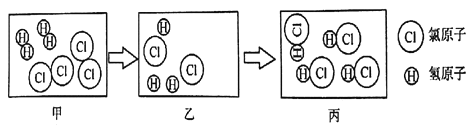
(1)请你将乙图补充完整,使该模拟图符合质量守恒定律。_______
(2)丙图中的物质是由两种元素组成的纯净物,从微观角度解释理由:__________。
(3)氯化氢在水中会解离出 ________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】四种物质在密闭容器内充分反应,测得反应前后各物质的质量分数如下表所示。则有关说法中错误的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前 | 17% | 10% | 25% | 48% |
反应后 | 19% | 10% | 41% | 30% |
A. 丁一定是化合物
B. 乙可能是这个反应的催化剂
C. 该反应可以是碳酸钙或过氧化氢的分解反应
D. 参加反应的丁的质量一定等于生成甲和丙的质量之和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com