
【题目】下列物质的性质与用途的对应关系错误的是
A. 苏打可与盐酸反应,可用于治疗胃酸过多症
B. 活性炭疏松多孔可用于吸附水中杂质
C. 氮气的化学性质不活泼可作焊接金属的保护气
D. 浓硫酸具有强吸水性,可用作干燥剂
科目:初中化学 来源: 题型:
【题目】小明在协助老师清理实验储备室时,发现一瓶存放多年的氢氧化钙,为检验其变质情况,进行如下探究:取氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,然后逐滴滴加14.6%的稀盐酸,加入稀盐酸的质量与锥形瓶中物质的质量关系如下表所示,请问:
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
锥形瓶中物质的质量/g | 60 | 70 | 80 | 90 | 100 | 109.12 | 118.24 | 128.24 |
(1)氢氧化钙变质的原因是 (用化学方程式表示)。
(2)与氢氧化钙反应的稀盐酸溶液的质量为 g。
(3)计算11.4g该样品中氢氧化钙的质量分数(写出计算过程,结果精确到0.1%)。
(4)根据计算所得数据画出生成CO2的质量的曲线。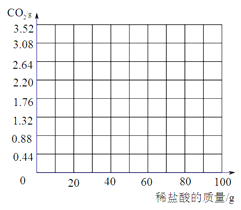
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体代谢产生的过氧化氢,对人体有毒害作用。人体肝脏中的过氧化氢酶能催化过氧化氢分解产生氧气和水。某同学查阅资料发现,FeCl3也能催化过氧化氢分解。为比较过氧化氢酶和FeCl3催化效率的高低,该同学在28℃环境下进行了如下探究:
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设: 。
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),适宜浓度的过氧化氢溶液等。
(4)实验步骤:
①取2支洁净的试管,编号为1、2,并各注入3mL适宜浓度的过氧化氢溶液;
②向1号试管内滴入2滴适宜浓度的FeCl3溶液,向2号试管内 ;
③观察并记录两支试管产生气泡的情况。
(5)预测实验结果:
请写出一种可能的实验结果: 。
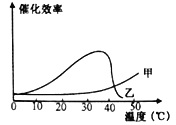
(6)在以上探究的基础上,该同学又完成了“探究温度对猪肝研磨液和FeCl3催化效率的影响”实验。实验结果如图所示。图中代表猪肝研磨液催化效率的曲线是 ,判断的理由是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH值变化的部分数据如表所示。(已知BaCl2溶液的pH=7)
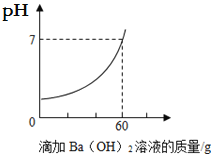
滴加氢氧化钡溶液的质量/g | 5 | 10 | 25 | 30 |
烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 | 4.66 |
求:(1)完全反应后生成沉淀的质量为_______;
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用化学用语填空:
①氯气分子____;②电解水过程中不变的微粒____;
(2)写出下列反应的化学方程式:①工业上用磁铁矿来炼铁:____;②2017年5月18我国首次试采可燃冰(CH4·nH2O)宣告成功,可燃冰分解后,可释放出水和天然气,请写出天然气完全燃烧的化学方程式:____;
(3)如图是A、B两种固体物质的溶解度曲线.回答:
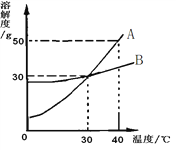
①要使接近饱和的A溶液变为饱和溶液,可采取的方法是__;
②在40℃时,等质量的A、B物质的饱和溶液降温到30℃时溶液质量的关系A____B(选填“大于”、“小于”或“等于”);
③30℃时,130gA的饱和溶液,升温到40℃时,至少需加入A物质的质量为____g才能变成饱和溶液;
④当A中混有少量B时,用____方法可以得到固体A.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学用语与含义相符的是( )
A. 3Al3+—— 三个铝离子带3个单位的正电荷 B. 2H2——两个氢气分子
C. 2H ——2个氢元素 D. S2-——硫元素的化合价为-2价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色粉末,可能由NaCl、Na2SO4、Na2CO3、MgCl2、FeCl3中的一种或几种组成。现做如下试验:①取少量粉末加水溶解,得到无色透明溶液;②取①中所得溶液少许加入NaOH溶液,无明显现象;③另取少量粉末,滴加稀盐酸,也无明显现象。请问:
(1)由实验①可知,原粉末中没有_________;实验②可证明原粉末中没有_________;实验③可证明原粉末中没有_________。(填化学式)
(2)根据上述实验,请判断原粉末中可能有的物质是___________________。
(3)为进一步探究原粉末中的成分,按下图试验:(提示:在AgNO3、BaCl2、Ba (NO3)2中选择两种作为A、B试剂,且A、B的阳离子不同)

用化学式填写:粉末成分________________;试剂A__________;试剂B__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黑火药是我国四大发明之一,距今已有一千多年的历史。黑火药爆炸原理可用下式表示:2KNO3 + 3C + S =====X + N2↑ + 3 CO2,根据质量守恒定律推断X的化学式为
A. CO B. K2S C. NO D. SO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com