

分析 (1)根据氢氧化钠溶液和硫酸铜反应解答;
(2)根据题中信息分析解答;
(3)根据
解答 解:
(1)氢氧化钠溶液和硫酸铜反应,氢氧化钠被消耗,制作碱处理茶渣时,忘记洗涤,结果会使碱处理茶渣得吸附率变大;
(2)根据题意可知:碱处理茶渣吸附铜离子效果最好,其他茶渣效果差不多.该结论存在明显的缺陷是:因为茶渣用碱处理中茶渣的种类不明确,实验次数只有一次;
(3)碱处理茶渣的吸附能力还受到到温度、PH值等因素的影响,茶渣最适宜吸附的温度在30°C左右;如果要找到茶渣最适宜吸附的温度.可行性操作是:设置不同间距的温度,再次进行实验.
答案:
(1)变大
(2)因为茶渣用碱处理中茶渣的种类不明确,实验次数只有一次
(3)在30°C左右; 设置不同间距的温度,再次进行实验
点评 在解此类题时,首先分析题中的反应流程,然后结合学过的知识、题中所给的知识以及题中的问题进行逐一的解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 编号 | 0.25%淀粉 溶液(ml) | 蒸馏水(ml) | 0.9%NaCl 溶液(ml) | 0.9%CuSO4溶液(ml) | 唾液溶液(ml) | 加入3滴 碘液后现象 |
| 1 | 3 | 2 | - | - | - | 变蓝色 |
| 2 | 3 | 1 | - | - | 1 | 不变蓝 |
| 3 | 3 | - | 1 | - | 1 | 不变蓝 |
| 4 | 3 | - | - | 1 | 1 | 变蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 浓硫酸可以干燥氨气 | |
| B. | 不能直接品尝实验室药品的味道 | |
| C. | 误食重金属盐,可服牛奶或鸡蛋清解毒 | |
| D. | 液化气起火,迅速关闭阀门,以断绝可燃物的来源 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
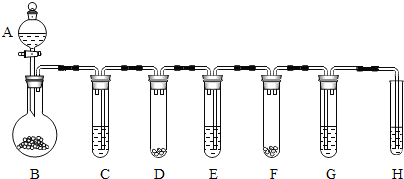
 小科利用日用品制作了一套如图装置,用来测定粗锌中锌的质量分数.
小科利用日用品制作了一套如图装置,用来测定粗锌中锌的质量分数.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| B. | 硫在氧气中燃烧发出蓝紫色火焰,产生刺激性气味的气体 | |
| C. | 铁在氧气中燃烧,火星四射,生成黑色固体 | |
| D. | 红磷在空气中燃烧产生大量白雾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com