
| A. | pH=1.2的工业废水 | B. | pH=5.6的雨水 | ||
| C. | pH=7.0的蒸馏水 | D. | pH=8.5的苏打水 |
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 金属材料与人类的生产和生活密切相关.
金属材料与人类的生产和生活密切相关.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
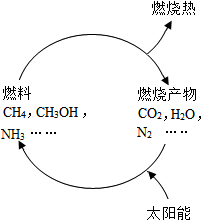 (1)从能源是否可以循环再生的角度看,可以将能源分为可再生能源和不可再生能源,譬如煤、石油、天然气就是不可再生能源.日益严峻的能源危机促进了可再生能源的研究.有专家提出:如果能够利用太阳能使燃料燃烧产物,如CO2、H2O、N2等重新组合(如图),可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为热能.
(1)从能源是否可以循环再生的角度看,可以将能源分为可再生能源和不可再生能源,譬如煤、石油、天然气就是不可再生能源.日益严峻的能源危机促进了可再生能源的研究.有专家提出:如果能够利用太阳能使燃料燃烧产物,如CO2、H2O、N2等重新组合(如图),可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为热能.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食盐溶于水后,溶质以离子的形式存在 | |
| B. | 将少许泥土加入水中,搅拌后得到浑浊的液体 | |
| C. | 在75%的消毒酒精中,溶质是酒精,溶剂是水 | |
| D. | 用洗头膏洗去头发上的油污,利用了溶解作用 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com