
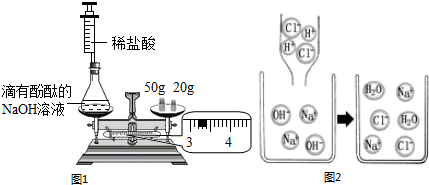
| 80 |
| x |
| 44 |
| y |
| 106 |
| 15.9g |
| 12g |
| 60g |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室需要质量分数为10%的NaCl溶液,配制质量分数为5%的氯化钠溶液.
实验室需要质量分数为10%的NaCl溶液,配制质量分数为5%的氯化钠溶液.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是市售某牙膏的部分说明.其主要成分是单氟磷酸钠(Na2PO3F),它是牙膏的常用添加剂,实验表明,单氟磷酸钠的质量分数达到0.76%--0.80%时,防龋齿效果较好.(②③小题计算结果精确到0.01%)
如图是市售某牙膏的部分说明.其主要成分是单氟磷酸钠(Na2PO3F),它是牙膏的常用添加剂,实验表明,单氟磷酸钠的质量分数达到0.76%--0.80%时,防龋齿效果较好.(②③小题计算结果精确到0.01%)查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com