
【题目】下表为元素周期表中某一周期元素的原子结构示意图。请回答下列问题:
元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
原子结构示意图 |
|
|
|
|
|
|
|
|
(1)氯离子的结构示意图为_____。
(2)下列说法正确的是_____(填序号)。
A 具有相对稳定结构的原子是氩
B 钠元素与氯元素形成的化合物是由分子直接构成的物质
C 镁离子失去电子形成原子
D 质子数决定元素种类,故质子数相等的微粒,一定是同种元素
(3)上表微粒中,与碳有相似化学性质的元素是_____。
(4)硫和地壳中含量最高的金属元素形成的化合物的化学式是_____。
【答案】 A 硅元素或
A 硅元素或![]()
![]()
【解析】
(1)由图中氯原子结构示意图可知,最外层电子数为7,容易得到1个电子形成稳定结构,形成氯离子,则氯离子的结构示意图为 。
。
(2)结合表格中元素周期表中第三周期元素的原子结构示意图可知:
A、第三周期的元素原子核外都有3个电子层,最外层电子数为8的具有相对稳定的结构,则具有相对稳定结构的原子是氩,A选项说法正确,符合题意;
B、钠原子最外层电子数为1,容易失去1个电子形成稳定结构,形成钠离子,氯原子最外层电子数为7,容易得到1个电子形成稳定结构,形成氯离子,因此钠元素与氯元素形成的化合物是由离子直接构成的物质,B选项说法不正确,不符合题意;
C、镁离子核电荷数为12,核外电子总数为10,得到2个电子形成镁原子,C选项说法不正确,不符合题意;
D、具有相同核电荷数或质子数的一类原子统称为元素,则质子数决定元素种类,但是质子数相等的微粒,不一定是同种元素,因为微粒包括原子、离子和分子,例如氩原子的质子数为18,硫化氢、氯化氢分子的质子数也为18,不能说分子与原子是同种元素,D选项说法不正确,不符合题意。故选A。
(3)原子的最外层电子数相同,元素的化学性质相似,碳原子的原子结构示意图为 ,最外层电子数为4,上表微粒中,最外层电子数为4的是硅原子,与碳有相似化学性质的元素是硅元素或
,最外层电子数为4,上表微粒中,最外层电子数为4的是硅原子,与碳有相似化学性质的元素是硅元素或![]() 。
。
(4)硫原子最外层电子数为6,容易得到2个电子形成稳定结构,形成硫离子![]() ,地壳中含最高的金属元素为铝元素,铝原子最外层电子数为3,容易失去个3电子形成稳定结构,形成铝离子
,地壳中含最高的金属元素为铝元素,铝原子最外层电子数为3,容易失去个3电子形成稳定结构,形成铝离子![]() ,则硫元素与铝元素形成的化合物的化学式是
,则硫元素与铝元素形成的化合物的化学式是![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】根据下列实验装置图回答问题:
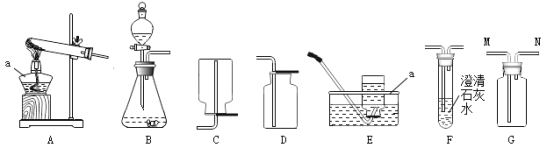
(1)写出图中标为a的仪器名称_______________。
(2)实验室用高锰酸钾制取氧气应选用的发生装置为_______________(填字母序号),写出该反应的化学方程式_______________,若用E装置来收集氧气,集满气体的集气瓶移出水面后应____________(填“正放”或“倒放”)在桌面上。
(3)实验室利用大理石和稀盐酸反应制取二氧化碳,该反应的化学方程式_______________,可选用B装置,该装置使用分液漏斗的优点是______________。
(4)实验室可利用装置F来检验生成的二氧化碳,其现象为_______________,请写出有关的化学方程式_______________。
(5)如果用G装置收集二氧化碳,气体应从_____________(填 “M”或“N”)端管口通入。
(6)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体。甲烷的密度比空气小,不溶于水。制取甲烷的发生装置可选用_______________(填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示为实验室中常见的气体制备和收集装置。

请回答下列问题:
(1)实验室用氯酸钾和二氧化锰制取氧气,应选用发生装置___(填标号),反应的化学方程式为_______。欲使用装置E排水法收集氧气,先将瓶中装满水,再将气体从____(填“a”或“b”)端通入。若用装置D收集氧气,验满的方法是_____。
(2)实验室用石灰石和稀盐酸制取二氧化碳,若选用C作发生装置,你认为选用C的优点是___________。
(3)已知一氧化氮气体难溶于水,在空气中易与氧气发生反应,则收集一氧化氮气体时应选用图中装置________(填标号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某硫酸铜溶液的质量分数,小杨同学取50.0g样品置于烧杯中,逐滴加入氢氧化钠溶液,加入氢氧化钠溶液质量和生成沉淀质量的关系如下图所示。请计算:
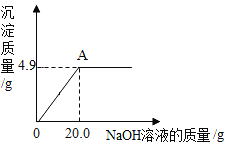
(1)NaOH的相对分子质量_______。
(2)硫酸铜刚好完全反应时,所得溶液的质量_______。
(3)硫酸铜溶液中溶质的质量分数是多少?(写出计算过程)_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关溶液的说法中正确的是( )
A.降低温度,KNO3溶液一定析出晶体
B.饱和溶液一定比不饱和溶液浓
C.在20 °C时,100g 氯化镁饱和溶液中含有12g氯化镁,则20°C时氯化镁的溶解度为12g
D.溶质的质量分数为10%的氢氧化钡溶液中溶质质量与溶剂质量的比为1:9
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用。电瓶的正极材料是二氧化铅(PbO2), 负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下:![]() 。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
(1) PbO2中铅元素与氧元素的质量比为_____。
(2)若用86.4%的浓硫酸来配制该稀硫酸1200克,需要加水多少克?_____
(3)假如某个电瓶中内装36%的稀硫酸1200克,当有414克的铅恰好反应完时,求反应后溶液中硫酸的质量分数_____(最后结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量![]() 和
和![]() 的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是
的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是

A.c点溶液中溶质为![]()
B.a点溶液中的溶质有2种
C.b~c段,溶液颜色逐渐加深
D.取d点的固体,加入稀盐酸,无气泡产生
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲转化为丙的微观过程。下列说法不正确的是
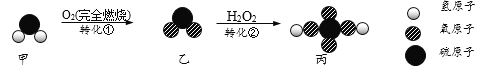
A. 反应前后原子种类不变 B. 转化①中甲和O2反应的分子个数比为1:1
C. 转化②是化合反应 D. 丙中氢、硫、氧元素的质量比为1:16:32
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如表:
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 13.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 1.0 | 7.2 | 8.8 | a |
下列判断错误的是( )
A. 该化学反应的反应物有两种
B. 表中a的值为2.8
C. X中含有氢元素
D. 该反应属于氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com