
【题目】2018年5月9日,我国“高分五号”卫星发射成功。“高分五号”是我国首颗对大气中二氧化硫,二氧化氮、二氧化硫,甲烷等多个环境要素进行监测的卫星。

(1)高氯酸钾(KClO4)可用作固体火箭燃料,其中氯元素的化合价为______。
(2)“高分五号”用钛镍形状记忆合金制作卫星天线。钛镍合金是______(“化合物”或“混合物”)。如图是镍的原子结构示意图,X的数值是______。
(3)镍和铁一样也能与稀盐酸反应生成氢气,同时生成NiCl2,请设计实验比较镍与铁的金属活动性强弱______。
(4)作为新时代的主人翁,你对防治大气污染有哪些建议和好的举措,请简要说出一点______。
【答案】+7 混合物 2 将铁丝伸入NiCl2溶液中,铁能将镍置换出来,说明了铁比镍活泼。 使用清洁的能源、植树造林等
【解析】
(1)在高氯酸钾(KClO4)中,由钾元素的化合价为+1价,氧元素的化合价为-2价,可推出其中氯元素的化合价为+7。
(2)钛镍合金是由不同种物质组成的,属于混合物;在原子中核内质子数等于核外电子数,可推出X的数值是:28-2-8-16=2;
(3)通过金属与盐溶液的反应可以比较两种金属的活动性,所以实验比较镍与铁的金属活动性强弱的方案是:将铁丝伸入NiCl2溶液中,铁能将镍置换出来,说明了铁比镍活泼。
(4)防治大气污染的建议和好的举措有很多,例如:使用清洁的能源、植树造林等。
故答为:(1)+7;(2)混合物,2;(3)将铁丝伸入NiCl2溶液中,铁能将镍置换出来,说明了铁比镍活泼。(4)使用清洁的能源、植树造林等。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】铝合金是目前广泛使用的合金材料,已知某铝合金由Al、Fe、Cu三种金属构成,为了测定各种金属含量,取12.5g合金样品与盐酸反应,消耗浓盐酸(质量分数36.5%)100g。另取12.5g合金样品与氢氧化钠溶液反应,消耗含氢氧化钠12g的溶液40mL。
已知:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Fe,Cu均不与氢氧化钠溶液反应。
请问:(1)12.5g样品中含铝多少克?
(2)铜在合金中所占的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在圆底烧瓶中充满CO2,通过注射器向瓶中分别加入同体积水和NaOH溶液。利用传感器得到的气压变化如下图所示。下列说法错误的是( )
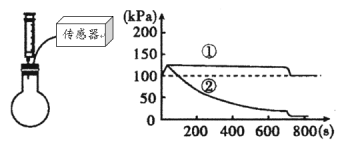
A. 800s时,曲线①表示的溶液显酸性
B. 曲线②NaOH与CO2发生的反应
C. 刚开始压强增大是因为加入液体后气体被压缩
D. 同体积水和NaOH溶液,吸收的CO2一样多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】清华大学研究人员成功研制出一种纳米纤锥催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图(图中的微粒恰好完全反应)所示。下列说法正确的是( )
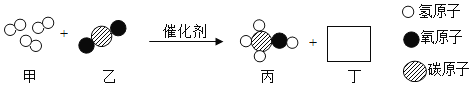
A. 反应前后原子和分子的种类都发生改变
B. 该反应属于置换反应
C. 甲是单质,乙、丙、丁均为化合物
D. 该纳米纤维在反应前后化学性质发生了改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年内,吉林德惠宝源丰禽业有限公司发生特大火灾,引发“液氨罐”爆炸,造成多人伤亡.液氨也是氨气加压降温液化而成的,氨气(NH3)在通常情况下是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气,反应的化学方程式为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O.请根据如图所示回答:
CaCl2+2NH3↑+2H2O.请根据如图所示回答:
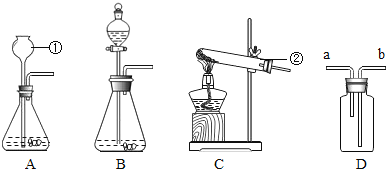
(1)写出所标仪器的名称:①是 ,②是 .
(2)A、B两装置均可供实验室制取氧气,与A装置相比较,用B装置的优点是 .写出用B装置制取氧气的化学方程式 ,若用D装置来干燥氧气,则D内应装的干燥剂是 (选填“固体氢氧化钠”或浓硫酸).
(3)在不做改动的情况下,C装置 (选填“能”或“不能”)用来做氢气还原氧化铜的实验.
(4)实验室制取氨气应选择的发生装置是 (填写装置对应的字母).
(5)若用D装置来收集氨气,则气体应从 (选填“a”或“b”)通入.
(6)若选用KClO3和MnO2加热制取氧气,要从反应后的残余物中回收MnO2,以下①﹣④的操作步骤,你认为正确的顺序是 .
①洗涤 ②烘干 ③过滤 ④溶解
A.④③①② B.④③②① C.①②④③ D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A,B,C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )
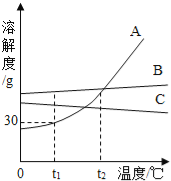
A. t1℃时,A的饱和溶液65g中含有溶剂50g
B. 将t2℃A,B,C三种物质的饱和溶液降温至t1℃时,C溶液中溶质的质量分数保持不变
C. 在t2℃,A,B两种溶液中溶质的质量分数相同
D. 要从B溶液中得到B,通常可采用蒸发溶剂使其结晶的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以菱锌矿(主要成分是ZnCO3,杂质为Fe2O3、FeO、CuO)为原料制备七水硫酸锌(ZnSO47H2O),同时得到铁红副产品,其工艺流程如图,回答下列问题:
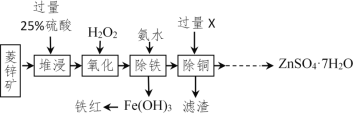
(1)“堆浸”前将菱锌矿粉粹成细颗粒,其目的是_____________________;
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要98%的硫酸质量为_____g(列出算式即可),需要用到的玻璃仪器有胶头滴管、玻璃棒、烧杯和________,此处玻璃棒的作用是____;
(3)物质X是___________,除铜时发生的反应属于________________反应(填基本反应类型);
(4)“氧化”中加入H2O2的目的是在硫酸的作用下将溶液中的FeSO4转化成Fe2(SO4)3,反应的化学方程式:_______________。
(5)流程中获得七水硫酸锌前省略的操作是______________、冷却结晶、过滤、洗涤和低温烘干;
(6)除铁过程中,反应温度、溶液pH对除铁效果均有影响,为探究除铁的最佳效果,某同学做了以下的实验并记录了相关数据,请回答问题:
编号 | 反应温度/℃ | 溶液pH | 除铁率/% |
a | 30 | 2 | 91.5 |
b | 30 | 2.5 | 93.3 |
c | 40 | 2.5 | 95.1 |
d | 40 | 3.1 | Y |
e | 50 | 3.1 | 99.5 |
①实验____和实验_____对比,得到的结论为其他条件不变时,反应温度增大,除铁率提高;
②实验a和实验b对比,得到结论是____________;
③表中Y的值可能为_____________(填编号)
A 93.4 B 94.1 C 97.8 D 99.6
④最佳的除铁条件为反应温度______℃,溶液pH_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁在国产大飞机C-919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图像如下),过滤,称量滤液质量为147g,求:
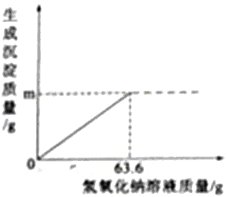
(1)图像中m=_____g。
(2)滤液中溶质的质量分数是____________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com