
【题目】元素周期表是学习和研究化学的重要工具。下面是元素周期表的部分信息:
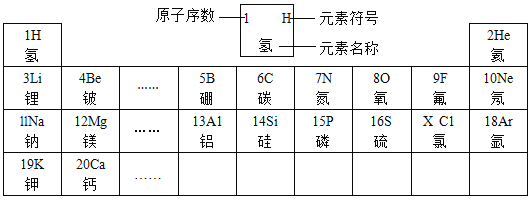
认真分析信息,回答:
(1)地壳中含量最多的元素的原子序数是___________;
(2)分析上表规律,可推知,表中X=____________;
(3)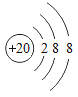 表示的是(写粒子符号)___________;
表示的是(写粒子符号)___________;
(4)写出一个由11、17号两种元素组成的化合物的化学符号_________。
科目:初中化学 来源: 题型:
【题目】取一定量的木炭在氧气中燃烧,生成23.2 g气体(氧气已完全反应)。将气体通入过量的澄清石灰水中,生成40 g沉淀。
计算:
(1)生成气体的成分及质量。
(2)生成气体中碳元素的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:A~H是初中化学中的常见物质,A与B的组成元素相同且都是液体,D能供给呼吸,E能使澄清石灰水变浑浊,F易与血红蛋白结合使人体中毒,且F和E组成元素相同,G与H都是黑色固体。它们有如下的转化关系(部分条件已省略)
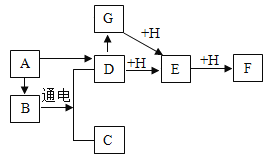
(1)写出A与F的化学式:A _____F _______
(2)写出A→B的化学方程式_________,该反应类型属于 _______,写出反应B→D+C化学方程式______,写出D+H→E化学方程式________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化石燃料在当今社会能源中担当“主角”。
(1)化石燃料包括煤、________和天然气。
(2)天然气是生活中常用的燃料,其主要成分充分燃烧的化学方程式是________。
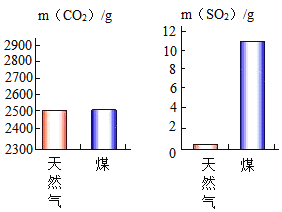
(3)分别充分燃烧1000g天然气、煤所产生的![]() 和
和![]() 气体的质量如下图所示,根据图示分析,则________产生的气体更易导致酸雨。
气体的质量如下图所示,根据图示分析,则________产生的气体更易导致酸雨。
(4)洁净的空气对人类非常重要。下列做法不利于保护大气的是________(填序号)
A燃煤取暖改为天然气供暖 B积极植树造林
C工业废气净化后排放 D焚烧落叶和垃圾
(5)为减少污染、提高煤的利用率,也可将煤与水蒸气在高温下反应转化为两种常见的可燃性气体,该反应的化学方程式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列所给的各反应属于分解反应的是( )
A.铁+氧气![]() 四氧化三铁B.石蜡+氧气
四氧化三铁B.石蜡+氧气![]() 二氧化碳+水
二氧化碳+水
C.氢氧化钠+盐酸![]() 氯化钠+水D.高锰酸钾
氯化钠+水D.高锰酸钾![]() 锰酸钾+二氧化锰+氧气
锰酸钾+二氧化锰+氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国科学家屠呦呦利用乙醚从黄花高汁液中提取出抗疟特效药青蒿素,从而获得了2015年诺贝尔医学奖已知青蒿素的化学式为C15H22O5,下列叙述正确的是( )
A.青蒿素属于混合物
B.1个青蒿素分子中含有11个氢分子
C.青蒿素由15个碳原子,22个氢原子,和5个氧原子构成
D.青蒿素中氢元素质量分数最小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究空气中氧气的体积含量的实验装置如图所示,实验步骤如下:
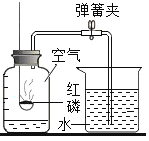
① 在集气瓶中加入少量水,并做好标记。将标记以上的部分按体积分为5等份;
② 检查装置的气密性;
③ 在燃烧匙内装入足量的红磷,将导管上的止水夹夹紧。在酒精灯上点燃红磷,立即伸入集气瓶中,并塞紧瓶塞;
④ 充分反应后,待集气瓶冷却到室温后打开止水夹。
请你根据实验回答下列问题:
(1)步骤④中打开止水夹后观察到的实验现象为____________________;
(2)实验得出的结论是___________________;
(3)该实验还可以推出氮气的性质有__________________(写出一条即可);
(4)确保该实验成功的关键是(写出两条即可)____________、___________
查看答案和解析>>
科目:初中化学 来源: 题型:
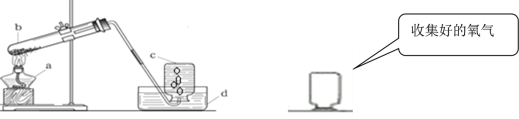
【题目】下图是某同学用高锰酸钾制取氧气时的装置图,请根据图回答:
(1)图中收集氧气的方法是:_________,能用此方法收集是因为氧气_______________。
(2)请指出图中标注仪器的名称: b__________;c_________;d_________。
(3)图中装置有三处最明显的错误,请指出并说明会有什么不良后果:
①._________,不良后果:_____________。
②._________,不良后果:___________。
③.__________,不良后果:____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纳米级Cu2O 因具有优良的催化性能备受关注.某兴趣小组开展了系列研究.
Ⅰ:纳米级Cu2O 的用途研究
(查阅资料)
②氨气是一种有刺激性气味的气体,在高浓度氧气中才能燃烧,生成氮气和水.
③在纳米级Cu2O的催化作用下,氨气与氧气在一定温度下发生以下化学反应生成NO ,工业上用NO 制备硝酸、氮肥等化工产品.
(实验1)
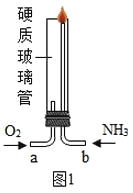
设计图1的实验装置验证氨气在氧气中燃烧:将过量的氧气与氨气分别从a 、b 两管进气口通入,并在b 管上端点燃氨气.实验组需先通入氧气,后通入氨气,理由是_____.
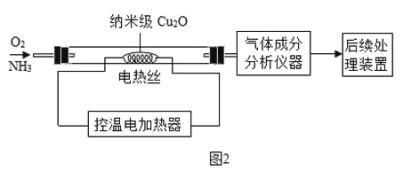
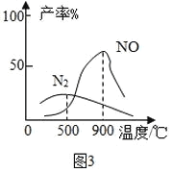
(实验2)设计如图2实验装置,根据气体成分分析数据,同学们绘制了曲线图(见图3),发现在纳米级Cu2O 的催化作用下,300℃时以生产_____为主.若利用后续处理装置模拟硝酸的工业制法,最好将电热丝的温度控制在_____℃左右.
Ⅱ纳米级Cu2O的制备研究
利用某些特殊的细菌,在一定条件下将某岩石中的不溶性硫化铜(CuS )转化为可溶性硫化铜,进得纳米级Cu2O ,其流程如图4:
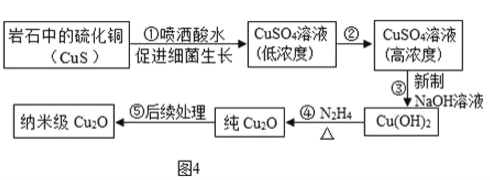
(1)在细菌作用下,岩石中的硫化铜(CuS )与空气中的氧气反应生成硫酸铜,反应的符号表达式为_____.
(2)③中观察到的现象是_____.
(3)物质所含元素化合价发生改变的反应称为氧化还原反应,在图4流程中,主要反应属于氧化还原反应的步骤是_____,Cu2O中铜元素的化合价是_____.
(4)经测定该岩石由硫化铜(CuS)和其他不含铜元素的物质组成.现用2000g该岩石制得43.2g纯氧化亚铜(Cu2O),该纯氧化亚铜(Cu2O)中铜元素的质量是_____g.若制得氧化亚铜Cu2O)的过程中,铜元素的总损耗为20%,通过计算确定该岩石中硫化铜(CuS)的质量分数_____(请写出计算过程).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com