
【题目】金属汞(Hg)滴到铝板上,能溶解铝,形成液态合金(铝汞齐),使表层的铝原子浓度变低,从而使铝与氧气反应时无法形成致密氧化膜,内部的铝原子不停地与氧气反应(出现“长毛”现象如图),变化过程的微观模型如图。

(1)铝汞齐属于____(填“单质”、“化合物”和“混合物”)。
(2)写出图9中铝被氧化的化学方程式____。
(3)若在表面清洁的铝板上滴上HgCl2溶液,也会出现“长毛”现象。该现象说明铝的金属活泼性比汞____(填“强”或“弱”)。
科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映的变化关系是
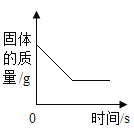
A. 加热高锰酸钾制氧气,随着反应的进行试管内固体的质量变化
B. 往铁粉中逐滴加入硫酸铜溶液,混合物中固体总质量变化
C. 往一定量的石灰石中逐滴加入稀盐酸产生二氧化碳的体积
D. 加热氯酸钾和二氧化锰制取氧气,固体中锰元素质量分数随时间的变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组同学做了如下实验,验证质量守恒定律。
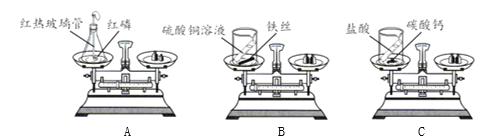
(1)实验A中发生反应的化学方程式为_______。
(2)上述实验中,不能用于验证质量守恒定律的是______(填实验序号),其原因是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碘化钾(KI)保存不当会变质。实验小组进行以下实验探究KI变质的因素。
(提出问题1) KI变质的条件是什么?
(查阅资料)
① KI为白色粉末,暴露在空气中或久置会被氧化为碘(I2)而泛黄变质。
② 碘水中含较多KI时,滴加淀粉溶液显紫色或蓝紫色
(进行实验)分别取适量KI于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
实验1 | 实验2 | 实验3 | 实验4 |
|
|
|
|
固体变潮、表面变微黄 | 固体无明显现象 | 固体变潮、无其他明显现象 | 固体变潮、表面变黄 |
继续实验:取实验1中少量微黄固体溶解,加入淀粉溶液,溶液变紫色。
取实验4中少量黄色固体溶解,加入淀粉溶液,溶液变紫色。
(解释与结论)
(1)实验3的目的是_______。
(2)对比实验_______,可以得出KI变质一定与水有关。
(3)从上述实验可推知,KI变质的条件是_______。
(4)CO2的作用是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实践活动中,化学小组的同学用下图所示装置进行如下实验。(说明:暖宝宝的原料中有铁粉、碳粉和少量氯化钠)

实验步骤 | 主要操作 | 实验现象 | 结论与解释 |
I | 按上图所示装置连接仪器。关闭止水夹,打开分液漏斗活塞,向分液漏斗中加入水 | ________________。 | 装置气密性良好。 |
II | 用集气瓶收集一瓶氧气,并向其中加入暖宝宝的原料。塞进橡胶塞,在分液漏斗和烧杯中分别加入水和稀盐酸,放置一段时间 | 集气瓶内无明显现象 | |
III | 打开止水夹和分液漏斗活塞,向集气瓶中加入少量水,关闭止水夹。 | 观察到部分液体变为棕红色。 | 暖宝宝原料中的部分铁被氧化 |
IV | 打开止水夹 | 稀盐酸流入集气瓶中,并有气泡产生 | 稀盐酸倒吸入集气瓶中的原因是__________。 产生气泡的原因是(用化学方程式表示)________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】三氯化铁(FeCl3)用于金属蚀刻等。化学兴趣小组想把铁燃烧产物转化成FeCl3。 请根据装置如图回答问题:
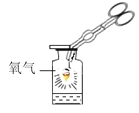
(1)写出铁在氧气中燃烧的化学方程式____。
探究一:铁丝在氧气中燃烧为什么会火星四射?
(查阅资料)
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时 的现象 | 剧烈燃烧,发白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 大量火星 |
(2)由上表可知铁丝燃烧能否产生火星与该物质____有关。
探究二:铁丝燃烧时溅落的黑色物质的成分
(查阅资料)Fe3O4能与稀盐酸反应生成可溶于水的FeCl2和FeCl3,溶液呈黄色。反应的方程式为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O。
(实验探究)将溅落的黑色物质碾碎,加入足量稀盐酸。
(3)观察到黑色固体逐渐溶解,溶液变成黄色,同时有气泡生成,写出产生气泡的化学方程式____。
(实验结论)
(4)由以上现象可得,铁燃烧时溅落的黑色物质含有____。
(5)反应完全后,发现还有固体残渣,你认为该残渣可能是____。
探究三:三氯化铁的制取与应用
(查阅资料)①通入Cl2可将FeCl2溶液转化成FeCl3溶液。
②废铜电路板上的铜与FeCl3溶液反应生成FeCl2和CuCl2。
③FeCl3能使KSCN溶液变红色,而FeCl2与CuCl2不能。
将探究二所得剩余物,通过分步实验,操作过程中氯化铁的质量变化如图16:
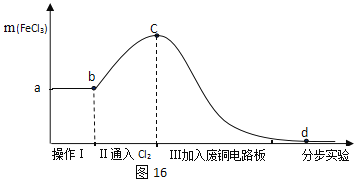
(6)操作Ⅰ可除去固体残渣,该操作的名称是____。
(7)通过操作Ⅱ,氯化铁的质量增加的原因是____(用化学方程式来表示)。
(8) 通过操作Ⅲ,得到d溶液,检验d溶液中是否还含有氯化铁的方法是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~L是初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中G是大理石的主要成分,A和I为红色固体,B、D和L为气体。请回答下列问题:
(1)反应①的化学方程式为_____。
(2)E的组成元素在化合物中常呈现的化合价有_____。
(3)图中涉及的反应中属于置换反应的是_____(填序号)。
(4)上述转化中,B和L表现出相似的化学性质是_____。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某反应的微观示意图,其中“![]() ”和“
”和“![]() ”表示不同元素的原子。下列说法正确的是
”表示不同元素的原子。下列说法正确的是
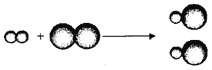
A. 反应前后元素的种类发生改变
B. 反应前后分子种类没有改变
C. 该反应属于置换反应
D. 参加反应的两种分子个数比为1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化碳能与过氧化钠(Na2O2,淡黄色固体)在常温下反应产生氧气,并生成碳酸钠,且伴有能量的释放。
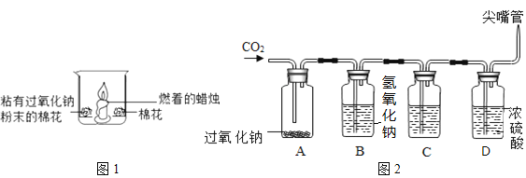
(1)如图1所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:①______;②粘有过氧化钠的棉花燃烧;③未粘有过氧化钠的棉花不燃烧。通过上述实验的对比分析,写出产生现象②的原因______。
(2)为验证二氧化碳能与过氧化钠在常温下反应产生氧气,设计了图2实验(氢氧化钠溶液能与二氧化碳反应;浓硫酸有吸水性,且既不与二氧化碳反应,也不与氧气反应)。
①B瓶的作用是吸收未反应完的二氧化碳,C瓶的作用是检验二氧化碳是否被B瓶吸收完,则C瓶中盛放的溶液是______(写名称)。
②为验证过氧化钠和二氧化碳反应生成氧气,采用的验证方法是______。
③写出过氧化钠和二氧化碳反应的化学方程式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com