
【题目】(1)经过一年化学学习.你可能已经喜欢上了在实验室做实验的感觉。让我们一起再来做实验吧
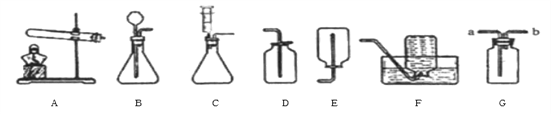
①实验室用装置A制取氧气,若要收集一瓶较纯净的氧气,应选择装置_____(填字母)若用G装置收集氧气,验满方法为_______________;
②通常情况下,乙炔是一种密度比空气略小.且难溶于水的气体。实验室常用块状碳化钙固体和水反应制取乙炔,该反应在常温下进行且非常剧烈。实验室欲制取乙炔,最好选用的装置组合是________(填字母),该发生装置的优点为__________。
(2)化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸 逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如下图所示。
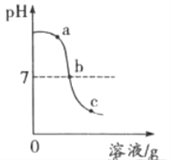
【提出问题】导致溶液pH变化的原因是什么?
【查阅资料】
①溶液的pH是由H+或OH-浓度决定,H+浓度越大,pH越小;OH-浓度越大,pH越大。
②溶液中某种离子浓度非常小时,可忽略不计。
【作出猜想】
猜想Ⅰ:溶液pH变化是因为氢氧化钠溶液被稀释。
猜想Ⅱ:溶液pH变化是因为发生了化学反应。
【进行实验】同学们分成两组分别进行实验。
甲组:同学们将4mL2%的稀硫酸换成__________,逐滴滴加到2mL2%的氢氧化钠溶液中,并测得溶液的pH始终大于7,说明猜想Ⅰ不合理。
乙组:同学们分别取a、b、c三处溶液进行实验。
实验操作 | 实验现象 | 实验分析 |
取适量a处溶液于试管中,加入镁条 | 无气泡产生 | 溶液中几乎不含___(填离子符号) |
取适量b处溶液于试管中,加入紫色石蕊溶液 | _________ | 溶液中几乎不含H+和OH- |
取适量c处溶液于试管中,加入___________ | ___________ | 溶液中几乎不含OH- |
【实验结论】猜想Ⅱ合理。
【知识拓展】从微观角度分析,中和反应的实质是_________。
【答案】 F 将带火星的木条放在b处 观察是否复燃 C F 能控制化学反应速率 4mL水(或4mL硫酸钠溶液等) H+石蕊溶液不变色 硫酸铜溶液(或氯化铁溶液等) 无沉淀产生 H+和OH-反应变成H2O(或H++OH-=H2O)
【解析】(1)因为氧气的密度比空气大,可以用向上排空气法收集,即用D装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;氧气密度比空气大,则应从a端进气,短管便于排尽空气,验满的方法是将带火星的木条放于b管处,观察木条是否复燃;(2)用块状固体碳化钙与水反应制备乙炔,不需加热,属于固液常温型,注射器可逐滴滴加液体,从而可控制反应速率,制取平稳的氧气流,乙炔密度比空气略小,难溶于水,所以最好用排水法收集,实验室欲制取乙炔,最好选用的装置组合是CF;【进行实验】猜想①是溶液pH变化是因为氢氧化钠溶液被稀释,故可以改成加入4mL水;加入镁条,无气泡产生,说明不含有酸,故不含有氢离子;溶液中几乎不含有H+和OH,故加入石蕊试液不会发生颜色的变化,故填:石蕊溶液不变色;氢氧根离子能与铜离子结合产生硫酸铜沉淀,故加入硫酸铜溶液根据无沉淀产生能证明不含有氢氧根离子,故填:硫酸铜溶液;无沉淀产生;【实验拓展】中和反应的实质是H+和OH反应变成H2O。


科目:初中化学 来源: 题型:
【题目】小明同学对家中久置的袋装固体食品防腐剂的成分产生了兴趣(品名和成分如图所示),于是和同学一起,设计实验进行探究:

[提出问题]久置固体食品防腐剂的成分是什么?
[查阅资料]铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
[作出猜想]久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 。
[实验探究]甲同学的探究方案如下表:
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有_______和氢氧化钙。此过程的化学方程式_______。 |
(2)另取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有Fe ,一定不含 Fe2O3 |
(3)将步骤(2)中产生的气体通入到澄清的石灰水中 | ________ | 固体中一定含有CaCO3 |
[交流与反思]
(1)“504双吸剂”中的铁粉可以吸收空气中的_______、______。
(2)实验操作(2)的实验现象里“有大量无色气体产生”, 根据甲同学的整体探究方案推测,无色气体的成分是一定含有______,可能含有________。
(3)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是______。
(4)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组设计了测定纯碱样品(含NaCl杂质)中碳酸钠质量分数的实验方案.请回答下列问题:
(1)碳酸根离子沉淀法.实验步骤:
①用托盘天平称取样品w克放入烧杯中加水溶解;
②加入足量BaCl2溶液充分反应.证明反应后BaCl2剩余的方法是____________;
③过滤、洗涤、干燥、称量沉淀的质量为mg;
④样品中碳酸钠的质量分数为_________________.
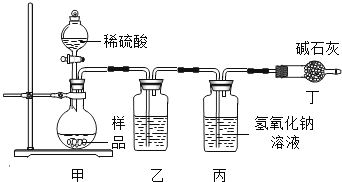
(2)气体法.学习小组利用如图装置测定样品中碳酸钠的质量分数.
①实验装置乙中盛放的试剂为_________,装置丁的作用是________________.
②学习小组通过测量丙装置实验前后的质量.确定二氧化碳的质量.实验中滴加稀硫酸的速度过快,产生的气流过急.会导致测得样品中碳酸钠的质量分数________(填写“偏高”“偏低”或“不变”).
(3)测氯化钠法.请你完成下列实验方案:
称取一定质量的样品放入烧杯中加水溶解:_____________________________________;
过滤、洗涤、干燥、称量沉淀的质量;计算出氯化钠的质量,再得样品中碳酸钠的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CuCl2 是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上以辉铜矿(主要含有Cu2S、Fe2O3 及一些不溶性杂质)为原料制备 CuCl22H2O晶体的工艺流程如下:
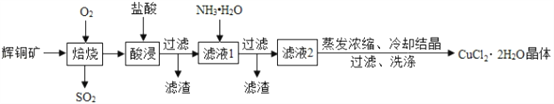
请回答下列问题:
(1)焙烧中生成黑色固体,反应的化学方程式为___________。
﹙2﹚酸浸时发生的化学方程式为__(写出一种)。为加快反应速率,以下措施无法达到目的的是___。
A.延长酸浸时间 B.将辉铜矿粉碎 C.适当增加盐酸浓度
(3)色光度是产品质量指标之一,合格 CuCl22H2O 晶体的色光度范围为﹣0.5~0.5,反应过程溶液pH对产率、色光度的影响。如下图所示,综合考虑制备时应控制pH的较合理范围是_________。
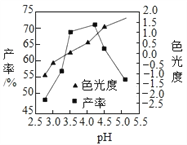
实验室用pH试纸测定溶液pH的操作方法是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将盛有等质量、等溶质质量分数的稀硫酸的两只烧杯,放在托盘天平(灵敏度较高)左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的铁和锌,待反应停止后(不考虑反应中水分挥发,不考虑空气成分参加反应),请判断,下列说法合理的是
A. 若天平失去平衡,指针一定偏向放锌的一边
B. 若天平仍保持平衡,烧杯中的铁一定没有剩余
C. 反应后两只烧杯中溶液的质量都比反应前的溶液质量减轻了
D. 放铁的一边产生的氢气一定比放锌的一边产生的氢气多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映所对应叙述关系的是
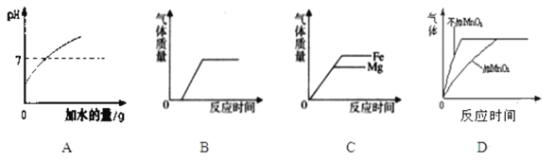
A. 向pH=2的硫酸中不断加水
B. 在久置的NaOH溶液中加盐酸
C. 分别向稀盐酸中加入等质量的Fe和Mg
D. 双氧水分解
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某稀硫酸和10克8%的氢氧化钠溶液的滴定实验中,溶液的pH变化如图所示:
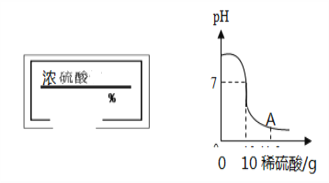
(1)A点溶液的溶质_________________(填化学式)
(2)计算所用的该稀硫酸的质量分数?_______________
(3)如果配制100克该稀硫酸所用图中浓硫酸的质量为10克,则图中浓硫酸的质量分数为_______(不写计算过程)
(4)图中的浓硫酸多次使用后,发现浓度变小了,原因是________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学利用下图所示装置探究燃烧的条件(热水温度远高于白磷着火点)。下列说法错误的是

A. 图①烧杯中水的温度应与②中相同
B. 图②中白磷燃烧,产生大量白烟
C. ①和③对比可以得出燃烧条件之一是“可燃物必须与氧气接触”
D. ②和③对比可以得出燃烧条件之一是“可燃物的温度必须达到着火点”
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图装置验证CO2的相关性质。
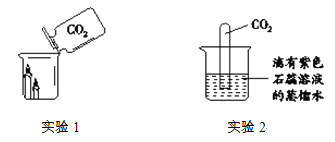
(1)实验1:观察到的实验现象是______。该实验说明CO2具有的性质是______。
(2)实验2:一段时间后,观察到的实验现象是______、______。该反应的化学方程式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com