
���� ���������ļ�������������������������������������0.2g�������������������п��������п�����ᷴӦ��������п��������������������������Ϊ0.2g����Ϸ�Ӧ�Ļ�ѧ����ʽ���ɷų�����������������Ʒ��п�����������������п����������п����������
��� �⣺��1�����ݽ������˳��ͭ�������Ӧ��п�����ᷴӦ��������п����������Ӧ�ķ���ʽΪ��Zn+H2SO4=ZnSO4+H2����
��2�����������غ㶨�ɿ�֪�����ļ�������������������������������������0.2g��
��μӷ�Ӧ����������Ϊy���μӷ�Ӧ��п����Ϊx��
Zn+H2SO4=ZnSO4+H2��
65 98 2
x y 0.2g
$\frac{65}{x}=\frac{98}{y}=\frac{2}{0.2g}$
y=9.8g��x=6.5g
��3��пͭ�Ͻ��У�п����������Ϊ��$\frac{6.5g}{10g}��$100%=65%��
��4��ϡ���������ʵ�����Ϊ9.8g��
��5����Ӧ��������Һ������=6.5g+100g-0.2g=103.5g
�𰸣�
��1��Zn+H2SO4=ZnSO4+H2����
��2��$\frac{65}{x}=\frac{2}{0.2g}$��
��3��65%��
��4��9.8��
��5��103.5g��
���� �����ؼ���Ҫ֪��ͭ�������Ӧ��ֻ��п�����ᷴӦ�������������п���������ٽ�һ�����м��㼴�ɣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
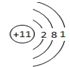
| A�� | ���ԭ������ | B�� | ��ʧ�������� | C�� | ԭ������ | D�� | Ԫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��˿��������ȼ���� | B�� | ʯ���ڿ�����ȼ�� | ||
| C�� | ����������������� | D�� | ��������Ͷ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���ʵ�Ӧ�� | ��ѧ����ʽ | ��Ӧ���� | |
| A | ��¯��������Ҫ��Ӧ | 3CO+2Fe2O3$\frac{\underline{\;����\;}}{\;}$4Fe+3CO2�� | �û���Ӧ |
| B | ���ˮ | 2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2�� | �ֽⷴӦ |
| C | ����Ȼ����ȼ�� | CH4+202$\frac{\underline{\;��ȼ\;}}{\;}$C02+2H2O | ���Ϸ�Ӧ |
| D | �Ƚ�ͭ�����Ļ�� | 2Ag+CuCl2�TCu+2AgCl | �û���Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ����������1 000g������������Ϊ4%������������Һ����ش��������⣻
ʵ����������1 000g������������Ϊ4%������������Һ����ش��������⣻�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com