
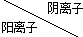
 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 没有白色沉淀产生 | 没有氢氧化钙 |
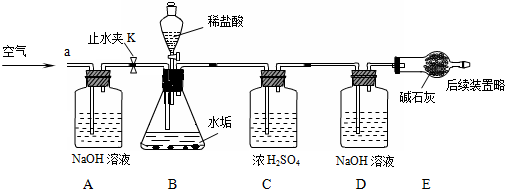
分析 【提出猜想】首先运用题中溶解性表分析得出提出猜想中的两个空;
【设计方案】实验1:根据氢氧化钙溶液能和碳酸钠反应生成碳酸钙沉淀进行解答;
【实验讨论】要测定二氧化碳的质量,必须保证装置气密性良好;可以根据反应前后装置D、E的质量差确定生成的二氧化碳的质量,进而确定水垢中是否含有碳酸镁,计算出所用的盐酸的质量分数,从而计算求出是否含有氢氧化镁;
实验3:根据装置D的增重判断生成的二氧化碳的质量为1.25g;
设水垢均为2.50g碳酸钙,根据方程式计算可生成的二氧化碳1.1g,所以含碳酸镁;
根据碳酸钙、碳酸镁、氢氧化镁与盐酸反应的方程式,分别计算它们2.50g消耗盐酸的质量,其中氢氧化镁消耗最多,其次为碳酸镁,假设2.50g全为碳酸镁,消耗盐酸56.8g,w>56.8g时,定有氢氧化镁.
解答 解:【提出猜想】由题中溶解性表知碳酸钙和氢氧化镁不溶于水,其余的氢氧化钙、碳酸镁微溶,碳酸氢钙和碳酸氢镁都溶于水,故水垢的主要成分中一定含有:CaCO3、Mg(OH)2故填:CaCO3;Mg(OH)2;
【设计方案】
实验1:氢氧化钙溶液能和碳酸钠反应生成碳酸钙沉淀,所以
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 没有白色沉淀产生 | 没有氢氧化钙 |
点评 即考查了实验也考查了根据化学方程式的计算,培养了学生实验分析能力和根据化学方程式计算能力及运用极值法解题的思想.本题考查了常见物质成分的推断,完成此题,可以依据物质的性质结合题干提供的信息进行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验装置 |  | 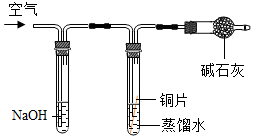 |  | 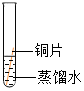 |
| 实验现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
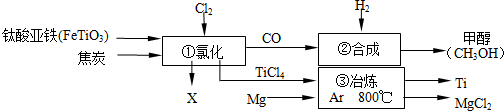
| A. | 钛酸亚铁(FeTiO3)中钛元素为+4价 | |
| B. | ①中反应为:2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,则X为FeCl3 | |
| C. | ③中氩气(Ar)作保护气,反应类型为置换反应 | |
| D. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com