
【题目】甲、乙、丙为初中常见物质,其转化关系如下图(“→”表示由一种物质转化成另一种物质,反应条件、部分反应物和生成物已略去)。
![]()
(1)若甲,乙、丙均含有同一种元素,甲为单质,乙、丙含有相同的两种元素,写出甲物质的用途:_____,则丙可能是_____。
(2)若甲、乙、丙均为含有钙元素的化合物,甲与水反应生成乙并放出大量的热,则甲→乙的化学方程式为_____,丙可能是_____(写一种)。
【答案】做导线(合理均可) CuSO4(合理均可) CaO+H2O═Ca(OH)2 CaCl2或CaCO3或CaSO4(填一个即可)
【解析】
(1)根据常见物质的性质和反应现象或条件以及题目中给出的要求进行分析推断,注意关键字眼,比如甲是单质,甲乙丙均含同一元素而乙、丙含两种相同元素,找出符合条件的物质即可;
(2)甲、乙、丙若都有钙元素,与水反应放热可知甲是氧化钙,在根据后续反应推断即可。
(1)根据题意甲必须是单质且甲乙丙含有同一种元素,乙、丙还必须含两种相同的元素,所以甲可以是Cu,铜和氧气在加热的条件下生成CuO,所以乙可以是CuO,CuO和硫酸反应生成硫酸铜,所以丙可以是CuSO4,即甲、乙丙都含有铜元素,且满足了甲是单质,乙、丙都含有铜、氧元素(答案不唯一,只要满足题目给出的条件,合理均可)。铜可以用来做导线,故填:做导线;CuSO4(合理均可)
(2)甲、乙、丙均为含有钙元素的化合物,甲与水反应生成乙并放出大量的热,则甲是氧化钙,俗称生石灰,与水反应生成的乙是氢氧化钙,丙可能是氢氧化钙生成的氯化钙、碳酸钙、硫酸钙写其中一种即可;故填:CaO+H2O═Ca(OH)2;CaCl2或CaCO3或CaSO4(填一个即可)。


科目:初中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含 SiO2、Fe2O3、CeO2 等物质),某课题组以此粉末为原料进行资源回收,其工艺流程如下:
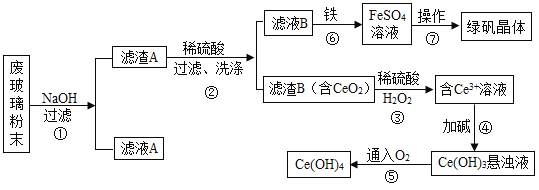
(1)写出第②步反应的化学方程式_____。
(2)洗涤滤渣B 的目的是为了除去_____(填离子符号)。
(3)第⑦步操作是把 FeSO4 溶液经蒸发浓缩、_____、过滤、洗涤、干燥等步骤得到绿矾 FeSO47H2O。
(4)若第④步所加的碱为 NaOH 溶液,写出该步骤中生成 Ce(OH)3 的反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究某些酸碱盐之间能否发生反应,进行了如图所示的实验:
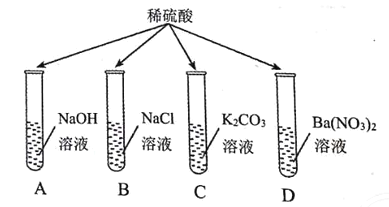
(1)四支试管中能反应且有明显现象的是____,写出有沉淀产生的化学反应方程式_____。
(2)若向试管A中滴入酚酞溶液不变色,则证明试管中溶液显_______性;
(3)实验结束后,将发生了反应的试管中所有物质倒入同一烧杯中,充分混合后过滤,得沉淀和滤液。下列说法中,不正确的是____。
A 若倒入烧杯前各试管中物质都恰好完全反应,则向滤液中滴入紫色石蕊溶液不变色
B 若烧杯中有气泡产生,则倒入烧杯前C中溶质可做钾肥
C 若检测滤液的pH为7,则滤液可直接倒入下水道
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回答与含碳物质有关的问题
(1)用金刚石硬度大的性质常用于_____。
(2)除去CO2中混有的少量CO,可将混合气体______。
(3)如图是在一定条件下生成二氧化碳的转化图
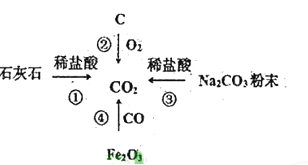
①最适合实验室制取CO2的反应是______(填序号)
②在④反应中,发生氧化反应的物质是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)按要求写出对应的化学符号(“![]() ”表示氧原子)。
”表示氧原子)。
微粒 |
|
|
|
化学符号 | _____ | _____ | _____ |
(2)模型是联系宏观与微观的桥梁。如图是氧原子的结构示意图。

①x的数值为 _____。
②“8”指的是 _____。
③氧原子在化学反应中易得到2个电子,形成_____(填离子符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析下列化学反应,回答有关问题:
① ![]()
② ![]()
(1)分析总结以上两个反应的规律是:碱与含铵根离子的盐反应都生成盐、水和_________________。
(2)标出硝酸铵中氮元素的化合价________________。
(3)根据以上两个方程式的反应规律写出氢氧化钙与氯化铵反应的化学方程式:_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿矾(FeSO47H2O)是重要工业产品,可用于制备Fe2O3,复印用Fe3O4粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作。某研究性小组展开了系列研究。
Ⅰ.制备Fe2O3
(资料一)
(1)无水硫酸铜遇水变成蓝色的硫酸铜晶体。
(2)绿矾(FeSO47H2O)高温分解产生一种金属氧化物和几种气态非金属氧化物。
(3)SO2是无色有刺激性的有毒气体,能使品红溶液褪色;SO3在0℃是一种无色晶体。
甲同学用如图1装置制备Fe2O3并验证绿矾受热分解的其他产物:
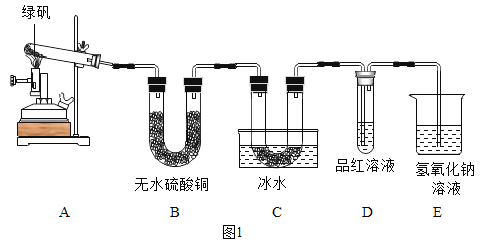
实验过程中发现:A中有红棕色固体生成,B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色。以上能证明有水生成的现象是______,装置E的作用是______,绿矾高温分解的化学方程式为______。
Ⅱ.制备Fe3O4
乙同学模拟生产复印用Fe3O4粉的实验流程如图2:

(资料二)Fe(OH)2是一种白色难溶于水的固体,在空气中易被氧气所氧化,制备时必须尽量排除氧气的干扰。
FeSO4溶液中加入NaOH溶液,反应的化学方程式依次为:①______,②4Fe(OH)2+O2+2H2O=4Fe(OH)3.由沉淀a获得Fe3O4的化学方程式为:Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O,若制取Fe(OH)2,采取的实验操作是:向盛有5mL新制FeSO4溶液的试管中加入10滴植物油,然后用胶滴管加煮沸的NaOH溶液(已经排尽O2),图3中该实验使用胶头滴管的滴加NaOH溶液使用方法正确的是______(填字母)。

Ⅲ.制备还原铁粉
制备还原铁粉的工业流程如图4:
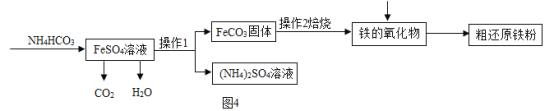
(1)操作1的名称是______。
(2)粗还原铁粉经加工处理后变成纯还原铁粉,纯还原铁粉和水蒸气在高温条件下也可制得四氧化三铁,同时生成一种气体。其装置如图5所示:
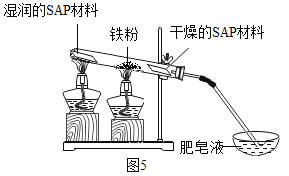
SAP材料用途较多,其吸水性强,湿润的SAP材料能为该反应持续提供水蒸气。实验开始一段时间后,观察到在肥皂液中有大量的气泡产生,此气泡用火柴即能点燃,同时有肥皂泡飘到空中。生成的气体是______,干燥的SAP材料作用是______,请写出该反应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】程伟同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用下图所示装置进行过滤,请问:
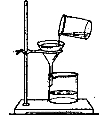
(1)图中还缺少的一种仪器是_________________ 。
(2)过滤后观察发现,滤液仍然浑浊。可能的原因之一______________________:
(3)改进后过滤,得到了澄清透明的水,若要制取纯水,还需采用的净化方法是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】材料和能源是制约社会进步的重要因素。
(1)地球上的金属资源大部分以①_______形式存在,工业上用一氧化碳还原赤铁矿(主要成分是Fe2O3)炼铁的化学方程式为②_______,保护金属资源的有效途径之一是③_______。
(2)化石燃料中,比较清洁的是①_______,化石燃料不充分燃烧均可产生的气体是②_______,氢气是目前最理想的清洁能源的原因是③_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com