
分析 根据锌的质量可求参加反应的硫酸铜的质量和生成的铜的质量;根据“反应后所得溶液的质量=锌粉的质量+原硫酸铜溶液的质量-生成铜的质量”,得出原硫酸铜溶液的质量;
解答 解:设参加反应的硫酸铜的质量为x,生成的铜的质量为y
Zn+CuSO4=Cu+ZnSO4
65 160 64
13g x y
$\frac{65}{13g}=\frac{160}{x}$
x=32g
$\frac{65}{13g}=\frac{64}{y}$
y=12.8g
反应后所得溶液的质量=锌粉的质量+原硫酸铜溶液的质量-生成铜的质量,即:
242.2g=13g+原硫酸铜溶液的质量-12.8g,得:
原硫酸铜溶液的质量=242.2g-13g+12.8g=242g;
答案:生成的铜的质量为12.8g,反应前硫酸铜的溶液质量是242g;
点评 根据“反应后所得溶液的质量=锌粉的质量+原硫酸铜溶液的质量-生成铜的质量”,求出原硫酸铜溶液的质量是关键.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:初中化学 来源: 题型:解答题
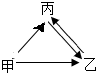 甲、乙、丙是三种初中化学常见的物质,相互转化关系如图所示,请完成下列问题:
甲、乙、丙是三种初中化学常见的物质,相互转化关系如图所示,请完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
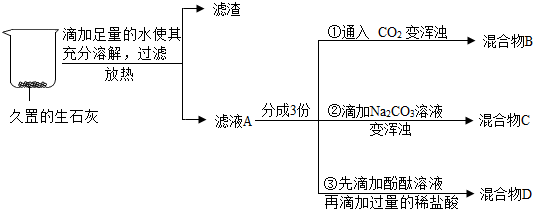
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用燃烧木炭的方法制备纯净的二氧化碳 | |
| B. | 用适量稀硫酸清除铁制品表面的铁锈 | |
| C. | 用紫色的石蕊溶液区分一氧化碳和二氧化碳 | |
| D. | 用足量稀盐酸检验久置的氢氧化钠固体是否变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
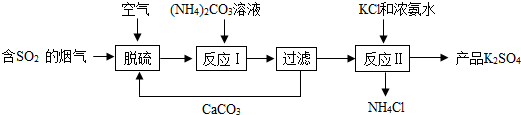
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
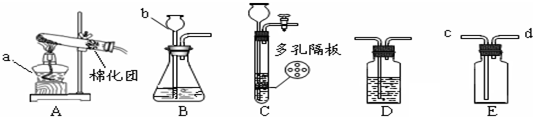
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | “MTBE”是一种有机物 | |
| B. | 一个“MTBE”分子由18个原子构成 | |
| C. | “MTBE”分子中,碳、氢、氧的质量比为5:12:1 | |
| D. | “MTBE”完全燃烧后,生成水和二氧化碳的质量比为55:27 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com