
| A. | “MTBE”是一种有机物 | |
| B. | 一个“MTBE”分子由18个原子构成 | |
| C. | “MTBE”分子中,碳、氢、氧的质量比为5:12:1 | |
| D. | “MTBE”完全燃烧后,生成水和二氧化碳的质量比为55:27 |
分析 A.根据有机物的概念来分析;
B.根据化学式的微观意义来分析;
C.根据化合物中元素的质量比计算方法来分析;
D.根据质量守恒定律来分析.
解答 解:A.由MTBE的化学式CH3OC(CH3)3可知,该物质是一种含碳元素的化合物,属于有机物,故正确;
B.由MTBE的化学式CH3OC(CH3)3可知,该物质的一个分子中5个碳原子、12个氢原子和1个氧原子,共18个原子,故正确;
C.“MTBE”分子中,碳、氢、氧的质量比为(12×5):(1×12):16=15:3:4,故错误;
D.该物质完全燃烧后,生成水与二氧化碳的质量比为:$\frac{1×12}{\frac{1×2}{18}}$:$\frac{12×5}{\frac{12}{44}}$=27:55,故错误.
故选CD.
点评 本题考查元素质量比的计算,及质量守恒定律的灵活运用,解题的关键是化学反应前后元素的质量相等.


科目:初中化学 来源: 题型:解答题
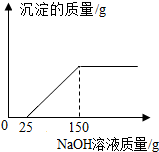 现有16g Fe2O3和CuO的混合物,进行如下实验;把混合物全部加入到100克足量的硫酸溶液中,完全溶解后,滴加溶质质量分数为16%的氢氧化钠溶液,滴加氢氧化钠溶液的质量与生成沉淀质量的关系如图所示,回答下列问题:
现有16g Fe2O3和CuO的混合物,进行如下实验;把混合物全部加入到100克足量的硫酸溶液中,完全溶解后,滴加溶质质量分数为16%的氢氧化钠溶液,滴加氢氧化钠溶液的质量与生成沉淀质量的关系如图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
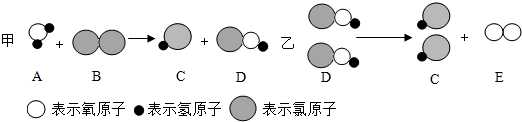
| A. | 物质D属于氧化物 | B. | 物质C的水溶液pH大于7 | ||
| C. | 甲属于复分解反应 | D. | 实验室可用H2O2和MnO2制取E |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 固体样品可能是由Cu和Cu2O组成 | |
| B. | 固体样品可能是由CuO和Cu2O组成 | |
| C. | 固体样品可能是Cu和CuO | |
| D. | 固体样品可能是由Cu、CuO和Cu2O组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
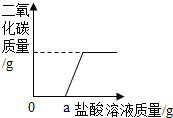
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X>Y>Z | B. | X>Z>Y | C. | Y>Z>X | D. | Z>Y>X |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
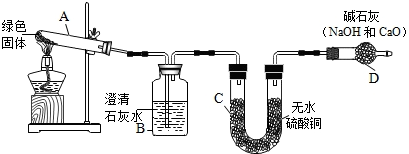
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
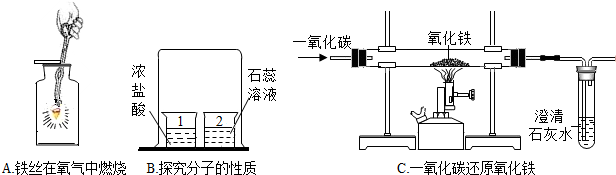
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com