
【题目】如图是实验室常用的实验装置,请根据要求回答下列问题。
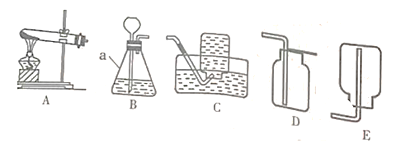
(1)写出图中a仪器的名称:_________。
(2)实验室加热氯酸钾和二氧化锰制取并收集氧气应选择的装置是_________(填序号),若用排空气法收集氧气,检验氧气是否收集满的方法是__________。
(3)实验室用装置B制取二氧化碳的化学方程式为_________;装置B中的长颈漏斗的下端管口应插入液面下,目的是_______。
【答案】锥形瓶A、C或A、D将带火星木条放在瓶口,若带火星木条复燃,则氧气集满CaCO3+2HCl=CaCl2+H2O+CO2↑防止生成的二氧化碳气体从长颈漏斗的下端管口溢出,起密封作用
【解析】
(1)a仪器的名称为锥形瓶;
(2)氯酸钾和二氧化锰制取氧气需要加热,故发生装置选择A,氧气的密度比空气密度略大,且不易溶于水,故收集装置可选择向上排空气法或者排水法,选择C装置或者D装置,故填A、C或A、D;检验氧气是否收集满,可将带火星木条放在瓶口,若带火星木条复燃,则氧气集满;
(3)实验室制取二氧化碳的原理是利用大理石或石灰石(主要成分为碳酸钙)和稀盐酸反应生成氯化钙、水和二氧化碳,故化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;装置B中的长颈漏斗的下端管口应插入液面下,防止生成的二氧化碳气体从长颈漏斗的下端管口溢出,起密封作用。


科目:初中化学 来源: 题型:
【题目】A,B,C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )
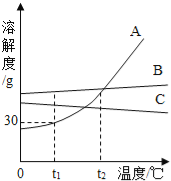
A. t1℃时,A的饱和溶液65g中含有溶剂50g
B. 将t2℃A,B,C三种物质的饱和溶液降温至t1℃时,C溶液中溶质的质量分数保持不变
C. 在t2℃,A,B两种溶液中溶质的质量分数相同
D. 要从B溶液中得到B,通常可采用蒸发溶剂使其结晶的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以菱锌矿(主要成分是ZnCO3,杂质为Fe2O3、FeO、CuO)为原料制备七水硫酸锌(ZnSO47H2O),同时得到铁红副产品,其工艺流程如图,回答下列问题:
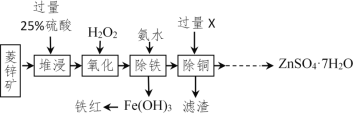
(1)“堆浸”前将菱锌矿粉粹成细颗粒,其目的是_____________________;
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要98%的硫酸质量为_____g(列出算式即可),需要用到的玻璃仪器有胶头滴管、玻璃棒、烧杯和________,此处玻璃棒的作用是____;
(3)物质X是___________,除铜时发生的反应属于________________反应(填基本反应类型);
(4)“氧化”中加入H2O2的目的是在硫酸的作用下将溶液中的FeSO4转化成Fe2(SO4)3,反应的化学方程式:_______________。
(5)流程中获得七水硫酸锌前省略的操作是______________、冷却结晶、过滤、洗涤和低温烘干;
(6)除铁过程中,反应温度、溶液pH对除铁效果均有影响,为探究除铁的最佳效果,某同学做了以下的实验并记录了相关数据,请回答问题:
编号 | 反应温度/℃ | 溶液pH | 除铁率/% |
a | 30 | 2 | 91.5 |
b | 30 | 2.5 | 93.3 |
c | 40 | 2.5 | 95.1 |
d | 40 | 3.1 | Y |
e | 50 | 3.1 | 99.5 |
①实验____和实验_____对比,得到的结论为其他条件不变时,反应温度增大,除铁率提高;
②实验a和实验b对比,得到结论是____________;
③表中Y的值可能为_____________(填编号)
A 93.4 B 94.1 C 97.8 D 99.6
④最佳的除铁条件为反应温度______℃,溶液pH_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验操作的规范性、安全性是实验成败的关键,同时也反映了实验者的化学素养。下列实验操作中正确的是( )
A.  过滤B.
过滤B. 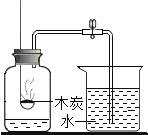 测定空气中氧气含量
测定空气中氧气含量
C. 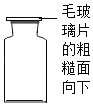 贮存氧气D.
贮存氧气D. 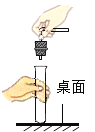 塞紧胶塞
塞紧胶塞
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )
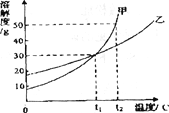
A. t1℃时,甲和乙的溶解度相等,都是30
B. t1℃时,将甲、乙两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等
C. 温度从t2℃降至t1℃时,甲和乙的饱和溶液中析出晶体的质量甲大于乙
D. t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纯碱产品中常含有少量的氯化钠杂质,在实验室中取50g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为30g),每次充分反应后都进行称量,得到的实验数据如表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入纯碱样品的质量/g | 10 | 10 | 10 | 10 | 10 |
电子天平的示数/g | 137.8 | a | 153.4 | 161.2 | 171.2 |
(1)a的值为_____。
(2)计算纯碱样品中碳酸钠的质量_____。
(3)计算所用稀盐酸的溶质质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁在国产大飞机C-919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图像如下),过滤,称量滤液质量为147g,求:
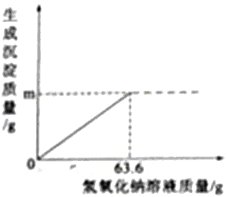
(1)图像中m=_____g。
(2)滤液中溶质的质量分数是____________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b两物质的溶解度曲线如图1所示,请根据图回答:
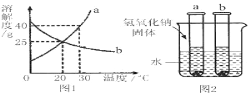
(1)30℃时,a的溶解度是____g。
(2)a的溶解度小于b的溶解度的温度范围是_________。
(3)如图2所示,现有20℃时等质量的a、b两物质的饱和溶液,试管底部有等质量的a、b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的是____(不考虑溶剂的蒸发,析出的固体不含水)
A a溶液中溶质质量增多,b溶液中溶质质量减少
B a溶液中溶质质量分数小于b溶液中溶质质量分数
C a溶液中溶剂质量小于b溶液中溶剂质量
D 试管底部a固体的质量小于b固体的质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com