
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | m | 4.0 |
分析 根据“镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应”,结合第一次加入氢氧化钠溶液所得的数据可知,每加入20g氢氧化钠溶液将会消耗铝16g-10.6g=5.4g;而第三次加入20g氢氧化钠溶液,金属的质量减少5.2g-4.0g=1.2g<5.4g,说明金属铝已完全反应,剩余固体为镁;根据第一次或第二次所加入氢氧化钠溶液的实验数据,通过反应消耗铝的质量,根据反应的化学方程式,计算所加氢氧化钠溶液中的氢氧化钠的质量,而得出所用氢氧化钠溶液中溶质的质量分数.
解答 解:(1)由前两次实验数据可得:每加入20g氢氧化钠溶液将会消耗铝16g-10.6g=5.4g,第二次加入20g氢氧化钠溶液,样品质量减少10.6g-5.4g=5.2g>4g,则m的值为5.2.
(2)由前两次实验数据可得:每加入20g氢氧化钠溶液将会消耗铝16g-10.6g=5.4g,第三次加入20g氢氧化钠溶液,样品质量减少5.2g-4.0g=1.2g<5.4g,则所剩余固体4.0g为金属镁的质量;
(3)第一次所加20g氢氧化钠溶液能反应的铝的质量为:16g-10.6g=5.4g
设20g氢氧化钠溶液中溶质的质量为x
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
54 80
5.4g x
则$\frac{54}{5.4g}$=$\frac{80}{x}$,解得x=8g
所用氢氧化钠溶液中溶质的质量分数=$\frac{8g}{20g}$×100%=40%
答:所用氢氧化钠溶液中溶质的质量分数为40%.
故答案为:
(1)5.2;(2)4;(3)40%.
点评 根据每次加入氢氧化钠溶液充分反应后合金样品质量减少的规律,判断反应进行的程度,从而得出剩余固体为不参加反应的金属的质量.


科目:初中化学 来源: 题型:选择题
| A. | 牛磺酸中含有14个原子 | B. | 牛磺酸的相对分子质量为125g | ||
| C. | 牛磺酸中氧、硫元素的质量比为3:2 | D. | 牛磺酸分子中含有臭氧(O3)分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 镁在空气中燃烧发出耀眼的白光 | B. | 铁丝在氧气中燃烧剧烈火星四射 | ||
| C. | 木炭在空气中燃烧发出蓝紫色火焰 | D. | 磷在空气中燃烧产生大量的白雾 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
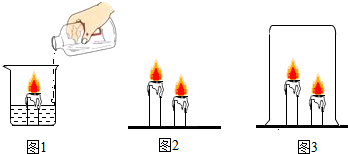
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 25 | 2 | 30 |
| 反应后质量(g) | 30 | 21 | 2 | X |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲烷燃烧生成二氧化碳和水 | B. | 磷在空气中燃烧产生大量白雾 | ||
| C. | 硫在氧气中燃烧产生淡监色火焰 | D. | 镁在空气中燃烧发出耀眼白光 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com