
【题目】碳元素组成的单质有多种。请回答下列问题:
(1)下列结构图中,依次表示石墨、金刚石、C60 的是(填序号)_____。
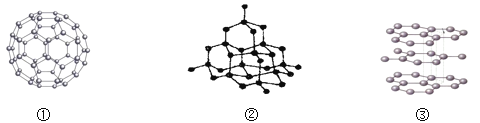
(2)金刚石、石墨、C60都是由_____组成的单质,但三者的物理性质有很大的差异,主要是因为_____。
(3)下列物质中,主要用石墨制取的是(填序号)_____。
①铅笔芯 ②玻璃刀 ③璀灿夺目的天然钻石 ④干电池电极 ⑤钻探机的钻头 ⑥固体润滑剂 ⑦无轨电车的“电刷”
(4)华为公司宣布即将推出高温长寿命石墨烯基锂离子电池,已知石墨烯是碳的单质,其与石墨分别在氧气中完全燃烧的产物_____(“是”或“否”)相同。
(5)石墨在一定条件下可转变为金刚石,该变化属于_____变化。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】某小组同学分别完成了图1所示的3个实验(图中a处连接压强传感器)。图2中的曲线1、2、3分别表示加入等体积相应液体后,烧瓶1、2、3内压强随时间的变化趋势。

下列说法不正确的是
A. 由于注入液体压缩了瓶内的气体,所以三个实验的起始阶段压强都快速增大
B. 对比曲线1和2可知,二氧化碳和水一定发生了化学反应
C. 对比曲线1和3可知,二氧化碳和氢氧化钠一定发生了化学反应
D. 对比曲线2和3可知,40% NaOH溶液比饱和石灰水更适合吸收二氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将光亮镁条放入一定量的稀HCl中,产生大量气泡后出现灰白色固体。某同学对该现象作如下探究。(已知:MgCl2晶体能溶于水)
(一)产生气泡反应的化学方程式____。
(二)过滤、洗涤、室温晾干得灰白色固体。对灰白色固体作如下猜测并进行实验:
(猜测)灰白色固体可能是:①剩余的Mg; ②____; ③Mg和MgCl2晶体。
(实验1)(1)取灰白色固体样品,加入稀HCl,无气泡产生,则猜测 __(选填序号)不成立。(2)称取等质量的灰白色固体和MgCl2晶体分别放入同温、等量水中,灰白色固体不溶解,而MgCl2晶体全部____,则猜测②不成立。
(查阅资料):灰白色固体的成分为碱式氯化镁,化学式可表示为Mgx(OH)yClznH2O[即每个Mgx(OH)yClz结合了n个H2O],它受热分解可产生氧化镁、氯化氢和水。
(实验2)另取该灰白色固体47.5g,按照正确的操作步骤进行受热分解实验,待反应停止后,测得氧化镁固体质量为24.0g,水的质量16.2g。
(问题讨论)
(1)X:Z=____。
(2)Mgx(OH)yCl的化学式可能是 ______。
(3)若沉淀Mgx(OH)yClznH2O中,n=5,则Y的数值为____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+ 3O2![]() 2X + 6H2O,则X的化学式为
2X + 6H2O,则X的化学式为
A. NO B. N2 C. NO2 D. N2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下表提供的信息,回答下列问题。
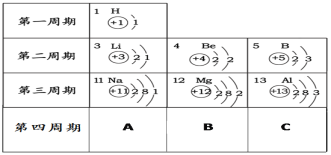
(1)锂元素的元素符号为_______,钠离子最外层有________个电子。
(2)锂、钠、镁、铝均属于__________元素(选填“金属”或“非金属”),它们的原子在化学反应中易_______(选填“得到”或“失去”)电子而形成_________(选填“阳”或“阴”)离子,其中地壳中含量最多的金属元素形成的离子其符号是________。
(3)钙元素的原子结构示意图为 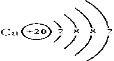 ,据此推测, 钙元素在元素周期表中的位置应该是___________(选填“A”“B”或“C”)。
,据此推测, 钙元素在元素周期表中的位置应该是___________(选填“A”“B”或“C”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关化学方程式2H2+O2![]() 2H2O的叙述中,错误的是 ( )
2H2O的叙述中,错误的是 ( )
A. 氢气和氧气在点燃条件下反应生成水
B. 每2个氢分子与1个氧分子在点燃条件下结合成2个水分子
C. 每2份质量的氢气和1份质量的氧气在点燃的条件下生成2份质量的水
D. 每4份质量的氢气与32份质量的氧气反应生成36份质量的水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我校化学兴趣小组同学为了测定当地石灰石中碳酸钙的质量分数,他们采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(杂质不和盐酸反应,也不溶与水),请帮他们计算:
序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
第1次 | 20 | 11 |
第2次 | 20 | 6 |
第3次 | 20 | 2.8 |
第4次 | 20 | n |
(1)碳酸钙的相对分子质量 _______。
(2)上表中n的数值是 _________ 。
(3)样品中碳酸钙的质量分数 _________ 。
(4)生成二氧化碳的质量为__________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的部分反应原理的微观示意图如下。请回答下列问题:

(1)画出硅原子的结构示意图____________ ,它位于第几周期_________ 。
(2)甲物质中两种元素的质量比为______。
(3)该反应的化学方程式为_____________________。
(4)反应后硅元素的化合价______(选填“升高”、“降低”或“不变”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】47中化学活动小组的同学要测定菱铁矿石(主要成分FeCO3,杂质不含铁元素也不与酸发生反应,且不溶于水)的含量,实验过程如下:

请回答下列问题:
(1)上述实验过程中发生的化学反应方程式为________;
(2)根据已知条件列出求解第一次所加的稀硫酸中溶质质量(X)的比例式________
(3)此菱铁矿石样品中 FeCO3的质量分数是______;
(4)若将反应后的滤液蒸发14.4g水,无晶体析出,所得溶液中溶质的质量分数为______
(5)用 98%的浓硫酸配制200g上述稀硫酸,所需浓硫酸的质量为_______。
(6)若用290t该菱铁矿石来生产含铁 96%的生铁,在冶炼过程中损失 4%的铁元素,则可得到生铁的质量为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com