
【题目】真真实验小组欲亲自探究适合在实验室制取二氧化碳的药品。她们准备利用碳酸钠粉未、块状大理石、稀盐酸、浓盐酸、稀硫酸五种药品进行实验探究
(提出问题)上述药品间的相互反应都适合在实验室制取二氧化碳气体吗?
(方案设计)(1)经过讨论大家都致认为浓盐酸不适合用于实验室制取二氧化碳你认为原因是___。
(2)真真小组同学经过反复设计研究后确定迸行如下图所示的四个实验
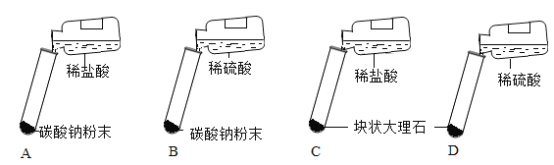
(结论分析)实验报告单如下表
实验编号 | 实验现象 | 实验结论 |
A | 剧烈反应,迅速产生大量气泡 | 反应速率过快,不便于气体收集 |
B | 剧烈反应,迅速产生大量气泡 | _________ |
C | ______ | 便于收集,适合在实验室制取CO2 |
D | 一开始产生气泡,之后便迅速减慢直到反应几乎停止 | 因为无法持续的产生气体,不适合用在实验室制取二氧化碳 |
(3)①结合上面的实验探究报告,可用于实验室制取二氧化碳气体的化学反应方程式为___;
②在确定实验室制取气体反应原理时,要考虑诸多因素,请你再写出一种需要考虑的因素:___;
(继续探究)在实验室里,小组同学利用12.3%的稀盐酸与块状大理石来制取二氧化碳。
(问题引入)(4)实验结束后发现裝置内废液中还有块状固体存在,但已观察不到气泡产生,反应后的废液中还有盐酸吗?甲同学用pH试纸测得该废液的pH=2,证明___;
(5)反应后废液中剩余的块状固体中还有碳酸钙吗?乙同学带着疑问取岀废液中块状的固体,洗净后放入试管中, 再加入约2mL的___, 立即产生大量的气泡, 证明___。
(猜想验证)(6)既然反应后废液中还有盐酸和碳酸钙,那为何观察不到实验现象呢?
①同学认为是废液中盐酸浓度太低,所以观察不到现象。甲同学将少许___置于试管中,加入约2mLpH=1的稀盐酸,立即观察到有气泡冒出
②乙同学认为是实验所用大理石块较大,与盐酸接触不充分,所以观察不到明显的现象,于是乙同学向老师要了一些纯净的碳酸钙粉未放入试管中,加入约2ml___,立即观察到有气泡冒出
(实验结论)
(7)依据(4)(5)确定发生反应后装置废液中的盐酸与碳酸钙共存,但不能观察到现象。结合实验(6)①②闸述其原因___;
(拓展延伸)(8)实验室用块状大理石与稀盐酸反应 pH至气泡逸出不明显后,测得残留液 pH=2,若取适量残留液体的上层清液于试管中,逐滴滴入碳酸钠溶液至过量。请在下图中绘出变化趋势___。

【答案】浓盐酸具有强挥发性,会发出HCl使收集到的CO2不纯 反应速率过快,不便于收集气体 固体逐渐溶解,有气泡产生 CaCO3+2HCl=CaCl2+H2O+CO2↑ 制取过程中是否会产生有害物质、实验条件是否节能 溶液中有盐酸剩余 12.3%的稀盐酸 有碳酸钙剩余 废液中残留的块状固体 废液中的上清液 稀盐酸的浓度过低,大理石与酸的接触面积过小,所以观察不到现象 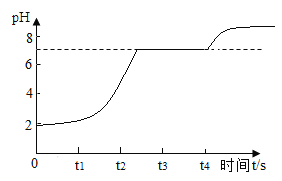
【解析】
碳酸钙和稀盐酸生成氯化钙、水和二氧化碳,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳。
[方案设计](1) 浓盐酸具有强挥发性,故经过讨论大家都致认为浓盐酸不适合用于实验室制取二氧化碳,原因是浓盐酸具有强挥发性,会发出HCl使收集到的CO2不纯。
[结论分析]碳酸钠和稀盐酸、稀硫酸反应速率较快,不便于收集生成的二氧化碳气体,稀硫酸和碳酸钙反应生成硫酸钙微溶物覆盖在大理石表面,阻止反应发生,实验室常用碳酸钙和稀盐酸反应制取氧气。
实验编号 | 实验现象 | 实验结论 |
A | 剧烈反应,迅速产生大量气泡 | 反应速率过快,不便于气体收集 |
B | 剧烈反应,迅速产生大量气泡 | 反应速率过快,不便于收集气体 |
C | 固体逐渐溶解,有气泡产生 | 便于收集,适合在实验室制取CO2 |
D | 一开始产生气泡,之后便迅速减慢直到反应几乎停止 | 因为无法持续的产生气体,不适合用在实验室制取二氧化碳 |
(3)①实验室制取二氧化碳气体的反应是碳酸钙和稀盐酸生成氯化钙、水和二氧化碳,反应的化学方程式为![]() 。
。
②在确定实验室制取气体反应原理时,要考虑诸多因素,需要考虑的因素是制取过程中是否会产生有害物质、实验条件是否节能。
[问题引入](4) pH小于7的溶液,显酸性,甲同学用pH试纸测得该废液的pH=2,证明溶液中有盐酸剩余。
(5)稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,取岀废液中块状的固体,洗净后放入试管中, 再加入约2mL的12.3%的稀盐酸, 立即产生大量的气泡, 证明有碳酸钙剩余。
[猜想验证](6)①废液中盐酸浓度太低,所以观察不到现象,则用浓度较高的稀盐酸做实验,故甲同学将少许废液中残留的块状固体置于试管中,加入约2mLpH=1的稀盐酸,立即观察到有气泡冒出。
②乙同学认为是实验所用大理石块较大,与盐酸接触不充分,所以观察不到明显的现象,于是乙同学向老师要了一些纯净的碳酸钙粉未放入试管中,加入约2ml废液中的上清液,立即观察到有气泡冒出。
[实验结论](7)稀盐酸和大理石反应,稀盐酸的浓度要达到一定量,大理石的面积要较小,故原因是稀盐酸的浓度过低,大理石与酸的接触面积过小,所以观察不到现象。
[拓展延伸](8)实验室用块状大理石与稀盐酸反应 pH至气泡逸出不明显后,测得残留液 pH=2,溶液显酸性,取适量残留液体的上层清液于试管中,上层清液含有盐酸,逐滴滴入碳酸钠溶液至过量,碳酸钠先和盐酸反应生成氯化钠、水和二氧化碳,随着反应的进行,pH增大,盐酸完全反应后,氯化钙与碳酸钠反应生成碳酸钙和氯化钠,反应完全pH=7,碳酸钠过量,pH增大,故图像为 。
。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:初中化学 来源: 题型:
【题目】北京时间2018年12月8日凌晨2时23分,中国在西昌卫星发射中心用“长征三号乙”运载火箭成功发射嫦娥四号探测器,开启了中国月球探测的新旅程。
(1)“长征三号乙”运载火箭的第三级采用的燃料是液氢,助燃剂是液氧。液氢燃烧的化学方程式为________________;氢能源是理想的绿色能源,原因是_____________。而目前我国常见的三种化石燃料为煤、石油和_____________。
(2)煤燃烧时会排放出________________(写出任意一种物质的化学式)等气体污染物,这些物质溶于雨水之后,会形成酸雨。
(3)在车用汽油中加入适量乙醇可在一定程度上减少汽车尾气的污染。乙醇属于____________(填“可再生”或“不可再生”)能源,其燃烧的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
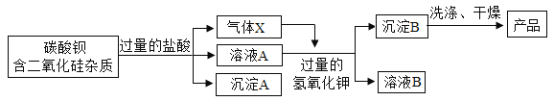
【题目】碳酸钡是一种重要的化工产品,某厂用含二氧化硅杂质的碳酸钡原料生产碳酸钡产品,采用了如图所示的工艺流程:(二氧化硅不溶于水也不与盐酸反应)
试
(1)气体X是____
(2)加入过量的盐酸目的是____
(3)溶液A中的阳离子是____(填离子符号)
(4)整个工艺流程中涉及到的化学反应有___个(填数字)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学的基本特征是研究和创造物质,我们从化学的几个角度分析物质:
(1)分类角度:“中国高铁”其车身主要采用的镍铬奥氏体不锈钢属于__________(填序号)
A无机非金属材料
B金属材料
C有机合成材料
D复合材料
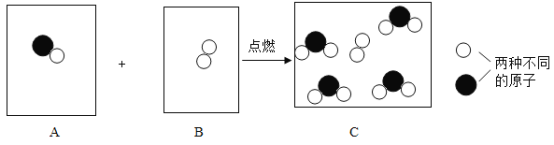
(2)微观角度:请把图中A、B 框中的微观粒子进行的化学反应补画齐全_______。
(3)性质角度:月球背面的陨石坑土壤中有天然的铁、铝、银等金属颗粒。根据铁锈蚀的条件分析,铁在月球上不锈蚀的原因是______________。
(4)变化角度:如图为碳的价类图,例如 C 点标示为+2 价的碳的氧化物,请回答:

A点所表示的物质是天然气的主要成分,其化学式为_______________;D和水反应能生成 E,化学方程式为___________________
(5)营养角度:
①鱼头汤中的蛋白质进入人体后会逐步分解成被人体吸收的______
②“砂锅鱼头”汤鲜汁浓,但其中几乎不含有的营养素是______(填字序号)。
A无机盐 B油脂 C糖类 D水
(6)环保角度:
用液化气灶煮食时,砂锅外壁出现黑灰,此时可将灶具的进风口____________(填“调大”或“调小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家成功研制出碳化钼(Mo2C)负载金原子组成的高效催化体系,能使水煤气中CO和 H2O在120℃时发生反应,其微观模型如下图所示,下列说法不正确的是( )
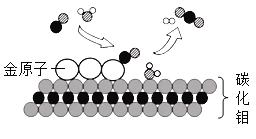
A.两种反应物均属氧化物B.金原子对水分子起吸附作用
C.催化剂质量在反应前后没有变化D.该化学反应的实质就是原子重新组合
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学进行了如下实验,验证一氧化碳与氧化铜的反应
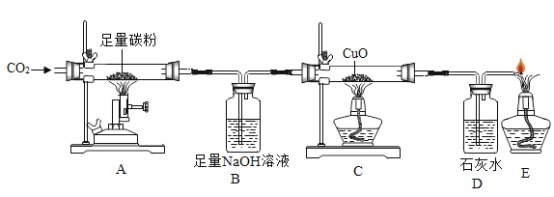
①进入装置 B 的气体中含有二氧化碳和_____
②C 处氧化铜发生反应的化学方程式是_____;D 中观察到的现象是______
③对于该实验的相关分析,正确的是_____(选填编号)
a 实验开始时,先缓慢通入二氧化碳,D 中无明显现象
b 装置 B 中无明显现象,说明该装置中没有发生反应
c 装置 E 的作用是将尾气点燃,防止污染空气
d 实验结束后,装置 C 玻璃管中固体减少的质量等于装置 D 中增加的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是初中化学常见六种物质之间的关系图(物质是溶液的只考虑溶质)。图中用“一”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质(部分反应物或生成物及反应条件已略去)。A中含有人体含量最多的金属元素,B、C中不含相同元素,C、D中所含元素种类相同。

(1)写出相应物质的化学式: A__________; B__________;C__________;D__________;
(2)写出C→D转化的化学方程式__________;
(3)写出B与Fe2O3反应的化学方程式__________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体在不同温度时的溶解度如下表所示。请回答下列问题:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度(g) | 甲 | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
乙 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | |
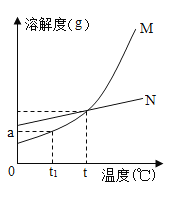
(1)依据上表数据,绘制出甲、乙两物质的溶解度曲线(如图所示),图中能表示甲物质溶解度曲线的是______;(填“M”或“N”)
(2)若t1=10℃,则a=________;
(3)40℃时,将30g甲物质溶于50g水中,充分搅拌,所得溶液中溶质的质量分数是_______(精确到0.1%);
(4)从甲、乙混合溶液中提纯乙的方法是________;
(5)t℃时甲、乙两物质的溶解度相等,此时t的取值范围是______。
A. 10~20 B. 20~30 C. 30~40 D. 40~50
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中A、B分别是某微粒的结构示意图,回答下列问题:
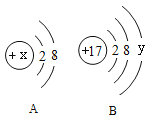
(1)若A表示某稀有气体元素的原子,该元素的单质的化学式为______________。
(2)若B表示某元素的原子,则y=_________,该元素的原子在化学反应中容易______(填“失去”或“得到”)电子。
(3)若A是阳离子的结构示意图,其离子符号可能是下列中的_________(填字母序号)。
a、Ca2+ b、Mg2+ c、Zn2+ d、Al3+
(4)若A中x=13,则A、B所表示的元素形成化合物的化学式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com