

分析 (1)认识常见仪器的名称;
(2)据A装置是加热固体制取氧气,且试管口有棉花可知是用加热高锰酸钾的方法制取氧气,据反应原理书写方程式,据氧气的密度和溶解性选择收集装置;
(3)根据反应物的状态和反应的条件确定发生装置,根据二氧化碳的密度确定收集方法;根据方程式的写法写出反应原理.
解答 解:(1)仪器a、b分别是酒精灯和长颈漏斗;故填:酒精灯;长颈漏斗;
(2)A装置是加热固体制取氧气,且试管口有棉花可知是用高锰酸钾制取氧气,反应方程式 是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,氧气的密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,故收集装置可选用C或F;故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;C或F;
(3)实验室制取二氧化碳的反应物是石灰水和稀盐酸,反应物的状态是固体和液体,反应条件是不需加热,故选用的发生装置是B,若用C装置收集二氧化碳气体,因为二氧化碳的密度大于空气,故气体应从导管a进入,实验室制取二氧化碳的化学方程式 CaCO3+2HCl=CaCl2+H2O+CO2↑,故填:B;CaCO3+2HCl=CaCl2+H2O+CO2↑;a.
点评 发生装置的选择与反应物的状态和反应条件有关:反应物的状态是固体和液体,不需要加热,如果固体与固体反应制取气体需要加热,收集方法的选择是根据:难溶于水或不易溶于水用排水法收集,密度比空气大用向上排空气法收集,密度比空气小用向下排空气法收集.


科目:初中化学 来源: 题型:解答题
| 实验一 | 实验二 | 实验三 | |
实验 方案 | 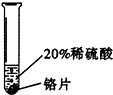 |  | 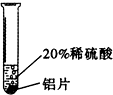 |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | |
| 三种金属在金属活动性顺序中的相对位置关系是Al Cr Cu(或“②”) | |||
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na+、K+、OH-、SO42- | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | Na+、Mg2+、SO42-、OH- | D. | Ca2+、SO42-、NO3-、CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 托盘天平是一种实验室常用的称量用具,请回答下列问题:
托盘天平是一种实验室常用的称量用具,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1gH2和8gO2 | B. | 0.1mol HCl和2.24L氯化氢 | ||
| C. | 28gCO和22gCO2 | D. | 9gH2O和0.5molCO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 土壤污染会影响食品安全,我国的某地区曾发生“镉大米”事件.镉的相关信息:①镉元素位于第五周期ⅡB族.②镉是银白色有光泽的金属,熔点320.9℃,沸点765℃,密度8.64g/cm3,有韧性和延展性;镉在潮湿空气中缓慢氧化并失去金属光泽;镉可溶于酸,但不溶于碱.③镉对人体十分有害,摄入过量镉污染的食品和水,会引起肺和肾脏疾病.回答下列问题:
土壤污染会影响食品安全,我国的某地区曾发生“镉大米”事件.镉的相关信息:①镉元素位于第五周期ⅡB族.②镉是银白色有光泽的金属,熔点320.9℃,沸点765℃,密度8.64g/cm3,有韧性和延展性;镉在潮湿空气中缓慢氧化并失去金属光泽;镉可溶于酸,但不溶于碱.③镉对人体十分有害,摄入过量镉污染的食品和水,会引起肺和肾脏疾病.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com