



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、生石灰放在空气中变质说明空气中有水蒸气存在 |
| B、氢氧化钠溶液变质说明空气中有二氧化碳的存在,证明氢氧化钠溶液是否变质,取少量样品放入试管中,加入足量的稀盐酸就可以证明 |
| C、大型载重汽车装有很多车轮,这是为减小压强 |
| D、物体受平衡力的作用,一定保持静止状态 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、1个 | B、2个 | C、3个 | D、4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
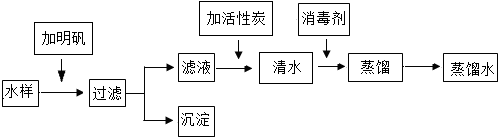
查看答案和解析>>
科目:初中化学 来源: 题型:
 某课外活动小组为测定铜粉(含炭粉)样品中铜的质量分数,进行了如图所示装置实验,图中铁架台等装置已略去.装置A中盛装的是过氧化氢溶液,装置B中是二氧化锰粉末,装置D中是碱石灰(固体氢氧化钠和氧化钙的混合物),装置E中是浓硫酸.
某课外活动小组为测定铜粉(含炭粉)样品中铜的质量分数,进行了如图所示装置实验,图中铁架台等装置已略去.装置A中盛装的是过氧化氢溶液,装置B中是二氧化锰粉末,装置D中是碱石灰(固体氢氧化钠和氧化钙的混合物),装置E中是浓硫酸.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com