

分析 (1)根据质量守恒定律反应前后减少的质量即为生成二氧化碳的质量;
(2)根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,然后结合题中的数据进行解答;
(3)根据实验实际测得的氯化钠质量往往会有偏差,其原因可能是二氧化碳部分溶解在水中(或与水反应)、有少量水蒸气进入空气等解答.
解答 解:(1)反应生成CO2的质量为13g+100g+100g-208.6g=4.4g;
(2)设样品中Na2CO3质量为x,稀盐酸的溶质为y,生成NaCl质量为z,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 73 117 44
x y z 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
x=10.6g
$\frac{73}{y}=\frac{44}{4.4g}$
y=7.3g
稀盐酸的溶质质量分数为:$\frac{7.3g}{100g}×$100%=7.3%
氯化钠的质量为:13g-10.6g=2.4g
(3)该实验实际测得的氯化钠质量往往会有偏差,其原因可能是二氧化碳部分溶解在水中(或与水反应)、有少量水蒸气进入空气等.
答案:
(1)4.4 7.3%
(2)混合物中氯化钠的质量为2.4g
(3)二氧化碳部分溶解在水中(或与水反应)、有少量水蒸气进入空气等.
点评 要想解答好这类题目,首先要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等,然后根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.


科目:初中化学 来源: 题型:选择题
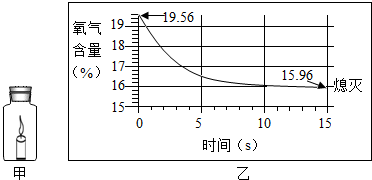
| A. | 蜡烛燃烧前装置内只有氧气 | |
| B. | 蜡烛熄灭后瓶内只剩二氧化碳气体 | |
| C. | 过程中装置内物质总质量不断减少 | |
| D. | 氧气含量小于一定值时,蜡烛无法燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2Cu中的“2”表示2个铜元素 | |
| B. | Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | |
| C. | H2S中的“2”表示1个硫化氢分子中含 有2个硫原子 | |
| D. | S2-表示-2价的硫元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定是纯净物 | B. | 一定是混合物 | C. | 可能是混合物 | D. | 可能是纯净物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 11.2g | B. | 22.4g | C. | 44.8g | D. | 89.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某学习小组对硫酸进行如下研究:
某学习小组对硫酸进行如下研究:| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水 质量/g | 浓硫酸 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 稀硫酸 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.| 我对气体的猜想是 | |
| 我猜想的依据是 |
| 实验方法及操作 | 可能观察到的现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
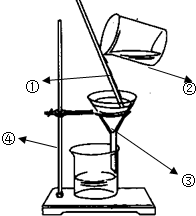 (1)指出图中所标的仪器的名称
(1)指出图中所标的仪器的名称查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com