
【题目】用某矿石(主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质)制取MgO的工艺流程简图如图:
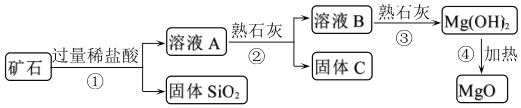
回答下列问题:
(1)步骤①和步骤②均用到的操作是_____。
(2)溶液A一定_____ (填“有”或“没有”)颜色,其中所含质量最小的阳离子是_____(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的pH范围为_____,固体C中所含成分的化学式为_____。
(4)已知在不同温度下,充分加热等质量的Mg(OH)2,加热温度与固体残留率的关系如图所示。则在上述流程步骤④中,加热的温度至少_____℃以 上,图中拐点的X值为_____(取整数)。

(5)写出步骤①中Fe2O3溶于盐酸的反应化学方程式:_____。
(6)上面工业流程中不用石灰水代替熟石灰工业意义是:_____(答一条即可)。
【答案】过滤 有 H+ 6.7~9.1 Cu(OH)2和Fe(OH)3 350 69 Fe2O3+6HCl═2FeCl3+3H2O 氢氧化钙微溶于水,饱和石灰水是稀溶液,用熟石灰粉末把金属离子转化成沉淀的效果更好
【解析】
(1)过滤可以将不溶性固体从溶液中分离出来,所以步骤①和步骤②均用到的操作是过滤,故填过滤。
(2)步骤①中盐酸和氧化铁反应生成氯化铁和水,盐酸和氧化铜反应生成氯化铜和水,盐酸和氧化镁反应生成氯化镁和水,由于溶液A中含有氯化铁和氯化铜,所以溶液A一定有颜色,故填有;
步骤①盐酸是过量的,所以溶液A中所含质量最小的阳离子是氢离子,其符号为H+,故填H+。
(3)由铁离子、铜离子沉淀时的pH和镁离子开始沉淀的pH可知,步骤②加入熟石灰,应调节溶液的pH范围为6.7~9.1,避免镁离子形成氢氧化镁沉淀,故填6.7~9.1;
由图可知,固体C中所含成分是氢氧化铜和氢氧化铁,其化学式为Cu(OH)2、Fe(OH)3,故填Cu(OH)2、Fe(OH)3。
(4)由加热温度与固体残留率的关系图可知,则在上述流程步骤④中,加热的温度至少350℃以上,故填350;
有图可知,当温度为350℃时,氢氧化镁全部转化为氧化镁,根据化学方程式Mg(OH)2![]() MgO+H2O可知,每58份质量的氢氧化镁完全分解可生成40份的氧化镁,则固体残留率=
MgO+H2O可知,每58份质量的氢氧化镁完全分解可生成40份的氧化镁,则固体残留率=![]() ×100%≈69%,所以图中拐点的X值为69,故填69。
×100%≈69%,所以图中拐点的X值为69,故填69。
(5)步骤①中Fe2O3与盐酸生成了氯化铁和水,故反应的化学方程式写为:Fe2O3+6HCl═2FeCl3+3H2O。
(6)由于氢氧化钙微溶于水,上面工业流程中不用石灰水代替熟石灰工业意义是:氢氧化钙微溶于水,饱和石灰水是稀溶液,用熟石灰粉末把金属离子转化成沉淀的效果更好。


科目:初中化学 来源: 题型:
【题目】实验室制取气体常用到下图所示装置。请根据要求回答下列问题:
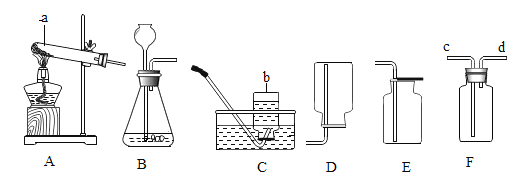
(1)请写出图中标号仪器的名称:a________b________;
(2)请写出实验室用B装置制取氧气的化学方程式________,收集该气体时选用的装置是_____(填“C”、“D”或“E”);
(3)若用B、E组合可以制取和收集CO2,此时在锥形瓶中事先放进的固体药品是_______;
(4)F可以代替C、D、E收集气体。欲收集具有下面性质的气体,应如何使用装置F?
①收集密度比空气大的气体:进气口为_______(填“c”或“d”下同);
②收集难溶于水的气体:瓶内应装满水,进气口为_______。
(5)NH3极易溶于水形成氨水,氨水可用作氮肥。实验室常用加热氯化铵(固体)与熟石灰(固体)混合物的方法来制取,此时应选择的发生装置是______(填“A”或“B”),收集装置是______(填“C”、“D”或“E”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】核电菏数为1~18的元素的原子结构示意图等信息如下,请回答下列间题:
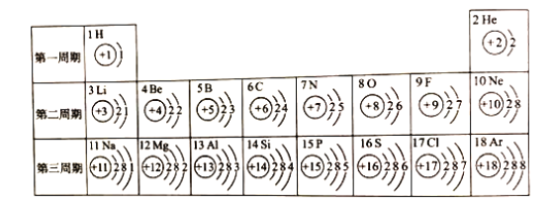
(1)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是_________。
(2)利用上表中给出的元素,写出含有氢元素的常见单质、氧化物、酸、碱、盐的化学式各一个:单质______、氧化物______、酸______、碱______、盐______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某市售某浓盐酸试剂瓶标签上的有关数据如图1所示。小张同学取5mL该浓盐酸加入锥形瓶中,加水稀释后,再逐滴滴加溶质质量分数为5%的NaOH溶液,反应过程中溶液的酸碱度变化如图2所示。

(1)小张同学所取的5mL浓盐酸的质量为_____克。
(2)通过计算,判断该浓盐酸中HCl的质量分数是否与试剂瓶标签上的数据相符_____(需要计算过程,计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。高温下,甲和乙反应生成丙和丁,结合表中信息判断下列说法正确的是
物质 | 甲 | 乙 | 丙 | 丁 |
|
化学式 | ? | C | CO | H2 | |
微观 示意图 |
|
|
| ? |
A. 甲的化学式为CO2 B. 保持丙化学性质的最小粒子为碳原子和氧原子
C. 反应物和生成物中都有化合物 D. 反应生成丙与丁的分子个数比为2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学利用下图装置探究工业炼铁的化学原理。

(1)实验前要先通入一氧化碳,然后再加热;实验过程中观察到硬质玻璃管内的红色物质逐渐变为_____色,写出反应的化学方程式_____。
(2)实验过程中必须对尾气进行处理,利用支架调节酒精灯的高度,用酒精灯火焰的_____点燃。
(3)通过上述实验探究,同学们总结一氧化碳的化学性质有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示的四个图像,能正确反映对应变化关系的是
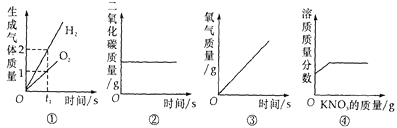
A. ①水的电解
B. ②木炭在密闭的容器内燃烧
C. ③加热一定量的高锰酸钾制氧气
D. ④20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学进行如下实验探究。
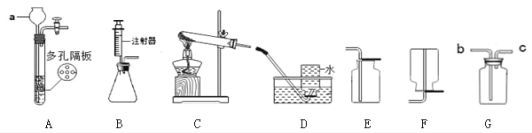
(1)仪器a的名称________。
(2)实验室用氯酸钾和二氧化锰的混合物制取氧气,化学方程式为________,选用的装置组合可以是________。
(3)实验室制取二氧化碳的化学方程式是________,若用 G 装置收集二氧化碳,气体应 从________端进入(填“b”或“c”),检验二氧化碳收集满的方法是________。
(4)用锌粒和稀硫酸制取氢气时,与装置B相比,装置A的优点是________。
(5)兴趣小组同学准备探究制取氧气的适宜催化剂,实验方案如下:
Ⅰ.用 MnO2、CuO、Fe2O3、Cr2O3 四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用图2装置进行实验。改用其他三种微球,分别 重复上述实验,得到图3的锥形瓶内压强随时间变化的曲线图。
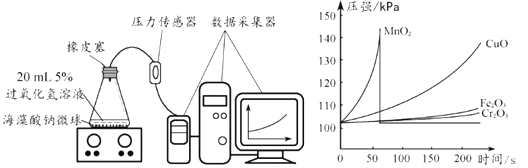
① 每次实验时,海藻酸钠微球数应相同的原因________。
② 用含MnO2的海藻酸钠微球进行实验,60S时压强瞬间回落,其原因是________。
③ 从实验曲线看,催化效果较好、反应温和的催化剂是________。
④CuO、Fe2O3、Cr2O3 对应的曲线最终________(填“不重合或“重合”) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com