
【题目】在含氯化钠杂质的碳酸钠13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量与pH的关系如图所示:
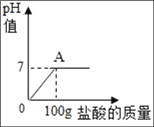
(1)100g稀盐酸中氯化氢的质量__.
(2)完全反应后,计算生成二氧化碳的质量为____________?(写出计算步骤)
(3)完全反应后,所得溶液中溶质的质量分数为____________?(写出计算步骤)
【答案】 7.3g 4.4g 13.5%
【解析】(1)100g稀盐酸中氯化氢的质量=100g![]() =7.3g
=7.3g
(2)由图可知,加入100g的稀盐酸后,稀盐酸与碳酸钠恰好完全反应,设生成二氧化碳的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl ==2NaCl+H2O+CO2↑
106 73 117 44
m 7.3g y x
![]() =
=![]() =
=![]() 求得x=4.4g,y=11.7g,m=10.6g
求得x=4.4g,y=11.7g,m=10.6g
(3)原样品中氯化钠的质量为13.6g-10.6g=3g,反应后溶液中溶质的质量为3g+11.7g=14.7g,反应后溶液的总质量为13.6g+100g-4.4g=109.2g,反应后溶液中溶质的质量分数为![]() =13.5%;
=13.5%;


科目:初中化学 来源: 题型:
【题目】下列四个图象分别对应四种实验操作过程,其中正确的是
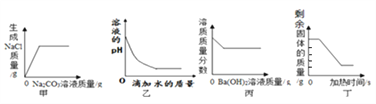
A. 甲表示向一定质量的盐酸和氯化钙的混合溶液中逐滴加入碳酸钠溶液至过量
B. 乙表示向稀硫酸中加水
C. 丙表示向一定质量的稀硫酸中逐滴加入氢氧化钡溶液至过量
D. 丁表示加热一定质量的高锰酸钾
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t1℃时,将等质量的硝酸钾和氯化钾分配加入到各盛有10g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.

(1)烧杯①中溶解的溶质是______(写名称或化学式);
(2)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水____g;
(3)关于图1中烧杯内的物质,下列说法正确的是____________.
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是化学学习的重要组成部分.请用正确的化学用语填空:
(1)3个铁原子______. (2) “西气东输”工程输送的“气”是_________;
(3 两个氢分子_______. (4)4个硫酸酸根离子________.
(5)氧化铜中铜元素的化合价为+2价________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为除去下表样品中的少量杂质(括号内为杂质),选试剂及操作方法均正确的是( )
序号 | 样品成分 | 所选试剂 | 操作方法 |
A | KCl(MnO2) | 水 | 溶解、过滤、洗涤干燥 |
B | CaO(CaCO3固体) |
| 加热至质量不再减少 |
C | CO2(HCl) | 氢氧化钠溶液 | 洗气 |
D | NaCl(MgCl2) | 过量NaOH溶液 | 过滤、蒸发结晶 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用化学用语表示:
铝原子___;二氧化氮分子___;氯化钠中的阳离子___;人体中含量最多的物质_______
(2)请用下列物质的字母序号填空:
A.硫酸铜 b.盐酸c.碳酸钠 d.熟石灰
①可用于改良土壤酸性的是 ______②侯氏制碱法制的碱_______
③用作配制波尔多液的盐___; ④可用于金属表面除锈的是_____;
(3)用化学方程式表示以下反应:
①铜和硝酸银溶液____ ②氯酸钾制氧气_______
③铁丝在纯氧中燃烧_____ ④电解食盐水得到烧碱、氯气和氢气_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】浩瀚的大海蕴含的元素有80多种,是一个巨大的宝藏库。地球上99%以上的溴元素都蕴藏在大海中,因此,溴被称为“海洋元素”。工业上常用“空气吹出法”工艺进行海水提溴。因卤水中溴(Br2)的含量较低,必须用工业方法将卤水进行浓缩、提纯从而达到节约成本和能源的目的。“空气吹出法”是目前世界上最成熟、最普遍采用的提溴工艺,此法可从低浓度含溴卤水中提取溴(Br2)。其工艺流程如下:
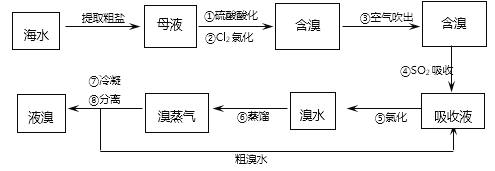
(1)粗盐中含有多种可溶性杂质如氯化镁、硫酸钠、氯化钙和一些不溶性杂质。粗盐的初步提纯需要先除去不溶性杂质,进行此实验时需要用到的玻璃仪器有烧杯、酒精灯、玻璃棒、量筒、胶头滴管和______。若需要将粗盐精制,则要除净其中的氯化镁、硫酸钠、氯化钙等可溶性杂质,常需用的试剂有:盐酸(过量)、BaCl2溶液(过量)、NaOH溶液(过量)和Na2CO3溶液(过量)。在此精制过程中,滴加过量盐酸的作用是________。
(2)步骤④:含溴(Br2)的空气被SO2吸收会转化成HBr和硫酸,请写出发生反应的化学方程式______。
(3)步骤⑥中的“蒸馏”是一种分离沸点相差较大的液体混合物的方法,根据物质沸点的差异通过控制温度进行分离。蒸馏过程中发生了__________(填“物理”或“化学”)变化。已知溴的沸点是58.5℃,而实际溴出口温度一般控制在80—90℃,温度过高或过低都不利于生产。温度不能过高的原因是______。
(4)氯化后的海水也含有溴单质,为什么不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”,其原因是____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】菱铁矿(主要成分是FeCO3)是炼铁的原料。现取30.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。已知:
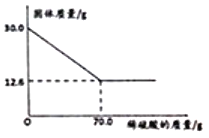
①FeCO3+H2SO4=FeSO4+CO2↑+H2O;②菱铁矿中杂质不参加反应,且难溶于水。请计算:
(1)30.0g菱铁矿中FeCO3的质量为__________g。
(2)所用稀硫酸的溶质质量分数(结果准确到0.1%)____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】玫瑰花中含有丁香油酚等,因而具有特殊的香味,丁香油酚的化学式为C10H12O2。下列说法错误的是( )
A. 丁香油酚中氢、氧元素的质量比为3∶8
B. 丁香油酚中氢元素的质量分数为12/164×100%
C. 丁香油酚分子中C、H、O的原子个数之比为5∶6∶l
D. 一个丁香油酚分子由10个C原子、12个H原子和1个O2分子构成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com