
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| OH- | Cl- | CO32- | HCO3- | |
| H+ | 溶、挥 | 溶、挥 | 溶、挥 | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 溶 |
| 实验步骤 | 实验操作 | 实验中可能出现的现象 | 相应结论 |
| 向A的试样中加入足量的水 | ①A的试样全部溶解 | A是Na2CO3和NaHCO3 | |
| ②A的试样部分溶解 | A是Na2CO3和CaCO3或NaHCO3和CaCO3 | ||
| 若A的试样部分溶解则向其滤液中加入 | ③液溶液显红色 | A是Na2CO3和CaCO3 | |
| ④溶液显浅红色 | A是NaHCO3和CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
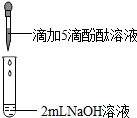 合肥市16年中考理科实验操作中,在NaOH溶液滴加酚酞溶液变红.有细心的同学发现,偶尔有意想不到的现象:有时溶液变红后很快褪成无色;有的溶液中出现白色浑浊物.
合肥市16年中考理科实验操作中,在NaOH溶液滴加酚酞溶液变红.有细心的同学发现,偶尔有意想不到的现象:有时溶液变红后很快褪成无色;有的溶液中出现白色浑浊物.| 实验 | 实验操作 | 实验现象 | |
| 1 | 将NaOH溶液加热煮沸,向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | 溶液变红,过一会儿红色消失 | |
| 2 | 向盛有2mL碳酸钠溶液的试管中滴加5滴0.5%的酚酞溶液 | 溶液变红 | |
| 3 | 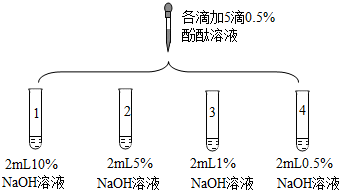 | 1号试管0.1min红色褪去 2号试管5min红色褪去 3号试管30min红色明显变浅 4号试管120min红色无明显变化 | |
| 4 | 取3支试管,分别加入2mL 水,分别滴加5滴5%的酚酞试液、2%的酚酞试液、0.5%的酚酞试液 | 酚酞溶液浓/% | 浑浊程度[来 |
| 5 | 大量浑浊物 | ||
| 2 | 少量浑浊物 | ||
| 0.5 | 无浑浊物 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10g/100g水 | B. | 20g/100g水 | C. | 30g/100g水 | D. | 40g/100g水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com