
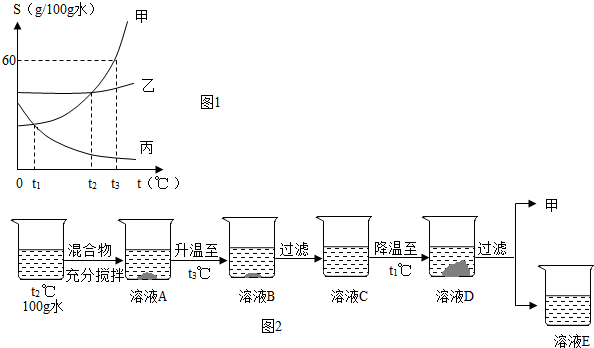
分析 ①溶解度曲线的交点表示该温度下两物质的溶解度相等;
②气体的溶解度随温度的升高而减小;
③据该温度下甲的溶解度及溶质的质量分数=$\frac{溶质的质量}{溶质的质量+溶剂的质量}$×100%分析解答;
④根据溶解度曲线的意义进行分析解答,根据溶解度曲线即可判断相同温度下各物质溶解度的大小,并结合饱和溶液中溶解度大则溶质的 质量分数大分析解答;
⑤据t3℃时三种物质的溶解度关系及降温溶液中溶剂的质量不变分析解答.
解答 解:①t1℃时,甲、丙的溶解度曲线相交于一点,二者的溶解度相同;
②若甲、乙、丙三种物质中,有一种是气态物质,则该物质是丙,因为丙的溶解度随温度的升高而减小;
③t3℃时甲的溶解度是60g,即100g水中最多溶解60g的甲,所以将35g 甲物质放入50g水中,充分溶解最多溶解30g,所得溶液的总质量为80g;若要进一步增大上述溶液的溶质质量分数,可以采用的方法是升温,因为其溶解度随温度升高而增大,升温后未溶解的溶质继续溶解,而溶剂的质量不变,则质量分数变大;
④饱和时质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,则饱和溶液中溶解度大则溶质的质量分数大;某同学想提纯甲中混有少量乙的混合物,首先配成t2℃时的甲的饱和溶液,且有溶质剩余,然后升温至t3℃,甲的溶解度增大,溶解一部分依然有溶质剩余,说明仍然是饱和溶液,然后过滤,过滤后的溶液还是该温度下的甲的饱和溶液,所以BC溶质质量分数相等,且大于A的质量分数;降温至t1℃甲的溶解度减小且小于t2℃时的甲的溶解度,所以析出晶体,过滤后的溶液是该温度下的饱和溶液,则溶质质量分数大小为A>D=E;整个过程中溶液溶质质量分数关系是:C=B>A>D=E;
⑤温度为t3℃时,三种物质中丙的溶解度最小,所以该温度下等质量的饱和溶液中甲含有的溶质质量最多,溶剂质量最小,将等质量甲、乙、丙三种物质的饱和溶液分别降温至低于t1℃,溶剂质量不变,所以溶剂质量最少的是甲;
故答案为:
①t1;②丙;③80;升高温度;④C=B>A>D=E; ⑤甲.
点评 本题着重考查了学生对溶解度曲线知识的掌握和分析、解决问题的能力,要结合所学知识细心分析解答.


科目:初中化学 来源: 题型:选择题
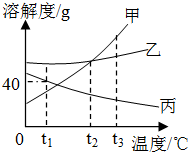
| A. | t2℃时,甲、乙两种物质的溶解度相等 | |
| B. | 当甲中含少量乙时,可用冷却热饱和溶液的方法提纯甲 | |
| C. | 分别将t3℃时等质量的甲、乙、丙的饱和溶液降温至t1℃,析出晶体最多的是甲 | |
| D. | t1℃时,某同学将40克丙固体加入60克水中,配成了溶质的质量分数为40%的丙溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
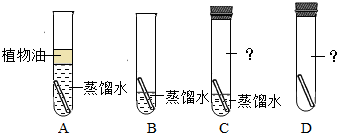
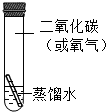 .
.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 11.7g | B. | 1.17g | C. | 5.85g | D. | 58.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | MgCl2、KOH、NaCl | B. | Na2SO4、BaCl2、HCl | ||
| C. | CuSO4、HCl、KCl | D. | Na2CO3、NaCl、K2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使反应顺利进行,则可以从长颈漏斗中添加的试剂是( )
如图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使反应顺利进行,则可以从长颈漏斗中添加的试剂是( )| A. | ①②④ | B. | ①③④ | C. | ②③⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
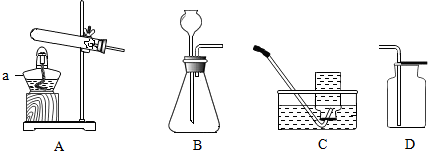
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
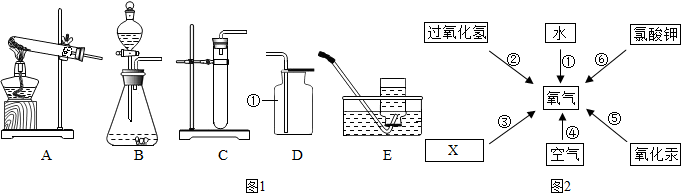
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com