
【题目】回答下列问题
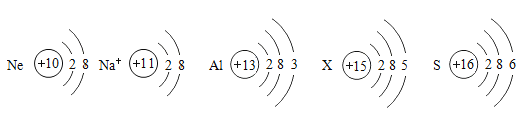
(1)具有相对稳定结构的原子是_________(填元素符号)。
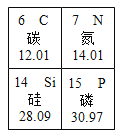
(2)含有X元素的化合物常用作化肥,请结合信息,回答:X元素的原子序数是_______,相对原子质量为______。
(3)在某金属单质与硫单质反应过程中,硫原子得到2个电子形成硫离子。下列说法正确的是_______(填字母序号)。
A 硫离子属于阴离子
B 硫离子可表示为S2+
C “S”既可以表示硫原子,也可以表示硫元素
D 硫离子的核外电子数与质子数相等
(4)我国是燃煤大国,烟道气体脱硫是治理燃煤带来的环境污染的重要措施之一。烟道气体脱硫中的“硫”指的是___________(填字母序号)。
A 单质
B 元素
C 分子
D 离子
【答案】Ne 15 30.97 AC B
【解析】
(1)最外层电子数为8的结构相对稳定,则具有相对稳定结构的原子是Ne。钠离子(Na+)不属于原子;
(2)X元素的原子中含有15个质子,原子序数是15,相对原子质量为30.97。
(3)在某金属单质与硫单质反应过程中,硫原子得到2个电子形成硫离子。下列说法正确的是:
A、硫原子得到2个电子形成硫离子,硫离子属于阴离;故选项正确;
B、硫离子带2个单位负电荷,可表示为S2-;故选项错误;
C、“S”既可以表示硫原子,也可以表示硫元素;故选项正确;
D、硫离子的核外电子数为18,质子数为16,两者不相等;故选项错误;
故选:AC。
(4)烟道气体脱硫中的“硫”是以化合物的形式存在,指的是硫元素;
故选:B。


科目:初中化学 来源: 题型:
【题目】在硝酸银溶液中加入过量铜屑充分反应。(注:析出的银单质呈黑色)

(1)可以看到的现象是_____。
(2)如图表示该反应前后溶液中存在的主要离子,请写出每种小球代表的离子分别是什么(填离子符号);
![]() :_____;
:_____;![]() :_____;
:_____;![]() :_____。
:_____。
(3)下列金属中能与硝酸银发生相同类型的反应是_____(填选项)
A Au B Zn C Na D Hg
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组欲探究实验室的一包白色固体( 已知含碳酸钠)的具体成分 。
他们猜测可能含有硝酸钡、硫酸钠、氢氧化钠中的一种或几种。 通过查阅资料发现硝酸钡溶于水呈中性,硫酸钠溶于水呈弱碱性。以下是实验步骤:
步骤一:取少量白色固体于烧杯中.向烧杯中加入足量水并不断搅拌,固体部分溶解。
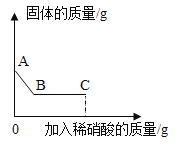
步骤二:接着向烧杯中加入足量稀硝酸并不断搅拌,测定固体质量变化,并画出如图所示图象。
(1)步骤一的实验目的是_______________________________________;
(2)步骤二中他们观察到的现象是_____________________________;综合步骤一、步骤二能确定该白色粉末中一定含有_____________________________。
(3)若要继续确定该白色粉末的成分,请你设计实验方案:
实验操作 | 预期实验现象 | 实验结论 |
____ | _____ | ____ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有Ca(OH)2、CaCO3和一些杂质(不与稀盐酸反应)组成的混合物共15g,取某浓度的稀盐酸,逐滴滴加到混合物中,充分反应,测得稀盐酸的质量与反应生成气体的质量,关系如图所示:
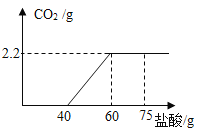
(1)生成CO2的质量是_______g;
(2)计算混合物中CaCO3的质量分数 (写出计算过程,结果精确到0.1%)_____;
(3)所取稀盐酸的浓度是______,欲配制100g该浓度的稀盐酸,需要溶质质量分数为36.5%的盐酸_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将7g废铁屑放入盛有100g7.3%稀盐酸的烧杯中,恰好完全反应(假设杂质不参加反应)。此时测得烧杯内各物质的总质量为106.8g。计算:(有关反应的化学方程式为:Fe+2HCl=FeCl2+H2↑)
(1)稀释_____g20%的盐酸溶液可得100g7.3%的稀盐酸。
(2)反应产生氢气的质量为_____g。
(3)废铁屑中铁的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲同学对寒痛乐熨剂(简称“寒痛乐”)的发热原理产生了浓厚兴趣,于是带了几包寒痛乐,来到实验室对其进行研究。

(查阅资料)
[用法用量] 外用,一日1次。将外袋剪开,取出药袋,晃动数次,使药物充分松散,接触空气,手摸有热感时,置于固定袋内,覆盖于痛患处,每袋可发热不少于15小时。
[原料层] 铁、蛭石、活性炭、水等。
[作用原理] 铁跟氧气和水反应生成氢氧化铁(固体),并放热。
(实验一)验证寒痛乐成分中所含铁的化学性质。
步骤 | 实验操作 | 实验现象 |
① | 将寒痛乐打开,将药物倒入一烧杯中,观察 | 药物为黑色固体粉末 |
② | 用一条形磁铁与烧杯中的黑色粉末充分接触,取适量吸附在磁铁上的黑色粉末放于燃烧匙中,在酒精灯上点燃后伸入盛有氧气的集气瓶中,观察 | 剧烈燃烧,_ |
实验结论:写出此反应的文字表达式_。集气瓶中加水的作用是__。
(实验二)用寒痛乐熨剂药粉测定空气中氧气的含量。
甲同学设计了如图所示装置,进行实验。

(实验记录 )
步骤 | 实验操作 | 主要实验现象 | 实验结论及解释 |
① | 连接好装置如上图所示,然后_____ | _______ | 装置的气密性良好 |
② | 加入足量药品,迅速将胶塞盖严,并充分振荡 | _____ | 进入集气瓶内水的体积即为空气中氧气的含量。 |
(实验反思)乙同学认为甲同学所做“寒痛乐药粉测定空气中氧气的含量”的实验不能证明上述结论,他将操作改进后再进行测量,得到了较为准确的结果。他改进后的操作为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你参与某学习小组的探究活动,并回答相关问题:
[发现问题]小丽发现盛水的铁锅在与水面接触的部位最易生锈;小茜发现自己的铜
制眼眶表面出现了绿色的铜锈;小玲发现苹果切开不久,果肉上会产生一层咖啡色物质,好像生了“锈”一般.
[提出问题]这三种物质“生锈”的原因是什么?
[收集证据] (1)回忆已有知识:铁生锈的条件是______________________________.
[查阅有关资料]“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成咖啡色的物质.碱石灰能吸水.
[实验探究]将四小块铜片分别按下图所示放置一个月,观察现象如下:
实验 装置 |
|
|
|
|
实验验象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重 |
由实验可知,铜生锈是铜与水、__________、_________等物质共同作用的结果.
[得出结论]经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与___________________(填物质名称)有关.
[反思与应用] 利用所得结论填空:
(1)写出一种防止铁或铜等金属制品生锈的具体方法_________________________.
(2)请你提出一条延长食品保质期的建议___________________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2020年1月16日,我国首颗通信能力达10 Gbps的低轨宽带通信卫星发射成功。
(1)高氯酸钾(KClO4)可用作固体火箭燃料,标出氯元素的化合价________________。
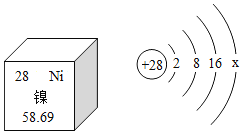
(2)“高分五号”是用钛镍形状记忆合金制作而成的卫星天线。如图是镍元素在元素周期表中的部分信息及原子结构示意图,镍原子的相对原子质量为________________,x=________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com