
【题目】在硝酸银溶液中加入过量铜屑充分反应。(注:析出的银单质呈黑色)

(1)可以看到的现象是_____。
(2)如图表示该反应前后溶液中存在的主要离子,请写出每种小球代表的离子分别是什么(填离子符号);
![]() :_____;
:_____;![]() :_____;
:_____;![]() :_____。
:_____。
(3)下列金属中能与硝酸银发生相同类型的反应是_____(填选项)
A Au B Zn C Na D Hg
【答案】铜表面有黑色固体析出,溶液逐渐由无色变为蓝色 Ag+ Cu2+ NO3- BD
【解析】
(1)在硝酸银溶液中加入过量铜屑充分反应产生银和硝酸铜溶液,可以看到的现象是:铜表面有黑色固体析出,溶液逐渐由无色变为蓝色;
(2)硝酸银与铜反应产生硝酸铜和银,银离子消失,铜离子产生,![]() 表示银离子:Ag+;
表示银离子:Ag+;![]() 表示铜离子:Cu2+;
表示铜离子:Cu2+;![]() 反应前后没有改变的是硝酸根:NO3-。
反应前后没有改变的是硝酸根:NO3-。
(3)
A、Au的活泼性小于银,不能与硝酸银发生置换反应;
B、Zn的活泼性大于银,能与硝酸银发生置换反应;
C、Na的金属活泼性很强,直接与溶液中的水发生反应,不能与硝酸银发生置换反应;
D、Hg的金属活泼性大于银,能与硝酸银发生置换反应;
故选:BD。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案科目:初中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水的固体,受热易分解,是生产电池、涂料以及感光材料的原材料。为探究纯净草酸亚铁晶体热分解的产物,设计装置图如下:
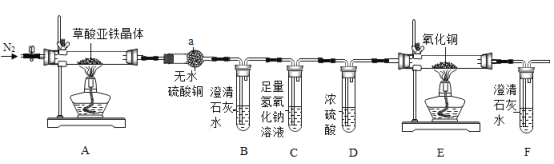
(1)实验中观察到仪器a中白色固体变蓝,可见草酸亚铁晶体分解产物中含有的物质是____。
(2)从绿色化学考虑,该套装置存在的明显缺陷是___________。
(3)实验前先通入一段时间N2,其目为__________。
(4)实验证明了气体产物中含有CO,依据的实验现为__________。
(5)称取5.40g草酸亚铁晶体用热重法对其进行热分解,得到剩余固体质量随温度变化的曲线如下图所示:
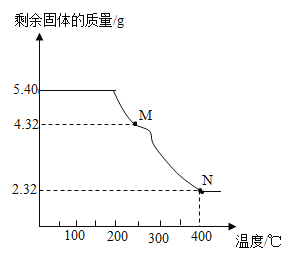
①上图中M点对应物质的化学式为_____。
②已知400℃时,剩余固体是铁的一种氧化物,试通过计算写出M→N发生反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述对应的示意图象表示正确的是( )
A. 加热一定质量的高锰酸钾固体
加热一定质量的高锰酸钾固体
B. 向硝酸钾饱和溶液中加入固体硝酸钾
向硝酸钾饱和溶液中加入固体硝酸钾
C. 向一定二氧化锰中加入过量过氧化氢溶液
向一定二氧化锰中加入过量过氧化氢溶液
D. 将等质量的铁、镁分别投入到足量等溶质质量分数的稀硫酸中
将等质量的铁、镁分别投入到足量等溶质质量分数的稀硫酸中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阿司匹林泡腾片是一种白色片状固体,具有解热镇痛作用,常用于治疗感冒发烧等疾病。下图是关于它的成份表说明书,为了知道其碳酸盐成分,某小组同学进行如下探究。

(初步实验)
(1)将阿司匹林泡腾片放入足量的水中,会产生大量气泡,将生成的气体通入澄清石灰水中,石灰水变浑浊,则产生的气体为______。所以,贮藏该泡腾片时应注意_____。
(成分猜想)
(2)某同学猜想该碳酸盐可能是①CaCO3 ②Na2CO3 ③BaCO3其中猜想③不可能成立,原因是_____。
(综合探究)
(3)①下图装置B中盛放稀盐酸的仪器名称为________;
②下图装置B中橡胶塞细端直径为3 cm,导管的直径为8 mm。从坚固和美观的角度考虑,请你在图圆中标出相应的打孔位置(用三个圆圈“○”表示)。
 ________
________
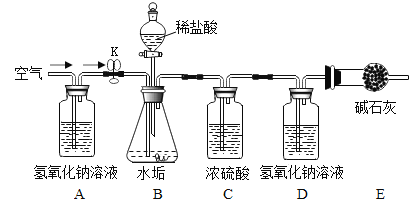
(小资料)碱石灰是氢氧化钠固体和氧化钙固体的混合物。
(4)主要步骤如下:①检查装置的气密性;②称取5.0g泡腾片粉末装入锥形瓶中,打开弹簧夹K,缓缓通入一段时间空气;③称量装置D质量为300.00g,关闭弹簧夹K,滴加足量稀盐酸至完全反应;④打开弹簧夹K,______;(填写实验操作)⑤称量装置D质量为300.44g。
(实验分析)
(5)①反应开始前通入空气的目的是____;
②在B装置中的反应发生时,弹簧夹K处于关闭状态,其原因是__;
③若无E装置,实验后装置D的质量将____(填“>”或“<”或“=”)300.44g;
④下列各项措施中,能提高实验准确度的是____(填字母序号)。
a 缓缓滴加稀盐酸
b 在装置A、B之间增加盛有浓硫酸的洗气瓶
c 在装置B、C之间增加盛有饱和NaHCO3的洗气瓶
⑤计算并推断该碳酸盐(请写出计算过程)____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术。已知反应:![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.铁元素的化合价由+3价升到+6价
B.该反应涉及的物质都是氧化物
C.化学计量数m=n
D.该反应类型为复分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元明粉(Na2SO4)常用于配制印染织物的促染剂,其溶质的质量分数一般在3%-5%范围。
(1)元明粉中钠、硫元素的质量比为_____。(写出最简整数比)
(2)配制1000g溶质的质量分数为4%的促染剂,需要_____mL(保留到小数点后一位)溶质质量分数为20%的硫酸钠溶液,需要水的质量为_____g。(已知常温下溶质质量分数为20%的硫酸钠溶液密度为1.2g/cm3)
(3)将某促染剂逐滴滴入100g氯化钡溶液中,恰好完全反应后过滤,洗涤干燥后得滤渣质量为8g。而氯化钡是由木炭在高温下还原重晶石(主要成分BaSO4)得到BaS,向其中再加入盐酸发生复分解反应而得到的。
①写出硫化钡与盐酸反应生成一种气体的化学方程式_____。
②通过滤渣质量计算需要这种含杂质20%的重晶石_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是几项基本实验操作的示意图
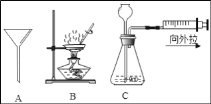
(1)A仪器的名称是_____。
(2)B操作中,玻璃棒的作用是_____,仪器的组装顺序是_____(填序号)。
①铁圈 ②蒸发皿 ③酒精灯
(3)C装置可以检查装置的气密性,当缓慢向外拉动活塞时,如果观察到_____说明气密性良好。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~G是初中化学常见的物质,其中A、B、D、E都是氧化物,C、F、G都是金属单质,A为红棕色固体,E为黑色固体,它们之间的转化关系如图所示(部分反应物和生成物已略去)。请回答:
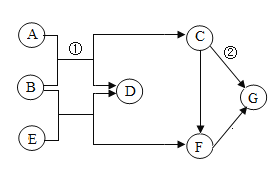
(1)E的化学式为_________。
(2)D的一种用途是_______________。
(3)C、F、G三种金属的活动性由弱到强的顺序为____________。
(4)反应①的化学方程式为__________。反应②的基本反应类型是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回答下列问题
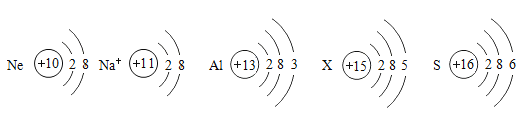
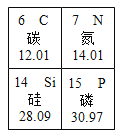
(1)具有相对稳定结构的原子是_________(填元素符号)。
(2)含有X元素的化合物常用作化肥,请结合信息,回答:X元素的原子序数是_______,相对原子质量为______。
(3)在某金属单质与硫单质反应过程中,硫原子得到2个电子形成硫离子。下列说法正确的是_______(填字母序号)。
A 硫离子属于阴离子
B 硫离子可表示为S2+
C “S”既可以表示硫原子,也可以表示硫元素
D 硫离子的核外电子数与质子数相等
(4)我国是燃煤大国,烟道气体脱硫是治理燃煤带来的环境污染的重要措施之一。烟道气体脱硫中的“硫”指的是___________(填字母序号)。
A 单质
B 元素
C 分子
D 离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com