
【题目】A、B、C、D中都含有地壳中含量最多的元素,它们之间的关系如图所示,一表示物质间可以相互反应,→表示一种物质可以转化成另一种物质。B可用于光合作用,A→D放热反应。
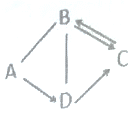
(1)B在生活中的用途是______。
(2)C的化学式为________。
(3)A→D反应的化学方程式是_______,基本反应类型是______
【答案】灭火等 CaCO3 CaO+ H2O= Ca(OH)2 化合反应
【解析】
A、B、C、D中都含有地壳中含量最多的元素,所以四种物质中都含有氧元素,B可用于光合作用,B为二氧化碳;A→D放热反应,氧化钙和水反应生成氢氧化钙,反应放热,所以A为氧化钙或水,D为氢氧化钙;A能与二氧化碳,所以A为水;二氧化碳和氢氧化钙反应生成碳酸钙,碳酸钙和盐酸反应或碳酸钙高温下分解都生成二氧化碳,所以C为碳酸钙,带入检验,合理。
(1)二氧化碳在生活中的用途是灭火(或其它合理答案);
(2)碳酸钙的化学式为CaCO3;
(3)氧化钙和水反应生成氢氧化钙的化学方程式是:CaO+ H2O= Ca(OH)2,基本反应类型是由两种物质生成一种物质的化合反应。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图是太阳能燃料电池的组成与功能示意图,请根据图示回答下列问题:

(1)电解槽的作用是电解水,写出该反应的化学方程式:_________;电解一定量的水,当正极产生5L气体时,负极产生的气体体积是 ________ L。
(2)夜晚,太阳能燃料电池工作时的能量转化途径为___________(填序号)。
A.太阳能→电能→热能 B.化学能→电能→热能
C.太阳能→化学能→电能→热能 D.电能→化学能→电能→热能
(3)太阳能燃料电池中可循环使用的原料是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对石灰石样品进行如下实验取12g样品放入烧杯中,将100g稀盐酸分4次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
求:
(1)样品中碳酸钙的质量为_____g:
(2)第4次加入稀盐酸后所得溶液中CaCl2的质量分数_______。(写出计算过程,最终结果保留0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中兴缺“芯”事件震惊国人。芯片的主要成分是纯度极高的硅。高纯硅的制备以石英砂(主要成分是二氧化硅)为原料,生产过程示意图如下:
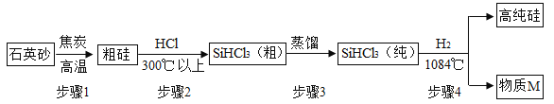
(1)上述四个步骤中属于物理变化的是______。
(2)物质M是该生产过程中可循环使用的物质,写出步骤4反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气中有多种成分
(1)奥运火炬的外壁上有成百上千个通气孔,这些孔不仅能把燃烧的废气排出去,还能_____以保证燃料能充分的燃烧。
(2)为防止深海潜水员患气体栓塞、减压病,潜水员在水下呼吸用的气体是由氧气和氮气按一定比例混合而成的人造空气。请写出氮气的化学式_______。
(3)汽车安全气囊中装有叠氮化钠(NaN3)等固体粉末,当发生碰撞时,叠氮化钠会分解释放出氮气,保护乘车人的安全。工业上利用以下反应制取叠氮化钠:第一步2Na+2NH3![]() 2NaNH2+H2↑;第二步:2NaNH2+N20
2NaNH2+H2↑;第二步:2NaNH2+N20![]() NaN3+X+NH3↑;第二步反应中X的化学式为_________。
NaN3+X+NH3↑;第二步反应中X的化学式为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年5月18日,我国首次海域可燃冰试采成功(如图1),实现了历史性的突破。可燃冰的最大特点是能量密度高,其主要成分是甲烷,甲烷燃烧的微观示意图如图2。依据图示,判断下列叙述正确的是( )
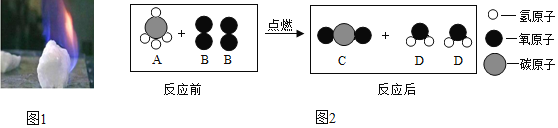
A. 化学方程式为![]()
B. 反应前后,元素和分子的种类都没有变化
C. 反应前后,氢原子、碳原子和氧原子的数目都没有改变
D. 反应中![]() 、
、![]() 、
、![]() 、
、![]() 四种分子的个数比是
四种分子的个数比是![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】构建知识网络能帮助我们理解知识间的内在联系,有助于知识的迁移与应用。如图为初中化学几种常见物质及其转化关系(部分反应物和生成物以及反应条件被省略)。已知![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 是初中化学中常见的物质,其中
是初中化学中常见的物质,其中![]() 为黑色单质,
为黑色单质,![]() 为红色金属,
为红色金属,![]() 、
、![]() 为氧化物,
为氧化物,![]() 是白色不溶于水的物质。
是白色不溶于水的物质。
请根据图示回答:
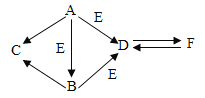
(1)![]() 的化学式为__________,固态
的化学式为__________,固态![]() 的名称为__________。
的名称为__________。
(2)![]() 的化学方程式__________。
的化学方程式__________。
(3)![]() 的化学方程式__________。
的化学方程式__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示,某校化学兴趣小组用过氧化氢(H2O2)溶液(MnO2作催化剂) 制取干燥氧气,并用来测定 10g 某铜粉样品(含少量杂质碳)中铜的质量分数。
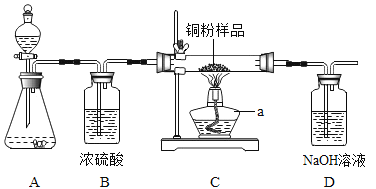
回答下列问题:(温馨提示:2Cu+O2![]() 2CuO;氢氧化钠溶液可以吸收二氧化碳)
2CuO;氢氧化钠溶液可以吸收二氧化碳)
(实验一)
(1)装置A 中发生的化学方程式是__________。装置B的作用是__________。
(2)通过称量完全反应前后装置__________的质量,进行计算便可求出样品中铜的质量分数。
(3)实验完毕,小华同学误将用剩的H2O2溶液和装置C玻璃管中的剩余固体一起倒入烧杯中,发同有大量的气泡产生,经检验确认产生的气体是氧气,小江和小田两位同学对此颇感兴趣,进而展开了他们的探究之旅。
(提出问题)
是哪种物质加快了H2O2的分解速率?
(大胆猜想)
猜想①:剩余固体中的氧化铜加快了H2O2溶液的分解。
猜想②:氧化铜能做H2O2分解的催化剂。
(实验二)
实验方案 | 实验现象 | 分析及结论 |
步骤一:将带火星的木条伸入盛有5mL5%过氧化氢溶液的试管。 | 带火星木条不复燃 | H2O2溶液常温下产生氧气的量很少,不足以使带火星复燃。 |
步骤二:向盛有 5mL5%H2O2溶液的试管中加入 1g 氧化铜固体,将一根带火星的木条伸入试管中。观察现象。待反应结束后将试管里的剩余物进行___________、洗涤、干燥、称量。对比反应前后固体的质量。 | 称得固体质量为 1g | 猜想①成立,并且反应前后固体的质量相等。 |
(讨论交流)
小川同学认为,根据步骤一、二的实验现象,得出的两个结论就能判断猜想②成立。你是否支持他的观点?___________。若要证明猜想②成立,你认为还应补做的实验是___________。
(4)该化学兴趣小组利用压强传感器,对MnO2、CuO、Fe2O3三种金属氧化物中,哪一个更适宜作过氧化氢制取氧气的催化剂,又做了如下数字化实验探究。
(实验三)实验方法如下:
Ⅰ.用MnO2、CuO、Fe2O3三种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用如下图所示装置进行实验。改用其他两种微球,分别重复上述实验,得到的锥形瓶内压强随时间变化的曲线如下图所示。
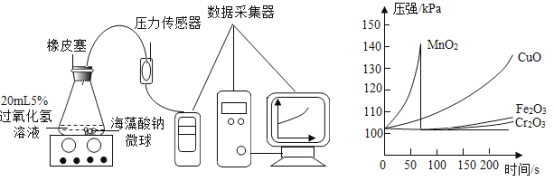
①每次重复实验时,海藻酸钠微球数应相同的原因是_________________________________。
②用含MnO2的海藻酸钠微球进行实验,60s 时压强瞬间回落,其原因可能是____________________。
③从实验曲线看,催化效果较好,反应温和的催化剂是______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其围观示意图如图(图中的微粒恰好完全反应),下列说法正确的是( )
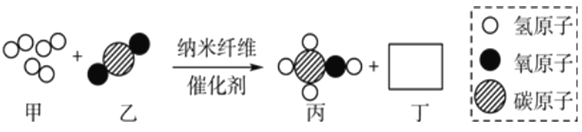
A. 丁的化学式为H2O,该反应为复分解反应
B. 参加反应的甲与乙的质量比为3:1
C. 甲是单质,乙、丙、丁均为氧化物
D. 该反应体现了化学反应中分子可分,原子不可再分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com