
【题目】钢铁的冶炼是人类文明的一个重要标志。下图1是实验室模拟炼铁的装置图。
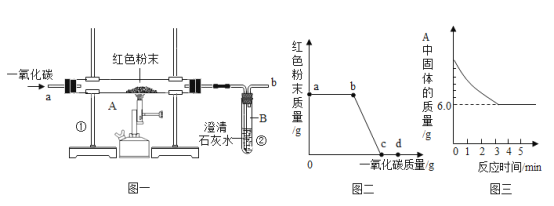
(1)写出图一中②处发生的化学反应方程式:___________________________________;
(2)实验过程中通入CO质量与红色粉末质量的关系如图2所示。根据图示,下列说法不正确的是_______(填序号)
①a 点表示开始通入CO,反应开始发生;
②b 点表示通入CO一段时间后加热,反应开始发生;
③c 点表示红色粉末已充分参加反应;
④d 点表示反应结束后仍需继续通入CO;
⑤可根据通入CO的质量计算出红色粉末的质量。
(3)图一装置中的不足之处是__________________________________;
(4)该实验炼制的铁与工业炼制出的铁最大的区别是________________________。
(5)某化学小组的同学们利用上述实验对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们取了固体样品质量7.2 g,用图1所示的装置重新实验,测定的部分数据如图3所示,则原样品中铁元素与氧元素的质量比是__________。
【答案】![]() ①⑤。 无尾气处理装置 该装置炼制的铁是纯净物,工业炼制的生铁是混合物 5:1
①⑤。 无尾气处理装置 该装置炼制的铁是纯净物,工业炼制的生铁是混合物 5:1
【解析】
图一中一氧化碳和氧化铁在高温条件下反应生成二氧化碳和铁,二氧化碳使澄清的石灰水变浑浊。图2一开始通入一氧化碳时,氧化铁质量不变,是因为装置中有空气,先用一氧化碳将空气排净,再点燃酒精喷灯,这时一氧化碳与氧化铁反应,反应结束后,为了防止倒吸,需继续通一氧化碳直至冷却至室温。
(1)图一中②处澄清的石灰水变浑浊,是二氧化碳和氢氧化钙反应生成了碳酸钙沉淀和水,化学方程式为![]() ;
;
(2)图二中a点反应并未开始,而是用一氧化碳将装置中的空气排净,b点一氧化碳与氧化铁开始反应,红色粉末质量减小,到c点反应结束,红色粉末质量不再变化,为了防止倒吸,需继续通一氧化碳直至冷却至室温。因为通入的一氧化碳不是都和氧化铁反应了,所以不能根据通入一氧化碳的质量计算出氧化铁的质量,故错误的是①⑤;
(3)一氧化碳有毒,不能直接排放到空气中,图1装置中的不足之处是无尾气处理装置;
(4)该实验炼制的铁与工业炼制出的铁最大的区别是该装置炼制的铁是纯净物,工业炼制的生铁是混合物;
(5)因为样品由氧化铁和铁粉混合而成,所以样品中只有两种元素:铁元素和氧元素,总质量为7.2g。反应完全后固体中只剩铁元素,根据质量守恒定律,反应前后铁元素的质量不变,所以样品中铁元素的质量就是6.0g,减少的质量是氧元素的质量1.2g,故样品中铁元素与氧元素的质量比=6.0:1.2=5:1。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 油脂是重要的营养物质,正常情况下,每人每天需要摄入![]()
B. 废电池中含有铅、镍、镉、汞,若随意丢弃会造成地下水和土壤污染
C. 碘是甲状腺素的重要成分,患有甲状腺肿大的病人应禁止碘的摄入
D. 食品添加剂虽然都是化学合成物质,但可以改善食品品质,可以适量使用
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列方法不能达到除杂目的的是( )
选项 | 物质(括号内为杂质) | 方法 |
A | N2(O2) | 将混合气体通过灼热铜网 |
B | Fe粉(Cu粉) | 加入足量稀H2SO4充分反应,过滤,洗涤,干燥 |
C | CaO(CaCO3) | 高温煅烧 |
D | FeCl2溶液(CuCl2) | 加入足量Fe粉,充分反应后过滤 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列图示,回答相关问题:
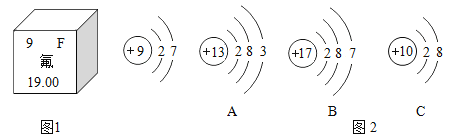
(1) 氟的相对原子质量为___________,氟元素的化学性质与图中______________(填字母序号)化学性质相似。
(2) A在化学变化中容易______________(填“得”或“失”)电子;AB对应的元素组成的物质的化学式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的SO2(Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H 2O),老师给他们提供了一瓶久置的亚硫酸钠溶液,兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
(查阅资料)
① Na2SO3不稳定,在空气中易被氧气氧化成Na2SO4;
②SO32-、SO42-均能与Ba2+反应产生白色沉淀;
③BaSO3 等亚硫酸盐能与稀盐酸反应,其反应原理与 BaCO3等碳酸盐与稀盐酸反应类似。
(1)(提出问题)①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
(分析问题) Na2SO3变质的原因是:_______________________。(用化学方程式表示)
(2) (作出猜想)
猜想1:没有变质,成分是Na2SO3;
猜想 2:完全变质,成分是Na2SO4;
猜想3:_____________。
(实验探究Ⅰ)甲、乙两组分别进行实验探究溶液是否变质:
小组 | 实验操作 | 现象 | 结论 |
甲组 | 取少量样品于试管中加入过量稀盐酸; | 产生气泡 | 没有变质,还是Na2SO3 |
乙组 | 取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸。 | 产生白色沉淀后 ________ | 已部分变质 |
甲组同学实验中发生的化学方程式为:________________________。有同学质疑甲组方案不合理,理由是_________________。
(3) (实验探究Ⅱ)甲组设计如下实验装置测定Na2SO3溶液的溶质质量分数。(已![]() )
)

①要测定Na2SO3溶液的溶质质量分数,实验中需要测得的数据是亚硫酸钠溶液样品的质量以及_______质量。
②D装置的作用为______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们的初中化学实验中有很多都与气压变化有关,请回答下列问题:
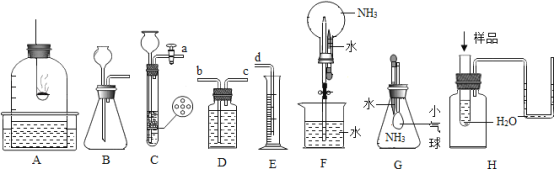
(1)如图A装置用红磷测定空气中氧气的体积分数,请写出化学方程式:_____,充分反应后,应先______,再读数,否则测得结果将_____![]() (填“大于”、“等于”或“小于”)。
(填“大于”、“等于”或“小于”)。
(2)实验室可用注射器连接到装置 B 的导管处,检查装置B的气密性.实验步骤:向锥形瓶中加水至____,向后拉动注射活塞,若观察到______时,则说明装置B气密性良好。
(3)实验室利用装置C制备H2,化学方程式为_____,相比较装置B,它的优点是_____,若选用装置D、E测定生成H2的体积,仪器连接顺序为a→____→______→d。
(4)装置F和G可用于验证NH3极易溶于水,F装置的实验现象是______,G装置的实验现象是_____。
(5)在装置H中,某样品投入到水中,右侧U型管出现液面左低右高现象,则该样品不可能是____。
① CaO ② NaOH固体 ③ 浓硫酸 ④ NH4NO3固体.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,它与我们的生活息息相关。
(1)“健康饮食、均衡营养”是青少年健康成长的重要保证。下列物质中富含蛋白质的有________(填字母)。
A 米饭和馒头 B 大豆油和花生油 C 牛肉和鸡蛋 D 蔬菜和水果
(2)“食品安全”是一个永恒的话题。你认为下列认识科学的是________(填字母)。
A 任何食品都不可以使用食品添加剂
B 霉变的大米、花生,即使经过蒸煮也不能食用
C 含钙、锌的奶粉有利于补充人体所需的常量元素
D 用工业用盐亚硝酸钠代替食盐来腌渍食品
(3)生活中可用__________鉴别硬水和软水。
(4)加入洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的________作用。
(5)尿素是一种常用的化肥,工业上生产尿素反应的微观示意图如图:
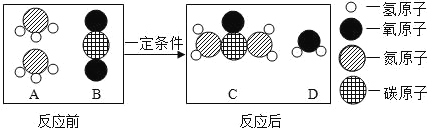
该反应中两种反应物A和B的质量比为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2011年11月,国家环境保护部将PM2.5作为一般评价项目纳入标准。PM2.5是指大气中直径≤2.5微米的颗粒物,与较粗的可吸入颗粒物相比,PM2.5粒径小,对人体健康和大气环境质量的影响更大。一般而言,PM2.5主要来自化石燃料的燃烧、有机物的挥发等。
(1)下途径中,产生PM2.5相对较少的是_____
A 道路扬尘 B 煤炭发电 C 炼制石油 D 汽车尾气
(2)减少煤、_____和天然气等化石燃料的燃烧,会有助于减少二氧化碳的产生。化石燃料燃烧时排放出的___________在空气中反应后的生成物溶于雨水,会形成酸雨。
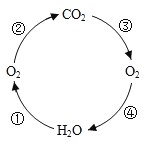
(3)如图是自然界碳、氧循环简图
a.图中③是自然界中消耗二氧化碳的主要途径,其名称为___。
b.写出图中①反应的化学方程式:_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们在学完酸的化学性质后,做了如下实验:
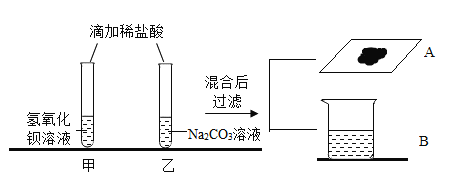
[观察与讨论1]乙试管中观察到_____现象,小组的同学们将实验后溶液混合起来对废液进行处理,混合过程中产生气泡,于是小组同学得出反应后甲试管中的溶质是_____,充分反应后过滤,得到滤液B和滤渣A,向滤渣中加稀硝酸,发现固体表面产生气泡,同学们接着对滤液B中的成分进行探究。
[提出问题1]滤液B中的含有哪些离子?
[猜想与假设]小欣同学猜想:Na+、Cl-
小研同学猜想:Na+、Cl-、SO42-
小洋同学猜想:Na+、Cl-、Ba2+、H+
你的猜想_____(一种即可)
[实验与探究]小研同学认为不需要证明就可得出_____的结论是错误的。
小研同学为证明自己猜想正确,取滤液少量加入足量的氯化钡溶液,发现溶液中产生白色沉淀,继续加入足量稀盐酸,一段时间后观察,固体不消失,则证明自己结论正确。请你对她的结论进行评价_____。
为了进一步证明滤液中离子成分,小群同学取滤液少量加入_____,根据产生的现象即可得出滤液中的离子成分。
[归纳总结]通过以上实验我们能够总结出,在研究反应后溶液中离子成分时,首先应该根据实验现象判断出_____的离子是一定不存在的。在探究过程中,加入试剂后,对物质在_____的现象,进行系统地、细致地观察和描述,得出可靠的结论。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com