
(5分)硫酸铜溶液对过氧化氢(H2O2)的分解有催化作用。取8.5%的过氧化氢溶液40 g倒入小烧杯中,向其中加入15%的硫酸铜溶液6.6 g,使过氧化氢完全分解。
计算:(1)过氧化氢溶液中溶质的质量为______g。
(2)产生氧气的质量(写出计算过程)。
(3)反应后所得硫酸铜溶液中溶质的质量分数(写出计算过程)。
(1)3.4;(2)[解]设过氧化氢完全分解生成氧气的质量为x。
2H2O2CuSO42H2O + O2↑
68 32
3.4 g x 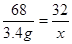 x=1.6g
x=1.6g
答:略。
(3)硫酸铜的质量:6.6 g × 15% =0. 99 g
所得溶液的质量:40 g + 6.6 g -1.6 g=45 g
所得硫酸铜溶液中溶质的质量分数=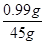 ×100% =2.2%
×100% =2.2%
答:略。
解析试题分析:(1)已知过氧化氢溶液的质量和溶质质量分数,即可求得其溶质质量;(2)利用化学方程式和过氧化氢的质量即可求得生成氧气的质量;(3)利用原硫酸铜溶液的质量和其溶质质量分数即可求得硫酸铜的质量,依据质量守恒定律可以求得放出氧气后的溶液质量,利用溶质质量分数的计算公式即可作答。
考点:溶质质量分数的计算;质量守恒定律;化学方程式的计算


 考前必练系列答案
考前必练系列答案科目:初中化学 来源: 题型:计算题
小英同学为了测定某地区石灰石样品中碳酸钙的质量分数,取该样品15g,现将75mL的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
| 实验 | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸的量/mL | 25 | 25 | 25 |
| 生成气体的质量/g | 2.2 | m | 1.1 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(14分)某兴趣小组用下图所示流程制取氧气(反应原理: 2KClO3 2KCl+3O2↑),并回收提纯氯化钾和二氧化锰。
2KCl+3O2↑),并回收提纯氯化钾和二氧化锰。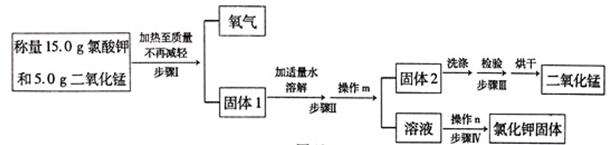
回答下列问题:
(1)根据化学方程式计算,理论上可制得氧气的质量是多少?(计算结果精确到0.1g)
解:
(2)在回收提纯的过程中需要控制水的用量,原因有 (填标号)。
A.提高实验效率 B.保证固体1全部溶解 C.节约能源
(3)①写出下图中仪器a、b的名称: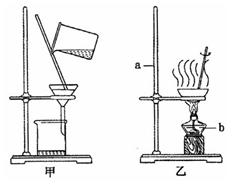
A ,b 。
②步骤Ⅱ中的操作m应选择图11中
(填“甲”或“乙”)装置,该操作中玻璃棒
的作用是 。
③步骤Ⅲ中用酸化的硝酸银(AgNO3)溶液检验洗出液中是否含有氯化钾,该检验方法的原理
为 (用化学方程式表示)。
(4)实验结束后,称得回收到的氯化钾的质量比理论值小,
可能的原因有 (写一点)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有 _性。(1分)
(2)某探究小组的同学对某工业废水(含有H2SO4、HNO3)中H2SO4的含量进行测定.取50g废水于烧杯中,加入足量BaCl2溶液、过滤、洗涤、干燥,得BaSO4固体11.65g.请解答下列问题:
①计算50g废水中H2SO4的溶质质量分数。(3分,要求写出计算过程)
②若改用KOH溶液(利用消耗的KOH的质量)测定50g废水中H2SO4
的含量,结果可能会 ____(选填“偏低”、“偏高”或“不变”),原因是_____________________________________。(每空1分,计2分)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀
质量的关系曲线如图所示。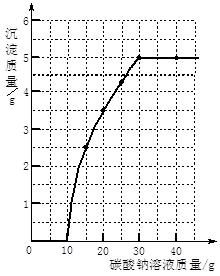
回答下列问题:
(1)从图中看出生成沉淀的最大质量是 g。
(2)开始加入碳酸钠溶液至10g时,还没有沉淀的原
因是 。
(3)计算原滤液中氯化钙的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定实验室废液中硫酸的质量分数。小红同学做了如图所示实验,废液中其他成份不与铁粉发生反应。
请计算:
(1)反应后产生的气体的质量是 g。
(2)该废液中硫酸的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将一定量的石灰石放入烧杯中,加入一定量的稀盐酸,恰好完全反应,产生4.4g气体,反应后所得溶液的溶质的质量分数为20%.(杂质不溶于水,也不参与反应)计算:反应前稀盐酸的溶质的质量分数.(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某烧杯中加入12.5 g含杂质的石灰石,与100 g稀盐酸恰好完全反应(杂质不与盐酸反应也不溶于水),称得烧杯中物质的总质量减少了4.4 g.求:
(1)石灰石含碳酸钙的质量分数.
(2)反应后溶液中溶质的质量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com