
家里蒸馒头用的纯碱中常含有少量的氯化钠,某实验小组要测完该纯碱中碳酸钠的含量,现取该纯碱样品8g,加入一定质量的某稀盐酸中到不再产生气泡为止,得到2.2g气体,试计算并回答
(1)纯碱样品中碳酸钠的质量分数?
(2)反应后所得氯化钠溶液中溶质的质量?
(3)你能否算出反应后所得到溶液中溶质质量分数 ,你的理由是 .
(1)66.25%;(2)8.55g;(3)不能;不能计算反应后溶液的质量.
解析试题分析:(1)设纯碱样品中碳酸钠的质量为x,同时生成氯化钠的质量为y
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
x y 2.2g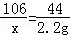

解得:x=5.3g y=5.85g
纯碱样品中Na2CO3的质量分数为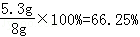
(2)反应后所得氯化钠溶液中溶质的质量为:5.85g+8g﹣5.3g=8.55g
答:(1)纯碱样品中碳酸钠的质量分数为66.25%;
(2)反应后所得氯化钠溶液中溶质的质量为8.55g.
(3)根据溶液中溶质的质量分数的计算公式可以知道,若求算反应后溶液中溶质的质量分数,必须知道反应后溶液的质量和反应后溶质的质量,而本题中不知道加入的盐酸的质量,所以不能计算反应后溶液的质量,故反应后溶液中溶质的质量分数也就无从求算.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:初中化学 来源: 题型:计算题
某锌样品15g加入50g稀硫酸中(杂质既不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为64.6g。试计算:
(1)生成氢气的体积。(精确到0.1L,在标准状况下氢气的密度为0.9g/L)
(2)锌粒中所含锌的质量分数(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
盐碱湖中捞出来的纯碱中含有一定量的食盐,为测定其中碳酸钠的含量,化学小组的同学将某纯碱样品24.6g放入烧杯中,逐滴加入150g稀盐酸,恰好完全反应,待不再产生气泡时,得到168g的食盐溶液.计算原混合物中碳酸钠的质量分数和反应后溶液的溶质质量分数(CO2的溶解忽略不计).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某硫酸厂废水中含有少量硫酸,为达标排放,技术员小张对废水中硫酸的含量进行检测.
(1)配制溶液: 欲配制溶质质量分数为4%的NaOH溶液100g,需要NaOH固体 g,水 ml(水的密度为1g/cm3);
(2)检测分析: 取废水样品98g,向其中逐滴加入NaOH溶液至恰好完全反应时,消耗4%的NaOH溶液20g。(假设废水中其它成分均不和NaOH反应;发生反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O); 试计算废水中硫酸的质量分数(写出计算过程).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
⑴一定条件下,下列物质在密闭容器内充分反应,反应前后各物质的质量如下:
| 物质 | A | B | C | D |
| 反应前的质量/g | 1.7 | 2.2 | 7.9 | 0.9 |
| 反应后的质量/g | 待测 | 6.6 | 0 | 2.7 |

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
小亮提出了“使带火星的木条复燃的氧气质量分数值是多少呢?”这个问题后,他对此展开探究,他先把一个集气瓶装满水后,倒出1/3体积的水后,用玻璃片盖上,倒置于水槽之中用排水法收集氧气,当气泡从瓶外冒出时,停止收集,正放于桌上,试计算,他收集的这瓶气体中氧气的体积数。(精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
氮化铝( AlN )被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应制得:Al2O3+N2+3C=2AlN+3CO,现欲制备8.2t氮化铝,试计算需要的氮气质量.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
我市庐江县小包庄去年发现一大型铁矿,主体为磁铁矿.冶炼磁铁矿的反应:4CO+Fe3O4 3Fe+4CO2.用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少?(答案保留一位小数)
3Fe+4CO2.用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少?(答案保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
已知金属钠能与水发生如下反应:2Na+2H2O═2NaOH+H2↑,若把4.6g金属钠投入到盛有足量水的烧杯中(如图),充分反应后烧杯中剩余溶液质量是40g,请计算:
(1)生成NaOH的质量.
(2)反应后所得NaOH溶液的溶质质量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com