
����Ŀ���±���NaCl��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ��ش����⡣
�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ��/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
��1�����������У��ܽ�����¶�Ӱ��仯�ϴ����______���ѧʽ����
��2��60��ʱ����ͼʾ������

A��������_______(����������������������)��Һ��C����Һ����������________g��
��3��50��ʱ�����������ʵı�����Һ��100g���ֱ��������10gˮ���ٻָ���50�棬ʣ����Һ��������NaCl��Һ________������������������������С������ KNO3��Һ��
��4���ɱ������ݿ�֪����KNO3��NaCl��T��ʱ������ͬ���ܽ��Xg����X��С��ȡֵ��Χ��____������ѧ����ʽ��ʾ,��ͬ����T��С��ȡֵ��Χ��______
���𰸡�KNO3 ��������Һ 167.6g ���� 36.0g <X<36.3g 20��<T<30��
��������
��1������NaCl��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȷ����ܽ�����¶�Ӱ��仯�ϴ����ʣ�
��2������60����20��ʱNaCl��KNO3���ܽ�ȵĺ�������жϻش�
��3��������50��ʱNaCl��KNO3�ܽ�ȵĺ�������жϣ�
��4������غ��Ȼ����ܽ����ͬ���¶ȼ����жϸö����ܽ�ȵ���ֵ�Ƿ������ȵĿ��ܣ�����غ��Ȼ�����ijһ�¶�ʱ������ͬ���ܽ��ʱ˵�����ܽ�ȴ���ͼ����ڽ��㣬����֪20��-30����һ���������Ǵ��ڽ��㡣
��1���ɱ��е����ݿ�֪�����������У��ܽ�����¶�Ӱ��仯�ϴ����KNO3��
��2���ɱ��е����ݿ�֪����60��ʱ��KNO3���ܽ����110g����A��Һ��100g��ˮ���ܽ���40g��KNO3���γɵ���ҺΪ��������Һ���ڽ��µ�20��ʱ��100g��ˮ�����ܽ�31.6g��KNO3��36g��NaCl�����γɵ���Һ������Ϊ167.6g��
��3���ɱ��е����߿�֪����50��ʱ��KNO3�ܽ�ȴ���NaCl���ܽ�ȣ�����50��ʱ�����������ʵı�����Һ��100g���ֱ��������10gˮ���ٻָ���50����KNO3�����ľ���࣬ʣ����Һ��������NaCl��Һ����KNO3��Һ��
��4������غ��Ȼ����ܽ����ͬ���¶ȼ����жϸö����ܽ�ȵ���ֵ�Ƿ������ȵĿ��ܣ�������֪��20��30��ʱ���������ʴ����ܽ����ͬ�Ŀ��ܣ�����غ��Ȼ�����ijһ�¶�ʱ������ͬ���ܽ��ʱ˵�����ܽ������ͼ����ڽ��㣬����֪20��~30����һ���������Ǵ��ڽ��㣮��ͬ���ܽ��x����36.0g~36.3g֮�䣬��36.0g <X<36.3g��20��<T<30����


 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д� ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���ͭCuCl��һ��������ˮ���Ҵ����ڳ�ʪ�������ױ��ʵ����ʣ��㷺Ӧ�����ν𡢵�ơ�ҽҩ����ҵ��CuC1���Ʊ��������£�
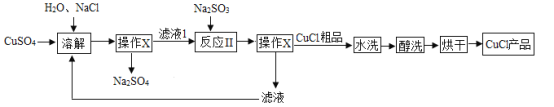
��1��Na2SO3����Ԫ�صĻ��ϼ�Ϊ_____��
��2��������X������Ҫ�õ�����������������_____��
��3������Һ���г���Na+��SO42���⣬�����ڽ϶��������_____��д���ӷ��ţ���
��4������Ӧ���з����Ļ�ѧ�仯��2CuCl2+Na2SO3��2CuCl��+2NaCl+SO3��������SO3����ˮ��������һ�ֳ������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ_____��
��5�����������п���ѭ�����õ����ʣ�ˮ���⣩��_____��д��ѧʽ����
��6�����á�ˮϴ����ԭ����_____������ϴ����Ŀ����_____����ֹϴ�ӹ������Ȼ���ͭ���ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѧУ�о���ѧϰС��Ϊ�˲ⶨ���ؿ�ɽʯ��ʯ��̼��Ƶ�����������ȡ����һЩ��ʯ��Ʒ����ȡϡ����200 g��ƽ���ֳ�4�ݽ���ʵ�飬������£�
ʵ�� | һ | �� | �� | �� |
������Ʒ������/g | 5 | 10 | 15 | 20 |
���ɵ�CO2����/g | 1.76 | 3.52 | 4.4 | m |
��1���ϱ���m����ֵ�� ��
��2����Ӧ�п�ʯ��ʣ���ǵ� ��ʵ�飻
��3������ʯ��ʯ����̼��Ƶ����������� ��
��4��ϡ���������ʵ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��CΪ���л�ѧ���������ʣ���������ͼת����ϵ��������������ȥ����
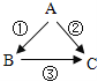
��1�����A��B���Ԫ����ͬ��B������ΪҺ�塣��CΪ_____��
��2�����AΪ��ɫ���壬BΪ�ж����塣��A��ѧʽΪ_____��B����;_____��
��3�����A��B��C���ǽ�����AԪ���ڵؿ��к����ŵ�����BΪ��ɫ����Ӧ�ٵ�������_____��A��B��C���ߵĽ������˳��Ӵ�С����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������Ϸ�չ��ϵʮ�����С�
��1�����������Խ�̿����������Ҫ�ɷ�������������������Ϊ��Ҫԭ����������Ӧ�������£�
��̿![]() CO2
CO2![]() CO
CO![]() Fe
Fe
��д������ 2 ��Ӧ�Ļ�ѧ����ʽ��_____��
��2��ÿ�������ϸ����IJ����ܸߣ���������ʴҲ����������˾����ʧ�����ڿ�������ʴ��ʵ���������������е�ˮ��_____��ͬ���õĽ����
��3��Ϊ�˷�ֹ������ʴ�����dz������������Ϳˢֲ���ͻ�������������ȸ��DZ���Ĥ�ķ�������Щ�������ܷ�ֹ��ʴ�Ĺ�ͬԭ����_____��
��4����ҵ������������ Al2O3 �� SiO2���������������ʣ���ȡ�������Ļ���������ͼ��ʾ��

��ͨ�������̿ɵó� SiO2 ��������_____������ţ���
A ������ˮ B ������ϡ���ᷴӦ C ��������������Һ��Ӧ
��������Ľṹ����ʯ���ƣ�������_____������ԭ���������������������ɵģ�������������_____������������������������������������������
������������������ϡ���ᷴӦ������������ˮ�Ļ�ѧ����ʽΪ_____��
��5�����Ͻ𱻹㷺Ӧ��������ɻ��������ȣ�������Ϊ���Ͻ����_____�������ᡢ��ʴ���� �ԡ����Ͻ���ϵĿ���ʴ������Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ά����C������������ƽʱ����Ϥ��ά���أ������dz��ֿ�ǻ�����ʱ���ܾ�������ȱ��������ġ���ʵ��ά����C������Զ��ֹ�����ǻ������������˯��֮ǰ�����IJ���һЩά����C���������ջ�����ô���ά����C�Ľṹ��ʽ��ͼ��ʾ�������й�����������ǣ�������
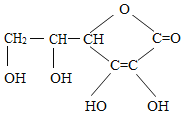
A. ά����C�Ļ�ѧʽΪ��C6H8O6
B. ά����C��һ�������к���20��ԭ�Ӻ�
C. ά���� C�����л��߷��ӻ�����
D. ά����C��̼���⡢������ԭ��������Ϊ9��1��12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ��ͼ���ش����⣺
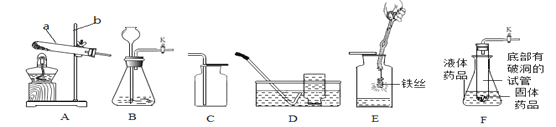
��1����ͼ������a ��������________������b��������________��
��2���ø��������ȡ�����Ļ�ѧ��Ӧ����ʽ��_______________��ѡ�õķ���װ����____������ţ���Ϊ��ֹ������ط�ĩ���뵼�ܣ���װ������һ��Ľ�����_____������Dװ���ռ����������۲쵽________ʱ����ɿ�ʼ�ռ���
��3��С��ͬѧ�ø��������ȡ�ռ���һƿ�������������������ƫ�ͣ�ԭ�������____
A ��������л����˶������� B �ռ�ǰ������ƿ��δע��ˮ
C �ռ�����ƿ����������ˮ D δ��������������ð��ʱ�Ϳ�ʼ�ռ�
��4������װ��B֤��SO2������ˮ����ƿ��װ��SO2���ӳ���©������ƿ��עˮ����ͼλ�ã��رջ���K��һ��ʱ���ɹ۲쵽��������___________________��������ĸ��
A ����©��������һ��ˮ�� B ����©���¶�������ð��
��5��ʵ������ȡ������̼ѡ�÷������ռ�װ�õ������_____������ţ�����Ӧ�Ļ�ѧ����ʽ��______________��ͼF��ijͬѧ���ñ����Թ���Ƶ��ƶ�����̼�ķ���װ�ã�����Ƴ��˷������õ��ŵ��⣬����дһ���ŵ�________���ҳ���������ͬ�ŵ��װ��______
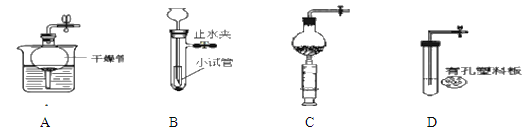
��6�����ռ����������ͼE��˿ȼ�յ�ʵ�飬����ƿ��Ԥ�ȷ�����ˮ��ԭ����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ����������ʵ��ܽ��������ͼ��ʾ���ش��������⣺
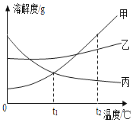
��1������������_____���ܽ�����¶ȱ仯�����������ܽ�ȵı仯���ƣ���������������������������
��2����t2��ʱ�ף��������ʱ�����Һ�ֱ�������������ˮ�����������������____�ң���������������������=����
��3�������л���������ʱ���ɲ���______�ķ����ᴿ��
��4����t2��ʱ�������ļס��ҡ����������ʵı�����Һͬʱ������t1�棬������Һ���ܼ�������С�����˳��Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���ʧȥ��ǩ��ϡ����Ũ�Ƚ��вⶨ��ȡϡ����50g���ձ��У���εμ�3.42%������������Һ���ձ�������������μ�����������Һ������ϵ����ͼ��ʾ�������������λС����
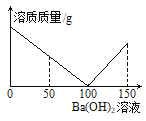
��1���μӷ�Ӧ��Ba(OH)2�������� g�����μ�Ba(OH)2��Һ50gʱ���ձ�����Һ��pH 7���������������������
��2�����������Һ����������������д��������̣��������0.01%����
��3������ͼ�л�����������������μ�Ba(OH)2��Һ��������ϵ��

��4���μ�Ba(OH)2��Һ��150gʱ��������Һ��������������Ϊ ���������0.01%����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com