
���� ��1�����������غ㶨�ɣ���Ӧ�����������ɵ�������������ڷ�Ӧǰ����Һ�����ļ��٣�
��2����Ʒ��NaOH����������������Ʒ��NaOH������������Ʒ�����������������ǿ��Ը�����һ����������������������������غ㶨�ɣ������Ʒ��Na2CO3������������������Ʒ��Na2CO3������������
��� �⣺��1�����������غ㶨�ɣ���Ӧǰ����Һ�����ļ��پ͵��ڷ�Ӧ�����������ɵ���������������Է�Ӧ������CO2������Ϊ200g+200g-395.6g=4.4g��
�ʴ�Ϊ��4.4
��2���⣺����ȡ��Ʒ�к���Na2CO3������Ϊx��
Na2CO3+H2SO4�TNa2SO4+H2O+CO2��
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$��
��֮�ã�x=10.6g
���ռ���Ʒ��Na2CO3����������=$\frac{10.6g}{50.0g}��100%=21.2%$
���ռ���Ʒ��Na2CO3����������Ϊ21.2%��
���� ������Ҫ���ڼ�Ļ�ѧ���ʵĻ����Ͽ����й������غ㶨�ɵ��й�֪ʶ���Լ�����������������ļ������⣬ע��ѧ���ۺ����������������п��Ŀ���֮һ��


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ | B�� | ֹ���ǽ� | ||
| C�� | ��ѹ�����е�Һ�� | D�� | ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 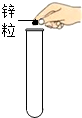 ȡ�ù��� | B�� |  ����NaOH���� ����NaOH���� | C�� | 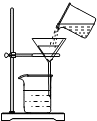 ���� | D�� | 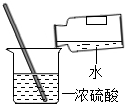 ϡ��Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ���Ҽ��ȸ������������ | |
| B�� | ��ҵ�Ϸ������������ | |
| C�� | ʵ������ϡ�����ʯ��ʯ�ƶ�����̼ | |
| D�� | ��ҵ������ʯ��ʯ�ƶ�����̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
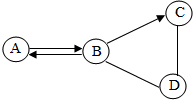 A��B��C��DΪ���л�ѧ�������������ʣ�����֮������ͼ16��ʾ��ת���ͷ�Ӧ��ϵ����������ʾijһ�����ʿ�ת��Ϊ��һ�����ʣ���-����ʾ�����������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ��
A��B��C��DΪ���л�ѧ�������������ʣ�����֮������ͼ16��ʾ��ת���ͷ�Ӧ��ϵ����������ʾijһ�����ʿ�ת��Ϊ��һ�����ʣ���-����ʾ�����������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Zn | B�� | Zn��OH��2 | C�� | ZnO | D�� | ZnCO3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com