
【题目】稀硫酸与氢氧化钠溶液混合没有明显现象,为证明硫酸与氢氧化钠发生了化学反应,小颖同学进行了如下探究:

(1)小颖同学通过图一所示的实验,证明硫酸与氢氧化钠发生了化学反应,她依据的实验现象是 。
(2)氢氧化钠是实验室常用药品,下列相关说法中,正确的是 (填序号)。
A.称量:可将NaOH固体直接放在天平左边托盘的纸上进行称量
B.溶解:NaOH固体溶于水时放出大量热,溶解时需用玻璃棒不断搅拌
C.应急:先用大量水冲洗皮肤上的NaOH溶液,再涂上3%~5%稀盐酸溶液
D.保存:NaOH固体易吸收空气中的水蒸气和CO2,应密封保存
(3)溶液的pH与加入稀硫酸的质量关系如图二所示,图中A点对应溶液中的溶质有 (写化学式)
(4)根据图示信息,当溶液恰好为中性时,求所得不饱和溶液中溶质的质量。(不计滴加的酚酞试液质量,计算精确到0.01g)
【答案】(1)溶液由红色变为无色(2) BD (3)NaOH、Na2SO4 (4)2.84g
【解析】
试题分析:(1)氢氧化钠显碱性,能使酚酞试液变为红色,盐酸与氢氧化钠反应生成氯化钠和水,氯化钠显中性,不能使酚酞试液变红,所以溶液由红色变为无色
(2)NaOH固体是种具有腐蚀性的药品,不能直接放在天平左边托盘的纸上进行称量,A错误;NaOH固体溶于水时放出大量热,溶解时需用玻璃棒不断搅拌,B正确;先用大量水冲洗皮肤上的NaOH溶液,再涂上3%~5%稀硼酸溶液,C错误;NaOH固体易吸收空气中的水蒸气和CO2,应密封保存,D正确。
(3)A点处于碱剩余,故溶液中的溶质有NaOH、Na2SO4
(4)解:H2SO4质量 = 20g × 9.8% = 1.96 g
设Na2SO4质量为x,则
H2SO4+2NaOH=Na2SO4 + 2H2O
98 142
1.96g x
98/142 =19.6g/x ,
得 x = 2.84g


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:初中化学 来源: 题型:
【题目】兴趣小组在研究溶液的酸碱性时发现,Mg与NH4Cl溶液(酸性)反应有气泡产生。为确定气体的成分,进行下列实验探究:
【提出猜想】气体可能是HCl,NH3,H2中的一种或几种。
【查阅资料】NH3和HCl常温下会生成NH4Cl固体;NH3、HCl极易溶于水。
【实验探究】
为确定是否含有HCl,将气体通入含有硝酸的硝酸银溶液中,观察到_________,说明该气体中无HCl。
为了探究NH3和H2是否存在,又设计如下实验装置(假设每步反应均完全):
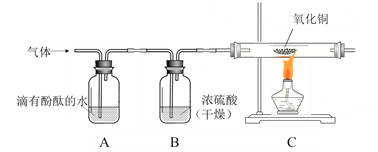
Ⅰ. A中观察到_________,证明有NH3;
Ⅱ. B中玻璃管内观察到__________,证明有H2;
【实验结论】Mg与NH4Cl溶液反应产生的气体是NH3和H2。
【实验反思】综合以上信息和实验结论,有同学认为无需单独检验HCl,就能证明HCl不存在。请评价这种说法是否合理并阐述理由_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属镁是一种重要的金属。小明在做镁带燃烧实验时,发现从实验室中取出来的镁条表面呈灰黑色,这灰黑色物质是什么呢?是氧化镁吗?小明想了一下,很快就把它否定了,他的理由是 。小明通过查阅资料灰黑色固体为碱式碳酸镁。
【查阅资料】1.碱式碳酸镁有多种组成。如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、等,可以表示为xMgCO3·yMg(OH)2(x、y都是正整数)。
2.MgCO3![]() MgO +CO2 ↑ ;Mg(OH)2
MgO +CO2 ↑ ;Mg(OH)2![]() MgO +H2O
MgO +H2O
3.碱式碳酸镁能与盐酸反应生成氯化镁、二氧化碳和水。
Ⅰ.确定镁带表面碱式碳酸镁的成分
小明同学为确定镁带表面碱式碳酸镁的组成,设计如图所示的实验:
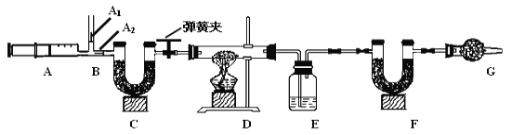
图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
【实验步骤】
①按图组装好仪器后, ;
②称取灰黑色样品,并将其放入硬质玻璃管中;
③打开弹簧夹,反复推拉注射器;
④称量E、F的质量,E的质量为87.6g,U型管F的质量为74.7g;
⑤关闭弹簧夹,加热D处试管直到反应不再进行;
⑥打开弹簧夹,再次反复缓缓推拉注射器;
⑦再次称量E、F的质量,E的质量为89.4g,U型管F的质量为87.9g。
【问题讨论】
(1)补充好实验步骤 ,E中所装药品是 ;
(2)C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是 ,若没有G装置,则测定的x的值会 (填“偏大”、“偏小”、“无影响”);
(3)步骤⑥目的是 ;
(4)根据上述实验数据,推算该碱式碳酸镁的化学式为 。
Ⅱ.测定镁带样品纯度

【问题讨论】
(5)装置B的作用是 ,装置C的作用是 ;
(6)称取1.0g镁带样品与足量浓盐酸充分反应后,收集到的氢气的体积为0.448 L(已知该实验条件下氢气的密度为0.089g/L),计算镁带样品纯度(写出计算过程,2分)
(7)有同学认为用这种方法测定的结果一定偏大,原因是 ;
(8)小江同学认为测定产物中CO2的质量(即反应前后装置②的质量差)也可测定样品中单质镁的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果偏低,你认为原因可能是 。(填序号)
①浓盐酸易挥发,产生的氯化氢气体被装置
②二氧化碳气体逸出时带出的水蒸气在装置B中冷凝而被吸收
③装置A、B内空气中的二氧化碳被装置B吸收
④实验结束时烧瓶中残留二氧化碳
⑤气体从氢氧化钠溶液中逸出时带走部分水蒸气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学。利用图中仪器和装置回答下列问题。

(1)配制一定质量分数的NaCl溶液,除需要量筒外,还需上述玻璃仪器中的_____ (填序号)。
(2)实验室制取的CO2中常混有HCl气体,为除去CO2中少量的HCl气体,不纯的气体应从E装置____________管口进入;实验室收集二氧化碳时,可选用的收集装置是____________ (填字母代号)
(3)SO2和Cl2均有毒有害,实验室可将两者同时通入水中,生成两种酸,发生的反应为:SO2+Cl2+2H2O═(酸)+2HCl,其中另一种酸的化学式是______;向吸收液中投入锌粉会见到大量气泡,此时发生的反应属于___________反应(填写基本反应类型)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国南海蕴藏着极为丰富的资源,在经济、国防上有重要意义。南海诸岛自古以来就是我国领土,我们要坚决捍卫在南海的主权。
(1)我们的食用盐大部分来自于海水,从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,可以将粗盐溶于水,然后进行如下操作:
① 过滤
② 加过量的Na2CO3溶液
③ 适量的盐酸
④ 加过量的Ba(OH)2溶液
⑤ 蒸发。
正确的操作顺序是 (填序号)。
(2)烧碱和氯气是重要的化工生产原料,我们可以利用海水为原材料大量制取。发生反应的化学方程式为:2NaCl + 2 A![]() 2 NaOH+ Cl2↑+H2↑, 则 A的化学式为 。
2 NaOH+ Cl2↑+H2↑, 则 A的化学式为 。
(3)如图是氯化钠、氢氧化钠两种固体物质的溶解度曲线。

① t1℃ 时,NaOH饱和溶液的溶质质量分数 NaCl饱和溶液的溶质质量分数(填“大于”、“小于”、“等于”之一)
② t2℃ 时,将 20gNaCl固体投入 50g水中,充分溶解后可得到NaCl的 (填“不饱和溶液”或“饱和溶液”之一),此时所得溶液的质量是 g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有关2CuO+C![]() 2Cu+CO2↑的反应,说法正确的是( )
2Cu+CO2↑的反应,说法正确的是( )
A.CuO具有还原性
B.C发生了还原反应
C.反应前后氧元素的化合价没有改变
D.反应前后固体质量不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在“宏观﹣微观﹣符号”之间建立联系,是学习化学的一种重要思维方式.如图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列问题.
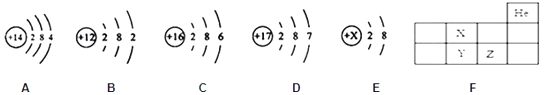
(1)如图A、B、C、D元素中,属于金属元素的是________(填元素符号);
(2)由B元素和D元素组成的化合物的化学式为_______;
(3)E粒子带2个单位负电荷,则X =_______,离子的符号为_______;
(4)F为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是______。
A.原子序数Z >Y B.核外电子数:X=Y
C.Y和Z处于同一族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com