
【题目】实验室制取气体时需要的一些装置如图所示,请回答下列问题。
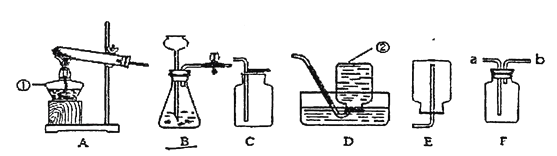
(1)实验室用氯酸钾和二氧化锰制取并收集较为纯净的氧气最好选用的装置为_____________________________(填字母标号,下同),该反应的化学方程式为_____________________________;
(2)若用F装置用排空气法收集氧气,气体从_____ (填 “a”或“b”)进入F中,且如何验证氧气已经收集满?_____________________________;
(3)实验室制取二氧化碳发生装置为______________________________;该反应的化学方程式为______________________________;检查该装置气密性的方法是_____________________________。
(4)现有10g黄铜(铜锌合金)样品,向其中加入100g一定浓度 的稀硫酸恰好完全反应,反应后称得烧杯中物质的质量109.8g,则原黄铜样品中铜的质量分数是_________________________。
【答案】AD  a 将一根带火星的木条放在b端,若木条复燃,证明氧气已满 B CaCO3+2HCl=CaCl2+CO2↑+H2O 用弹簧夹封闭右侧导管,向长颈漏斗中加水,长颈漏斗颈部形成稳定的水柱,装置气密性良好 35%
a 将一根带火星的木条放在b端,若木条复燃,证明氧气已满 B CaCO3+2HCl=CaCl2+CO2↑+H2O 用弹簧夹封闭右侧导管,向长颈漏斗中加水,长颈漏斗颈部形成稳定的水柱,装置气密性良好 35%
【解析】
(1)实验室用氯酸钾和二氧化锰制取氧气,属于固、固加热型,适合用装置A作发生装置;因为氧气不易溶于水,要收集较纯净的氧气,可用装置D收集;氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,反应的化学方程式为: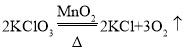 ;
;
(2)氧气的密度比空气大,所以用装置F收集氧气时,氧气从长管进入,即a端进入,b端出,将一根带火星的木条放在b端,若木条复燃,证明氧气已满;
(3)实验室制取二氧化碳是用大理石和稀盐酸反应生成二氧化碳,常温即可反应,发生装置可选B,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;检查装置B气密性的方法:用弹簧夹封闭右侧导管,向长颈漏斗中加水,长颈漏斗颈部形成稳定的水柱,装置气密性良好;
(4)反应恰好进行,根据质量守恒定律,产生氢气的质量=10g+100g-109.8g=0.2g;
设反应消耗锌的质量为x;
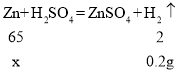
![]()
解得:x=6.5g;
该铜锌合金中铜的质量为:10g-6.5g=3.5g,
则该铜锌合金中铜的质量分数为:![]() ×100%=35%。
×100%=35%。
答:该铜锌合金中铜的质量分数为35%。


科目:初中化学 来源: 题型:
【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化作用呢?于是进行了以下探究。
(猜想)Ⅰ.CuO不是催化剂,也不参加反应,反应前后质量和化学性质不变;
Ⅱ. CuO参与反应生成O2,反应前后质量和化学性质发生改变;
Ⅲ. CuO是反应的催化剂,反应前后_________________。
(实验及结论)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
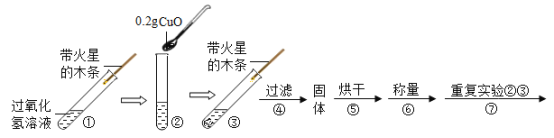
(1)填写下表:
步骤③现象 | 步骤⑥ | 步骤⑦现象 | 结论 |
溶液中有气泡冒出,带火星木条复燃 | 称量所得固体质量为 ____________g | 溶液中有气泡冒出,_____________ | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立。 |
(表达与交流)过氧化氢被CuO催化分解放出氧气的化学反应方程式为_____________。
(反思与拓展)
(1)甲同学为研究催化剂种类对催化效果的影响,用等量的两份过氧化氢溶液设计了以下实验,大家认为该方案不可行,其原因是_________。
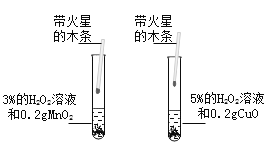
(2)以下有关催化剂的说法正确的是_____________(填序号)。
①二氧化锰是催化剂
②某些化学反应可以有多个催化剂
③一种物质可能作为多个反应的催化剂
④所有化学反应都需要催化剂
⑤催化剂只能加快化学反应速率
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某同学进行电解水实验的装置图,据此回答:
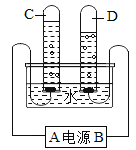
(1)图中B端为电源的 _____ (填“正”或“负”)极.
(2)D试管中收集到的气体是_____,检验该气体用_____,则此检验中的化学反应符号表达式为_____,属于_____反应(填基本反应类型).
(3)上述实验可以得出:在化学变化中,_____可分.
(4)在水的电解实验中,没有发生改变的微粒是_____(填符号).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是汽车“尾气催化转换器”将尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子。下列说法错误的是
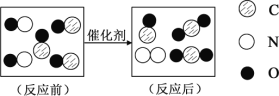
A. 此反应中有单质生成
B. 原子在化学变化中是不可分的
C. ![]() 极易与人体血液中的血红蛋白结合
极易与人体血液中的血红蛋白结合
D. 参加反应的 ![]() 与
与 ![]() 个数比为 2:3
个数比为 2:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用15g石灰石样品,把160g稀盐酸平均分4次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后实验数据如下,请计算:
实验次数 | 1 | 2 | 3 | 4 |
稀盐酸的累计加入量/g | 40.0 | 80.0 | 120.0 | 160.0 |
产生CO2的总质量/g | 2.2 | m | 5.5 | 5.5 |
(1)m=_____;
(2)15g大理石样品与稀盐酸反应最多产生二氧化碳的质量是_____g;
(3)15g石灰石样品与盐酸恰好完全反应时,消耗的盐酸质量为_____g;
(4)在下图中画出生成气体的质量与加入稀盐酸的质量的关系_____。
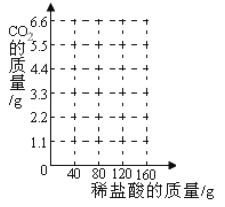
(5)石灰石样品中碳酸钙的质量分数是多少?_____(写出计算过程,结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是最重要的自然资源,也是生命之源。
(1)为了人类和社会经济的可持续发展,我们必须爱护水资源,节约用水是每个公民的责任和义务,下列做法属于节约用水的是_____(选填序号)
A 城市生活废水直接排入河流
B 农业上合理使用化肥和农药
C 工业上冷却水循环使用
D 用水后关闭水龙头
(2)将含有泥沙的的河水变得澄清用_____的方法;实验室用_____的方法获得纯水。
(3)自来水厂净化水的主要步骤如图所示,有关说法错误的是_____。
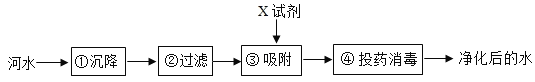
A 步骤①②可以除去难溶性杂质
B X试剂可以是活性炭
C 步骤④可用硫酸铜杀菌、消毒
D 步骤①中可加入明矾作絮凝剂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
很多人畏甲醛如虎、谈甲醛色变,甚至希望生活在“零甲醛”的世界里,你真的了解甲醛吗?甲醛常温下易溶于水,其水溶液具有防腐杀菌功能,35% ~ 40%的甲醛水溶液俗称福尔马林,可用来浸制生物标本,给种子消毒等,但不能用于保鲜虾仁、鱿鱼等食品。在纺织品加工过程中,向助剂中添加甲醛,能防皱、防缩、防褪色等,但穿着或使用时会释放甲醛。《国家纺织产 品基本安全技术规范》(GB 18401-2010)规定纺织品甲醛最大残留量如下表:
项目 | A类 | B类 | C类 |
甲醛含量(mg/kg) | 20 | 75 | 300 |
甲醛可用于生产脲醛树脂、酚醛树脂、三聚氰胺-甲醛树脂等胶黏剂。这些胶黏剂生产工艺简单、性能良好、价格低廉,广泛应用于装修材料,但会缓慢释放出甲醛。我国室内空气质量标准(GB/T 18883-2002)规定,甲醛1小时均值浓度不得超过0. 10 mg/m3。下图是3个房子在7个时间点测定的甲醛均值浓度。
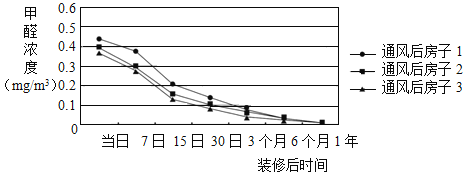
甲醛还能用于合成有机材料,这些材料性能优良,在工业机械、汽车制造、电子电器、日常用品等领域有广泛应用。现在你对甲醛一定有了新的认识!
依据文章内容回答下列问题。
(1)甲醛的物理性质有________________ (写出一条即可)。
(2)按照国家标准,B类衣服中甲醛的含量不得超过____________mg/kg。
(3)装修后的房子通风6个月,甲醛含量___________ (填“符合”或“不符合”)国家标准。
(4)下列说法正确的是____________ (填序号) 。
A通风换气可降低室内甲醛含量
B甲醛是防腐剂,但不能用于食品保鲜
C甲醛有百害而无一利,应禁用甲醛
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学发现,除二氧化锰外其他物质也能作氯酸钾分解的催化剂,那么氧化铜是否能作氯酸钾分解的催化剂?于是进行了如下的探究。
提出问题:氧化铜是否能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
设计实验:同学们设计了下面三组实验,实验中“待测数据”是生成相同体积的氧气所需时间(其它可能影响实验的因素均忽略)。
实验编号 | 氯酸钾 | 其它物质质量 | 待测数据 |
① | 1.2g | / | |
② | 1.2g | 二氧化锰0.5g | |
③ | xg | 氧化铜0.5g |
问题讨论:
(1)实验②中反应的文字表达式是_____,实验③中x的数值为_____。
(2)由实验③与实验_____的“待测数据”相对比,若实验③“待测数据”更_____(填“大”或“小”),则说明氧化铜能加快氯酸钾的分解速率。
反思提升:
(1)若要证明氧化铜是该反应的催化剂,还要设计实验验证它在化学反应前后的_____和_____不变。
(2)你认为同学们设计实验②和实验③的对比的目的是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com