
【题目】硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为: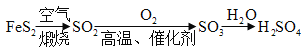
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是 。
②在实验室中不慎将浓硫酸沾到皮肤上的处理方法是
A 立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液
B 立即用稀氢氧化钠溶液冲洗,然后再用水冲洗
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,反应为:H2SO4+ Ba(OH)2=BaSO4↓+2H2O,沉淀不再产生时(此时恰好完全反应),求反应中Ba(OH)2的质量。
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:初中化学 来源: 题型:
【题目】请用合适的化学用语填空:
(1)3个氯原子_____。
(2)铵根离子_________。
(3)2个甲烷分子_______。
(4)标出硝酸镁中镁元素的化合价_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究中和反应是否发生的方法有多种。小华同学进行了以下四个实验,并用图像分别描述了实验过程中的现象。其中,依据图示现象不能判断中和反应一定发生的是()
A.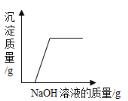 在稀盐酸中加入氯化铜,然后向其中逐滴加入NaOH溶液
在稀盐酸中加入氯化铜,然后向其中逐滴加入NaOH溶液
B.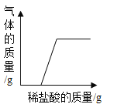 在NaOH溶液中加入CaCO3,然后向其中逐滴加入稀盐酸
在NaOH溶液中加入CaCO3,然后向其中逐滴加入稀盐酸
C.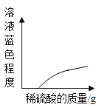 在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸
在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸
D.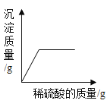 在NaOH溶液中加入Ba(NO3)2,然后向其中逐滴加入稀硫酸
在NaOH溶液中加入Ba(NO3)2,然后向其中逐滴加入稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上利用生产钛白的副产品硫酸亚铁制备还原铁粉的流程如图
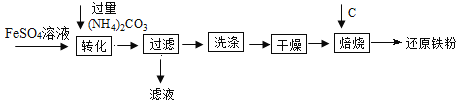
下列说法不正确的是
A.“转化”时在溶液中生成了FeCO3沉淀,该反应的基本反应类型是复分解反应
B.“过滤”后得到的滤液中的溶质只有(NH4)2SO4
C.“干燥”过程中有少量的FeCO3转化为FeOOH和CO2,此时与FeCO3反应的物质有O2和H2O
D.取14.06g还原铁粉(仅含有Fe和少量FexC)在氧气流中充分加热,得到0.22gCO2,另取相同质量的还原铁粉与足量稀硫酸充分反应(FexC与稀硫酸不反应),得到0.48gH2,则FexC的化学式是Fe2C
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】周末的生活,丰富多彩。
晨练时,我们一家人去打了一场篮球。我知道涤纶运动衣、橡胶制的篮球和盛装用品的塑料筐都由______________________________材料制成。
上午,我在家看书。了解到1869年,俄国化学家门捷列夫(1834-1907)发现并编制了元素周期表,从此人们对化学的学习和研究有规律可循。在元素周期表与原子结构的关系中,原子序数=_________。
下午,爸爸妈妈带我去参观了制碱厂。制碱厂应用的是“侯氏联合制碱法”,其原理是我国化学工业的先驱侯德榜(1890-1974)创造的:X+NH3+CO2+H2O=NaHCO3↓+NH4Cl 2NaHCO3![]() Na2CO3+H2O+CO2↑,我知道了制碱厂的原料之一“X”是________,产品“碱”是Na2CO3。
Na2CO3+H2O+CO2↑,我知道了制碱厂的原料之一“X”是________,产品“碱”是Na2CO3。
晚上,电视节目中有这样一段情节:科考人员野外考察时要经过一小段沼泽地,为顺利通过,有人提议向沼泽地上铺一层生石灰,沼泽地将会变硬,人们能顺利通过,同时铺撒和通过时应小心“烫伤”。这是真的吗?我要继续看下去。我知道这一过程中的两个化学方程式是(写一个即可)_____________,并且能从化学角度说明“烫伤”的原因是_____ 。
学习了化学,我会用化学的眼光看生活,看世界!
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为氢氧化钙的溶解度曲线,下列说法不正确的是( )

A.氢氧化钙的溶解度随温度的升高而减小
B.30℃时,100g水中最多溶解0.15g氢氧化钙
C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数变小
D.70℃时,饱和石灰水中溶质和溶液的质量比为0.1:100
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.非金属元素原子的最外层电子数都多于 4 个
B.参加反应的各物质质量总和等于反应后的各物质的质量总和
C.若等质量的铁、镁和铝三种金属,分别与足量的等溶质质量分数的稀盐酸充分反应后,生成氢气质量的大小依次为 x、y 和 z,则 z>y>x
D.从粒子角度看,稀硫酸和浓硫酸的共同点是它们都含有氢离子和硫酸根离子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合下列实验装置图,回答有关问题:
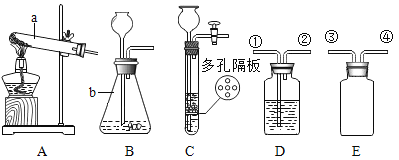
(1)仪器b的名称为_______。
(2)实验室用高锰酸钾制取氧气应选择的发生装置是_______(填字母),该反应的化学方程式为______。
(3)对于实验室制取气体,小虹总结了如下规律,你认为正确的是________。
a反应必须加热.
b反应物必须是纯净物
c生成物中只有一种气体
(4)实验室常用装置C代替B制取气体,装置C的优点是________。
(5)实验室用B制取气体,欲验证制得的气体为二氧化碳,应在装置D中盛放_______试剂(填试剂名称),并把气体从________端通人,该装置中发生的化学反应的方程式为_________。
(6)用E收集二氧化碳,从③端通人,请把装置图补画齐全。(请将补充完整的E装置图画在答题卡.上相应的位置)________
查看答案和解析>>
科目:初中化学 来源: 题型:
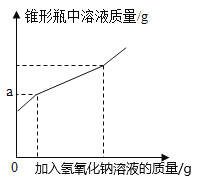
【题目】现有盐酸和铁锈反应后的溶液,为测定溶液中氯化铁的含量,某化学活动小组称取样品溶液50g放入锥形瓶中,再向锥形瓶中滴加氢氧化钠溶液,反应过程中产生沉淀质量的部分实验数据和锥形瓶中溶液质量变化的图象如表所示:
加入氢氧化钠溶液的质量/g | 70 | 90 | 120 | 140 |
产生沉淀的质量/g | 2.14 | 3.21 | 4.28 | m |
(1)表中m的值是 ;
(2)50克样品中氯化铁的质量分数是 ;
(3)求该实验中所用氢氧化钠溶液的溶质质量分数。(写出计算过程)
(4)如图图象中a的数值是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com