
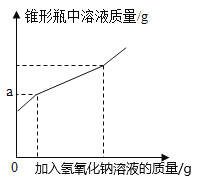
【题目】现有盐酸和铁锈反应后的溶液,为测定溶液中氯化铁的含量,某化学活动小组称取样品溶液50g放入锥形瓶中,再向锥形瓶中滴加氢氧化钠溶液,反应过程中产生沉淀质量的部分实验数据和锥形瓶中溶液质量变化的图象如表所示:
加入氢氧化钠溶液的质量/g | 70 | 90 | 120 | 140 |
产生沉淀的质量/g | 2.14 | 3.21 | 4.28 | m |
(1)表中m的值是 ;
(2)50克样品中氯化铁的质量分数是 ;
(3)求该实验中所用氢氧化钠溶液的溶质质量分数。(写出计算过程)
(4)如图图象中a的数值是 。
【答案】(1)4.28(2)13%(详见解析)(3)6%(4)80
【解析】
氯化铁和氢氧化钠反应生成氢氧化铁沉淀和氯化钠,化学方程式为:![]() 。
。
(1)根据表中数据分析,加入70g氢氧化钠溶液时,产生2.14g沉淀,加入90g氢氧化钠溶液时,产生3.21g沉淀,说明加入20g氢氧化钠溶液,就能产生1.07g沉淀,那么加入120g氢氧化钠溶液时,又多加了30g氢氧化钠溶液,如果完全反应,可以产生1.605g沉淀,则沉淀总质量为1.605g+3.21g=4.815g,但实际上总沉淀的质量是4.28g,说明氯化铁已经反应完全,再加入氢氧化钠溶液不会产生沉淀,所以m=4.28;
(2)根据(1)可知,最终生成的氢氧化铁沉淀是4.28g,设氯化铁的质量为x。
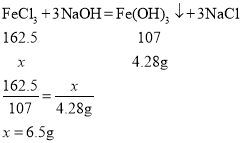
则50克样品中氯化铁的质量分数![]() ;
;
(3)根据(1)可知,每加入20g氢氧化钠溶液,就能产生1.07g氢氧化铁沉淀,设20g氢氧化钠溶液中的溶质质量为y。
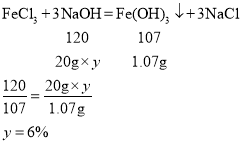
则氢氧化钠溶液的溶质质量分数为6%;
(4)根据图像分析,当刚开始加入氢氧化钠溶液时,氢氧化钠先和溶液中的盐酸反应生成氯化钠和水,此过程增加的质量就是氢氧化钠溶液的质量,反应完全后,氢氧化钠继续和氯化铁反应生成氢氧化铁沉淀和氯化钠。根据(1)可知,加入20g氢氧化钠溶液,就能产生1.07g氢氧化铁沉淀,所以当加入70g氢氧化钠溶液时,产生的沉淀是2.14g,则产生沉淀消耗的氢氧化钠溶液质量为40g,那么与盐酸反应的氢氧化钠溶液的质量=70g-40g=30g,所以由起始到a点溶液增加的质量是30g,溶液起始质量为50g,则a=80。


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:
【题目】硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为: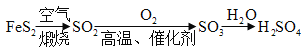
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是 。
②在实验室中不慎将浓硫酸沾到皮肤上的处理方法是
A 立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液
B 立即用稀氢氧化钠溶液冲洗,然后再用水冲洗
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,反应为:H2SO4+ Ba(OH)2=BaSO4↓+2H2O,沉淀不再产生时(此时恰好完全反应),求反应中Ba(OH)2的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某干燥剂含有CaO、NaOH和CaCl2中的两种物质,为探究其成分,设计如图所示实验。依据实验流程回答相关问题。
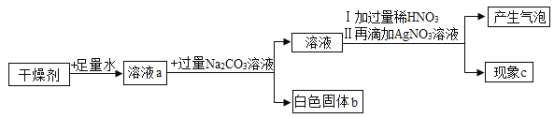
(1)向溶液a中加入紫色石蕊试液,现象是__________________。
(2)白色固体b一定是_______________(填化学式)。
(3)加入过量稀HNO3的目的是_______________。
(4)现象c:①若无白色沉淀,干燥剂成分为_______________。
②若有白色沉淀,写出产生此现象的化学方程式_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是
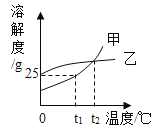
A.t1℃时,25g甲充分溶解于100g水中,可得甲的饱和溶液125g
B.t2℃时,甲、乙的溶液的溶质质量分数相等
C.若甲中含有少量乙,可用降温结晶的方法提纯甲
D.将t2℃时的甲的饱和溶液降温到t1℃,可析出晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属和塑料在生产和生活中应用广泛,如2019年1月,嫦娥四号和玉兔二号互拍成像,实现了探月工程五战五捷,嫦娥四号上使用了大量的金属和塑料。
(1)嫦娥四号使用了大量复合材料,下列关于复合材料的说法中正确的是________。
A不锈钢是常见的复合材料
B多种材料混在一起就是复合材料
C复合材料集中了组成材料的优点
(2)航天器的天线用钛合金制成。工业上通常是在高温下用四氯化钛(TiCl) 与金属镁发生置换反应获得金属钛,该反应的化学方程式为_________。
(3)铁制品广泛应用于生产、生活中。下列属于铁合金的是_________(选填字母)。
A Fe(OH)2 B生铁 C不锈钢
(4)为减少污染要对废弃的塑料制品回收,例如回收的保鲜膜经过焚烧后会生成CO2,生成的CO2可用来生产化工产品乙酸(CH3COOH),转化的微观过程如图所示。
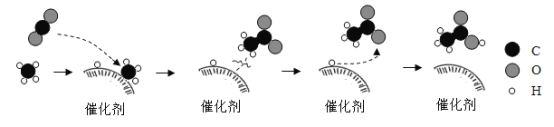
该反应过程中,反应物CO2,与产物CH3COOH的分子个数比为_______,反应的化学方程式为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化,如图所示。
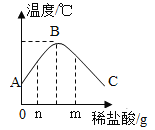
(1)由图可知,稀盐酸与氢氧化钠溶液发生的反应是________________(填“放热”或“吸热”)反应。
(2)从A到B过程中,烧杯中溶液的pH逐渐______ (填 “增大”或“减小”),B点表示的含义是_________。
(3)加入ng稀盐酸时,溶液中溶质有_______,加入盐酸到mg时pH_________(填“大于”“小于”或“等于”) 7.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】火柴这种曾经的生活必需品,已经渐渐地淡出了人们的视线。火柴又称“洋火”,包括火柴头,火柴杆和火柴盒三部分。其中火柴头是由氯酸钾 KClO3,二氧化锰 MnO2,三硫化二 锑Sb2S3和硫S组成的。下列说法正确的是 ( )

A.氯酸钾的相对分子质量是 122.5g
B.二氧化锰分子中含有一个锰原子和两个氧原子
C.三硫化二锑是由锑元素和硫元素组成的
D.二氧化锰中锰元素的化合价为+2价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学,现有下列仪器:
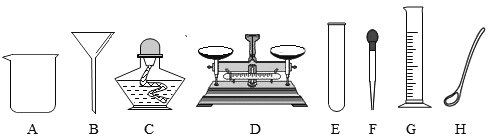
(1)大量试剂的反应容器要用____;量取7.2mL溶液用_____、_____。若小红同学量取7.2mL某液体时,如果俯视量筒的刻度(其他操作无误),所量取液体的体积_____(填“大于”或“小于”或“等于”)7.2mL。
(2)给物质加热要用到_____,加热时要用_____。可以直接加热的仪器是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究化学反应规律是化学科学的核心任务。根据下列微观示意图回答问题。
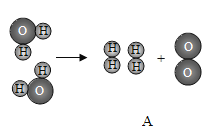
(1)图 A 表示的是电解水反应的微观示意图。写出反应的化学方程式______________;在该反应中水分子、氢分子、氧分子的个数比为________________。
(2)物质之所以发生化学反应,从微观的角度看,是因为反应物的微粒之间在一定条件下发生有效的相互作用,使微粒的结构发生改变,或微粒重新排列组合。
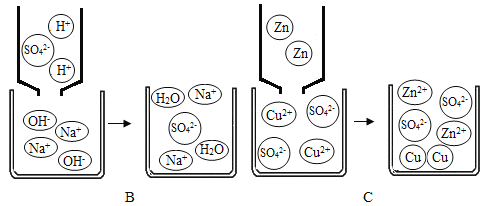
①从微粒的角度说明图 B 反应的实质是___________。
②图 C 所示反应中,发生有效的相互作用而促使反应发生的微粒是_____________(写出微粒的符号)。
(3)在点燃条件下,A 和 B 反应生成 C 和 D。反应前后分子变化的微观示意图如下所示。
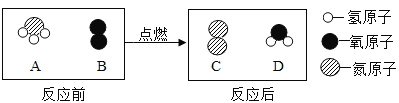
下列说法正确的是___________(填数字序号)。
①该反应类型为复分解反应
② 4 种物质中属于氧化物的是 D
③反应前后,元素化合价均未发生变化
④若 48 gB 完全反应,则生成 C 的质量为 28 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com