
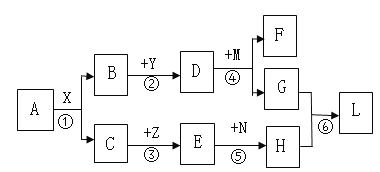
【题目】图中所涉及到的物质均为常见的化合物,图中“—”表示相互反应,“→”表示转化关系,部分反应物、生成物、反应条件已略去。其中A、B常温下均为液态,且组成元素相同,F是大理石的主要成分,Y为氧化物,Z是紫红色固体,L为蓝色絮状沉淀。回答下列问题:
(1)写出A物质的化学式___________。
(2)反应①—⑥涉及的基本反应类型有__________种。
(3)写出反应④的化学方程式__________________________________。
(4)写出N物质的一种用途_______________________________________。
【答案】H2O2 3 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 除锈
【解析】
A、B常温下均为液态,且组成元素相同,A与X反应后生成B与C,所以A为过氧化氢,B为水,C为氧气。X为二氧化锰;Z是紫红色固体,则Z为铜,E为氧化铜;F是大理石的主要成分,所以F是碳酸钙;Y为氧化物,能与B(水)反应生成D,D与M反应生成碳酸钙,所以Y为氧化钙,D为氢氧化钙,则M为碳酸钠,G为氢氧化钠;L为蓝色絮状沉淀,则L为氢氧化铜沉淀;G(氢氧化钠)与H反应生成氢氧化铜沉淀,则H为硫酸铜,N为硫酸。
(1)由分析可知,A为过氧化氢,其化学式为H2O2,故填H2O2。
(2)反应①是过氧化氢反解生成水和氧气,属于分解反应,反应②是氧化钙与水反应生成氢氧化钙,属于化合反应,反应③是铜和氧气反应生成氧化铜,属于化合反应,反应④是氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,属于复分解反应,反应⑤是氧化铜与硫酸反应生成硫酸铜和水,属于复分解反应,反应⑥是氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,属于复分解反应,涉及的基本反应类型有分解反应、化合反应和复分解反应,共3种,故填3。
(3)反应④是氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故反应的化学方程式写为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。
(4)N为硫酸,能与金属氧化物反应生成盐和水,所以N可以用来除锈,故填除锈。


科目:初中化学 来源: 题型:
【题目】取硫酸钠和氯化钠的混合物15g,加入180g水使其完全溶解,再加入100g氯化钡溶液恰好完全反应,过滤,得271.7滤液(不考虑实验过程中质量的损失)。
计算:
(1)该混合物中硫酸钠的质量分数(计算结果精确到0.1%)。
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下文字叙述与图象不相符的是( )
A. 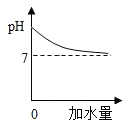 常温下向pH=13的氢氧化钠溶液中加水稀释
常温下向pH=13的氢氧化钠溶液中加水稀释
B. 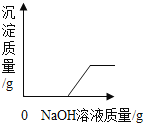 向一定质量的硫酸铁和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
向一定质量的硫酸铁和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
C. 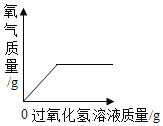 向一定质量的二氧化锰中加入过氧化氢溶液
向一定质量的二氧化锰中加入过氧化氢溶液
D. 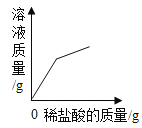 向一定质量的氧化铁粉末中加入稀盐酸
向一定质量的氧化铁粉末中加入稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】市场上有一种名为“污渍爆炸盐”的洗涤产品,它能高效去除衣物上的顽固污渍。小明对这种产品产生了兴趣,与小刚进行了如下探究。
(查阅资料)(1)“污渍爆炸盐”的主要成分是过碳酸钠(2Na2CO3 ·3H2O2),易溶于水且能与水反应生成一种碱性物质和一种强氧化性的物质;
(2)过碳酸钠的去污能力主要与其在反应中释放出的“活性氧”有关,“活性氧”含量越高,去污能力越强。
(实验1)小明向过碳酸钠水溶液中加入少量MnO2时产生大量气泡,该气体能使带火星的
木条复燃,反应的化学方程式是___________。
(提出问题)实验1反应后的溶液中溶质的成分是什么?
(做出猜想)根据过碳酸钠和水的组成作出三种猜想。
猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH
(实验2)为证明猜想一是否正确,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
小明取一定量溶液于试管中,向其中滴加CaCl2溶液 | 有白色沉淀 | 猜想一正确 |
小刚提出质疑,认为产生的白色沉淀不一定是CaCO3。他的理由是______。
(实验3)为证明猜想二是否正确,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
小刚取一定量溶液于试管中,向其中滴加足量稀盐酸 | 观察到___ | 溶液中一定含有Na2CO3,猜想二不正确 |
Na2CO3与稀盐酸反应的化学方程式是_____________。
(实验4)为进一步确定溶液中是否含有NaOH,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
向实验1反应后的溶液中滴加CaCl2溶液至不再产生沉淀为止,取上层清液,加入____ | 无明显现象 | 证明溶液中无NaOH,猜想一正确。 |
该实验中用CaCl2溶液而不能用石灰水,原因是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示的图象能正确反映对应变化关系的是
A. 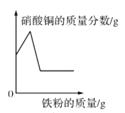 在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量
在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量
B.  向一定质量的打磨光亮的锌片中滴加盐酸
向一定质量的打磨光亮的锌片中滴加盐酸
C. 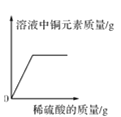 向盛有一定量氧化铜粉末的烧杯中不断加入稀硫酸至过量
向盛有一定量氧化铜粉末的烧杯中不断加入稀硫酸至过量
D. 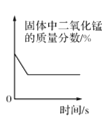 加热一定量氯酸钾和二氧化锰固体混合物
加热一定量氯酸钾和二氧化锰固体混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蜡烛是初中化学实验中的常用品,请回答下列有关问题:
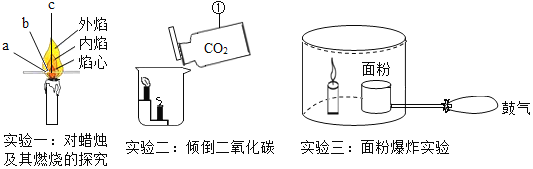
(1)实验一:实验中看到火柴梗的____________ 处最先炭化,由此可知蜡烛火焰的________温度最高;
(2)实验二:仪器①的名称为____________ ;实验时观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是_________________________。
(3)实验三:燃着的蜡烛的作用为___________ ,快速鼓入大量空气的目的为______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小宇为了测定实验室中氯酸钾样品的纯度,取10g样品与1g二氧化锰混合,依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 9.68 | 9.04 | 7.16 | 7.16 |
试计算:
(1)完全反应后产生的氧气的总质量为_____________g;
(2)样品中氯酸钾的纯度是____(写出计算过程)
(3)加热时间t1后,9.68g剩余固体中除杂质外还含有的物质为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们在实验室用下图装置制取氧气。
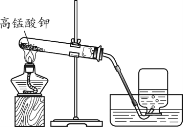
(1)加热高锰酸钾时,试管口略向下倾斜的原因是______。
实验后,同学们发现沾有高锰酸钾的白抹布洗完晾干后变为棕褐色。
(查阅资料)
草酸溶液能将棕褐色物质除去。
(提出问题)
哪些因素能加快草酸除去棕褐色物质的速率?
(进行实验)
将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
实验 编号 | 实验1
20℃ 水 | 实验2
20℃ 0.5%草酸溶液 | 实验3
20℃ 0.25%草酸溶液 | 实验4
20℃ 0.125%草酸溶液 | 实验5
30℃ 0.25%草酸溶液 | 实验6
40℃ 0.25%草酸溶液 |
现象 | 颜色 没有褪去 | 70秒后 颜色褪去 | 98秒后 颜色褪去 | 150秒后 颜色褪去 | 51秒后 颜色褪去 | 40秒后 颜色褪去 |
(解释与结论)
(2)配制200g溶质质量分数为 0.5%的草酸溶液,需要草酸的质量为______。
(3)实验1的目的是______。
(4)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比______(填实验序号)。
(5)由实验2、3、4可以得出的结论是______。
(反思与评价)
(6)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,进行中和反应实验
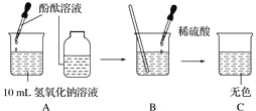
(1)B中发生中和反应的化学方程式_____。
(2)写出C的溶液(除酚酞外)溶质可能存在的几组情况_____(用化学式表示)
(3)反应过程中,不断滴入稀硫酸的话,温度会如何变化?_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com