
【题目】化学就在我们身边,它与我们的生产、生活息息相关。
(1)现有下列四种物质:
A 干冰 B 碳酸钙 C 小苏打 D 石墨
请选择适当的物质填空(填序号)。
①常用于制作干电池电极的是_____。
②可用于发酵糕点的是_____。
③可用于人工降雨的是_____。
④可用作补钙剂的是_____。
(2)能源和环境已成为人们日益关注的问题。
①目前,人们使用的燃料大多来自化石燃料,化石燃料属于_____(填“可再生能源”或“不可再生能源”)。燃煤的不充分燃烧会导致一系列的环境问题,下列环境问题与煤燃烧有直接关系的是_____(填字母);
A 酸雨 B 温室效应加剧 C 可吸入颗粒物增加
②分析下表,与煤炭相比,用天然气作燃料的优点有_____。
1g物质完全燃烧 | ||
产生二氧化碳的质量/g | 放出的热量/kJ | |
天然气 | 2.75 | 56 |
煤炭 | 3.67 | 32 |
④为提高煤的利用率,可将其转化为可燃性气体,反应的微观示意图如下,则生成物的分子个数比为_____。
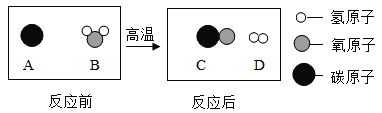
【答案】D C A B 不可再生能源 ABC 产生的二氧化碳少,放出的热量高(合理即可) 1:1
【解析】
(1)①石墨具有导电性,常用于制作干电池的电极,故选D。
②小苏打(碳酸氢钠)加热后会分解生成二氧化碳,可用于发酵糕点,故选C。
③干冰升华吸收大量的热,可用于人工降雨,故选A。
④碳酸钙含钙元素且对人体无害,可用作补钙剂,故选B。
(2)①化石燃料属于不可再生能源;煤燃烧会产生SO2、CO、NO2、CO2、可吸入颗粒物等,其中SO2、NO2会形成酸雨,CO2会加剧温室效应,故选ABC。
②天然气的主要成分是甲烷,从表中可看出,等质量的甲烷和煤炭完全燃烧,甲烷生成二氧化碳的质量比煤炭的少,而燃烧放出的热量却比煤炭高。
③由反应的微观示意图可看出,反应前后原子的种类、数目都不变,反应的化学方程式为
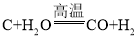 ,则生成物的分子个数比为1:1。
,则生成物的分子个数比为1:1。


科目:初中化学 来源: 题型:
【题目】熊去氧胆酸(C24H40O4)被用来治疗胆结石。下列有关熊去氧胆酸的说法正确的是( )
A. 熊去氧胆酸中氢、氧元素的质量比为10:1
B. 392g熊去氧胆酸中含有40g的氢元素
C. 熊去氧胆酸中氧元素的质量分数最小
D. 熊去氧胆酸是由68个原子构成的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组利用下列实验装置,开展O2、CO2的实验室制取和有关性质的研究。
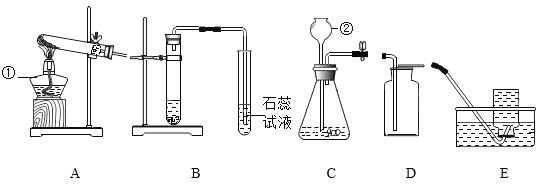
(1)写出A、C装置编号仪器的名称:①____________②____________。
(2)甲同学在B装置左侧试管中加入稀盐酸和大理石,则右侧试管中将观察到____________现象。
(3)乙同学用高锰酸钾制取O2的化学方程式为____________:若用C装置制取氧气的选用的药品和高锰酸钾相比,它的优点是____________,(写一条)。
(4)某同学在完成“氧气的制取与性质”的基础实验后,他还想进行蜡烛在不同浓度的氧气中燃烧情况的探究,现要较简便地获得两瓶不同浓度的氧气,应选择收集氧气的方法是____________(填字母),简述具体的操作方法是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各图能正确反映其对应变化关系的是
A.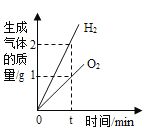 图1,电解水
图1,电解水
B. 图2,加热碳和氧化铜的混合物
图2,加热碳和氧化铜的混合物
C. 图3,用等质量、等浓度的双氧水分别制取氧气
图3,用等质量、等浓度的双氧水分别制取氧气
D. 图4,向一定质量的稀盐酸中逐滴加入氢氧化钙溶液
图4,向一定质量的稀盐酸中逐滴加入氢氧化钙溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液与人类生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示。
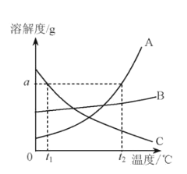
①![]() 时,A、B、C三种物质的溶解度由大到小的顺序是_____。
时,A、B、C三种物质的溶解度由大到小的顺序是_____。
②A、B、C三种物质中,溶解度随温度升高而减小的是_____。
③![]() 时,完全溶解ag A物质最少需要水的质量是_____ g。
时,完全溶解ag A物质最少需要水的质量是_____ g。
④![]() 时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量_____B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)
时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量_____B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、_____和滤纸。
(3)在实验室中,配制溶质质量分数为![]() 的氯化钠溶液45g,需要氯化钠固体的质量是_____g。将
的氯化钠溶液45g,需要氯化钠固体的质量是_____g。将![]() 的氯化钠济配成含氯化钠为0.9%的溶液,得到氯化钠溶液的质量是_____g。
的氯化钠济配成含氯化钠为0.9%的溶液,得到氯化钠溶液的质量是_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某粗铜粉末中含有少量的铁、锌和金。某化学兴趣小组的同学为测定该粗铜粉末中铜的质量分数,开展如下实验探究:
步骤I:称取质量为m1的粗铜样品;
步骤Ⅱ:向样品中逐滴加入足量的稀盐酸,充分反应;
步骤Ⅲ:过滤,将滤渣洗涤、干燥后称量,质量为m2;
步骤IV:将步骤Ⅲ所得固体在空气中充分灼烧,冷却至室温后称量,质量为m3。
请回答下列问题:
(1)步骤Ⅱ的目的是______;
(2)判断步骤Ⅱ中加入的稀盐酸足量的方法是_________:
(3)步骤IV中反应的化学方程式为_________;
(4)按此方法测得粗铜中铜的质量分数为_____(用m1、m2、m3的代数式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据实验室制取气体的常用装置图,回答问题:
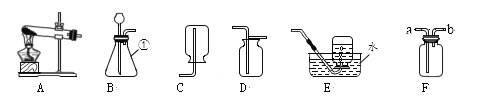
(1)图中①仪器名称是______________。
(2)实验室既可制取二氧化碳,又可制取氧气的发生装置______(填装置字母),用该装置制取氧气的化学方程式为:______________________________。
(3)若F装置装满水,收集氧气,则气体从F装置的______端通入;若F装置中盛有浓H2SO4,则不能干燥______(填序号)。
①氨气 ②氢气 ③氧气 ④二氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种物质的溶解度曲线,下列所获信息正确的是
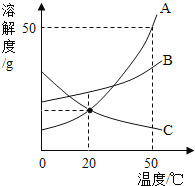
A.在50°C时,A物质的溶解度为50
B.当A中混有少量B时,可采用蒸发溶剂的方法提纯A
C.相同质量的水分别溶解A、B、C达到饱和状态时,所溶解的质量A>B>C
D.将50°C时A、B、C三种物质的饱和溶液降温至20°C时,这三种溶液的溶质质量分数的大小关系是B>A>C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com