
【题目】某化学兴趣小组的同学欲在常温、常压下,用一定质量的大理石与足量的稀盐酸反应,测定大理石中碳酸钙的质量分数(杂质不参与反应)。利用如下图所示的装置(盛放大理石的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成二氧化碳的体积为V。已知本实验条件下,二氧化碳的密度为ρ。
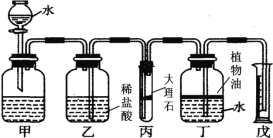
关于该实验,有如下说法:①打开分液漏斗的活塞并不断注水,可观察到乙中稀盐酸进入装置丙中;②实验结束后读数时,视线要与量筒内凹液面最低处保持水平;③丁中若没有植物油会导致测定结果会偏大;④装置中的空气对实验结果无影响;⑤若将乙中的稀盐酸换成稀硫酸,反应速率会更快。其中正确说法的个数有
A. 4个 B. 3个 C. 2个 D. 1个
科目:初中化学 来源: 题型:
【题目】高纯硅可用于制备硅半导体材料.制备高纯硅的主要生产流程如下图所示:
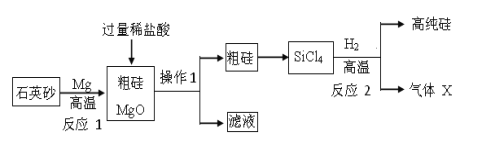
查阅资料:①石英砂的主要成分是二氧化硅;
②MgO能与稀盐酸反应生成氯化镁溶液。
(1)标出二氧化硅中硅元素的化合价_________;写出合理处理中间产物CO的一种方法_____________;
(2)操作1中用到的玻璃仪器有烧杯、玻璃棒和______________;
(3)反应2除生成高纯硅外,同时还生成一种气体化合物.请写出此过程所发生反应的化学方程式___________;
(4)反应 2 要在无氧气环境中进行,从安全角度考虑,原因是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我市东临渤海,有着丰富的海洋资源。请思考下列问题:
(1)已知东营盐场测得:①海水中含NaCl约为3.5%。②在海边打深井,井水中含NaCl约为8%。晒盐最好用_____(填序号)作原料。
(2)关于晒盐原理的说法正确的是
A.利用阳光和风力,使水分燕发,析出盐
B.日光照晒后,板化钠的溶解度变小
(3)海水晒盐提取食盐晶体后留下的母液叫卤水,其中含有的KCl、MgCl2、MgSO4等物质可作为重要的化工原料。它们的溶解度曲线如右图所示。
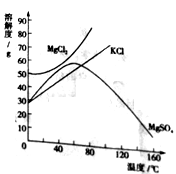
①60℃ 时,将50g硫酸镁加入到100g水中,充分搅拌,所得溶液的溶质质量分数为______,若使其形成饱和溶液,可采取的措施有____。
A.增加溶质 B.蒸发溶剂 C.升高温度 D.降低温度
② 对卤水中含有的KCl、MgCl2、MgSO4三种物质,下列说法正确的是_____
A.三种物质均为易溶物质
B.20℃时,向40gKCl固体和40gMgCl2固体中分别加入100g水充分溶解后,两种溶液均能达到饱和状态
C.60℃时,三种物质溶于水形成的溶液浓度可能相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工业废液中含有CuSO4、ZnSO4、FeSO4,如果将废液直接排放就会造成水污染.于是几位同学设计实验处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:

请回答:
(1)操作①的名称是_____.需要的玻璃仪器有烧杯、________ 、玻璃棒。
(2)步骤①中加入过量M的化学式_________.请写出工业上用赤铁矿(主要成分为Fe2O3)炼铁的化学方程式____________.
(3)若加入一定量M(不考虑上述实验过程中后续实验现象和结论),则滤液A中一定含有的溶质的化学式是_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学符号回答下列问题:
(1)两个氮分子____________; (2)2个氢原子_____________;
(3)氢氧化镁____________; (4)五氧化二磷中磷元素的化合价____;
(5)n个铵根离子_______; (6)电解水的化学方程式____________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁(MgO2)都是重要化工原料。
Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧:高温煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊,煅烧时反应的化学方程式为________。
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO + H2O2 = MgO2+H2O,温度升高,说明该反应________热量(填“放出”或“吸收”)。其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(![]() )的影响分别如图1所示,则最佳的煅烧温度为________℃、煅烧时间_______小时。
)的影响分别如图1所示,则最佳的煅烧温度为________℃、煅烧时间_______小时。

(3)分离:得到产品。
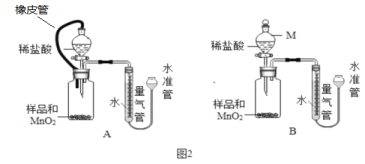
(4)测定:假设产品中仅少量MgO,某小组设计图2装置,通过测定生成O2体积,计算MgO2的质量分数.
已知:a. MnO2与稀盐酸不反应 b. MgO2+2HCl = MgCl2+H2O2
c. 2MgO2![]() 2MgO+O2↑ d. MgO+C
2MgO+O2↑ d. MgO+C![]() Mg+CO↑
Mg+CO↑
①仪器M 的名称是_______________,MnO2的作用是__________。
②相同条件下,装置______能使测定结果更准确。(填图2 中“装置A”或“装置B”)
③经讨论,该小组又设计了下列2种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是__________(填序号)。
a.加热,使MgO2完全分解,测出剩余固体的质量
b.与足量炭粉在高温下充分反应,测出生成Mg的质量
Ⅱ.MgCl2是制备Mg2(OH)2CO3的原料,工业上通常用碳酸镁来制备MgCl2,反应如下:MgCO3 + Cl2 + CO![]() MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的碳酸镁多少吨_____?(写出计算过程)。
MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的碳酸镁多少吨_____?(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,请使用化学用语完成下列各题
![]()
(1)①已知如图为某粒子的结构示意图,则该粒子的离子符号是_______②构成氯化钠的微粒符号_____ ③2个碳酸根粒子______ ④n个氧分子________
(2)下列物质中:混合物有________,氧化物有________,单质有_______
A.水银 B.蒸馏水 C.硫酸铜 D.双氧水 E.冰水混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年5月30日,媒体公布我国新疆准噶尔盆地探明一储量为10亿吨的大型油田。石油是工业的“血液”,是多种碳氢化合物的混合物。
(1)石油不直接作为燃料的原因是____。
(2)石油在综合利用时,可以得到多种产品,如石油液化气(主要成分丁烷)、汽油等。 丁烷燃烧的化学方程式为:2R+13O2![]() 8CO2+10H2O,则丁烷(R)的化学式是______。
8CO2+10H2O,则丁烷(R)的化学式是______。
(3)化石能源是有限的,用一点少一点,最终会被耗尽,这充分说明了化石能源具_____有性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)如下图是氧、硫、氯三种元素的原子结构示意图。

①氯原子的结构示意图中x的数值是_____;其在化学反应中易_______电子(填“得到”或“失去”),其离子符号为____________。
②氧和硫两种元素最本质的区别是它们原子中的__________________不同。
③具有相似化学性质的元素是______和______(填元素符号)。
④由氧元素组成的气体单质参与反应生成了一种白色固体,符号表达式为__________________。
(2)如图为元素周期表图,请回答下列问题:
IA | 0 | ||||||||
1 | 1 H 氢1.00 | ||||||||
IIA | IIIA | IVA | VA | VIA | VIIA | ||||
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | X P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 | |
①表中磷原子的核电荷数x=_______,该元素位于元素周期表的第_____周期。
②表中具有相对稳定结构的元素是________,它属于_________元素(填金属或非金属)。
③若某种铝原子的相对原子质量为27,则它的中子数为____。它与氧元素形成的化合物的化学式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com