
【题目】碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁(MgO2)都是重要化工原料。
Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧:高温煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊,煅烧时反应的化学方程式为________。
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO + H2O2 = MgO2+H2O,温度升高,说明该反应________热量(填“放出”或“吸收”)。其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(![]() )的影响分别如图1所示,则最佳的煅烧温度为________℃、煅烧时间_______小时。
)的影响分别如图1所示,则最佳的煅烧温度为________℃、煅烧时间_______小时。

(3)分离:得到产品。
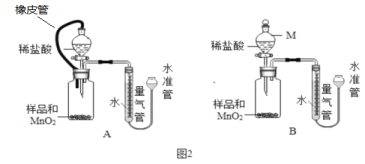
(4)测定:假设产品中仅少量MgO,某小组设计图2装置,通过测定生成O2体积,计算MgO2的质量分数.
已知:a. MnO2与稀盐酸不反应 b. MgO2+2HCl = MgCl2+H2O2
c. 2MgO2![]() 2MgO+O2↑ d. MgO+C
2MgO+O2↑ d. MgO+C![]() Mg+CO↑
Mg+CO↑
①仪器M 的名称是_______________,MnO2的作用是__________。
②相同条件下,装置______能使测定结果更准确。(填图2 中“装置A”或“装置B”)
③经讨论,该小组又设计了下列2种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是__________(填序号)。
a.加热,使MgO2完全分解,测出剩余固体的质量
b.与足量炭粉在高温下充分反应,测出生成Mg的质量
Ⅱ.MgCl2是制备Mg2(OH)2CO3的原料,工业上通常用碳酸镁来制备MgCl2,反应如下:MgCO3 + Cl2 + CO![]() MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的碳酸镁多少吨_____?(写出计算过程)。
MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的碳酸镁多少吨_____?(写出计算过程)。
【答案】Mg2(OH)2CO3![]() 2MgO + H2O + CO2↑ 放出 650 2 分液漏斗 催化作用 A a 16.8t
2MgO + H2O + CO2↑ 放出 650 2 分液漏斗 催化作用 A a 16.8t
【解析】
Ⅰ、(1)镁元素对应的氧化物是氧化镁,氢元素对应的氧化物是水,使澄清石灰水变浑浊的气体是二氧化碳,碱式碳酸镁在高温条件下反应生成氧化镁、水和二氧化碳,故反应的化学方程式写为:Mg2(OH)2CO3![]() 2MgO + H2O + CO2↑。
2MgO + H2O + CO2↑。
(2)反应后温度升高,说明该反应是一个释放热量的反应,故填放出;
由图可知,MgO2产率最高时的温度为650℃,故填650;
由图可知,MgO2产率最高时的煅烧时间为2小时,故填2。
(4)①仪器M 的名称是分液漏斗,故填分液漏斗;
MnO2与稀盐酸不反应,其出现在反应中就是作催化剂,起催化作用,故填催化作用。
②装置A是一密闭装置,使反应在密闭装置中反应,没有外界因素的影响,结果更准确,故填A。
③a、加热使MgO2完全分解,测出剩余固体质量,可以根据质量差为生成的氧气的质量求出MgO2的质量,进而确定MgO2的质量分数,选项正确;
b、由于氧化镁和过氧化镁都能和碳反应,无法确定过氧化镁生成的镁的质量,也无法求算MgO2的质量分数,选项错误,故选a。
Ⅱ、解:设需要碳酸镁的质量为x
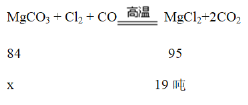
84:95=x:19t
x=16.8t
答:需要碳酸镁的质量为16.8吨。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:初中化学 来源: 题型:
【题目】某小组同学为探究二氧化锰对过氧化氢分解速度的影响,设计了以下实验:
(1)完善实验一、实验二:
实验步骤 | 实验现象 | 实验结论 | |
实验一 |
| 带火星的木条不复燃 | 过氧化氢分解的速率较慢 |
实验二 |
| ___________ | ________ |
(2)实验三:待实验二结束,剩余的液体化学式为_____,倒出多余液体,继续向其中加入5%的过氧化氢溶液,实验现象为____________,得出结论__________,写出此时的反应方程式__________;
(3)实验四,实验之前称量加入二氧化锰的质量为m1,待实验三结束后,取出二氧化锰,干燥后称量质量为m2,则m1_____m2(填“>”、“<”、“=”),得出结论___________,从液体中取出二氧化锰的操作名称为______;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】美国普度大学研发出一种制备氢气的新工艺,流程如下图所示.下列说法错误的是( )
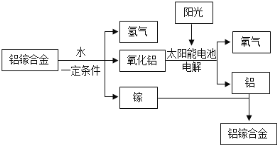
A. 铝镓合金可以循环使用
B. 流程中的氧化铝、水和氧气都属于氧化物
C. 太阳能的利用可以部分解决能源危机问题
D. 铝镓合金与水反应的化学方程式为:2Al+3H2O ![]() Al2O3+3H2↑
Al2O3+3H2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】把一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法中正确的是( )
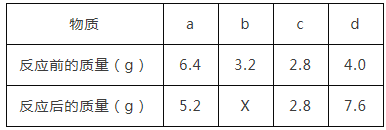
A. a和c是反应物 B. d一定是催化剂
C. X=2.0 D. 该反应是化合反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学欲在常温、常压下,用一定质量的大理石与足量的稀盐酸反应,测定大理石中碳酸钙的质量分数(杂质不参与反应)。利用如下图所示的装置(盛放大理石的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成二氧化碳的体积为V。已知本实验条件下,二氧化碳的密度为ρ。
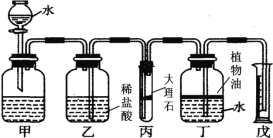
关于该实验,有如下说法:①打开分液漏斗的活塞并不断注水,可观察到乙中稀盐酸进入装置丙中;②实验结束后读数时,视线要与量筒内凹液面最低处保持水平;③丁中若没有植物油会导致测定结果会偏大;④装置中的空气对实验结果无影响;⑤若将乙中的稀盐酸换成稀硫酸,反应速率会更快。其中正确说法的个数有
A. 4个 B. 3个 C. 2个 D. 1个
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳和碳的化合物都是非常重要的物质。
(1)碳原子的结构示意图为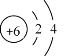 ,碳原子的核电荷数为_______。
,碳原子的核电荷数为_______。
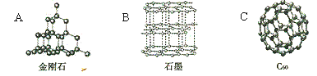
(2)碳的单质有多种,具有下列结构的碳单质中,由分子构成的是_____。
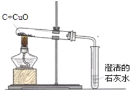
(3)古代用墨书写或绘制的字画虽年久仍不变色,原因是墨中主要成分碳具有________________性。如图是木炭还原氧化铜的实验,大试管中的反应体现了碳的还原性,其反应的化学方程式是______,单质碳的还原性可以用于冶金工业。
(4)二氧化碳能参与光合作用完成大气中的“碳循环”,但是大气中二氧化碳的含量不断上升,会使全球变暖,从而导致______________。蔬菜大棚用作气肥的二氧化碳,可用多种方法制得,例如可以用稀硫酸(H2SO4)与碳酸氢铵(NH4HCO3)反应制得,反应后生成硫酸铵[(NH4)2SO4]、水和二氧化碳,这个反应的化学方程式是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】密闭容器中盛有CH4和O2的混合气体,点燃使其充分反应,CH4全部转化为CO、CO2和H2O,待容器恢复至室温,测得容器内混合气体中碳元素的质量分数为36%.则反应前CH4和O2的质量比为( )
A. 4:13 B. 3:10 C. 2:7 D. 1:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)如图是某金属元素形成微粒的结构示意图,该金属在空气中燃烧时放出大量的热,并发出耀眼的白光。该金属元素原子核外电子数 = ______;其所示微粒的符号为________;
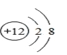
(2)下图是该反应的微观示意图。如图所示的该金属在空气中燃烧时反应的化学方程式为____________
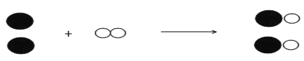
(3)决定元素种类的是(_________)
A.质子数 B.电子数 C.中子数 D.最外层电子数
(4)下列微粒中,质子数少于核外电子数的是(______)
A.OH﹣ B.Fe2+ C.HCl D.H2O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】等质量甲、乙、丙三种金属分别放入三份浓度相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知甲、乙、丙在生成物中的化合价均为+2价)。则下列说法中错误的是( )
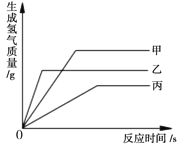
A. 生成氢气的质量:甲﹥乙﹥丙
B. 相对原子质量:乙﹥丙﹥甲
C. 金属活动性:乙﹥甲﹥丙
D. 消耗硫酸的质量:甲﹥乙﹥丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com