
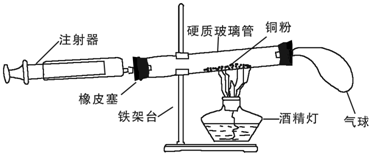
分析 (1)根据铜丝被加热生成氧化铜解答;
(2)根据交替缓慢推动两注射器的目的是使空气中的氧气与铜充分反应解答;
(3)根据计算空气中氧气的含量的方法和质量守恒定律解答;
(4)根据使实验成功的合理操作分析解答.
解答 解:
(1)铜丝被加热生成氧化铜;实验过程中出现的现象是:铜粉由红色变为黑色,反应的文字表达式为:铜+氧气$\frac{\underline{\;\;△\;\;}}{\;}$氧化铜.
(2)在实验的加热过程中,交替缓慢推动两注射器的目的是使空气中的氧气与铜充分反应.故保证空气跟铜粉充分接触的操作是:交替缓慢推动两注射器;
(3)由此数据计算空气中氧气的含量为:$\frac{19mL-7mL}{19mL+40mL}×$100%≈20.3%,<21%,可能是装置漏气,加热时气体体积膨胀,跑出一部分;根据质量守恒定律,实验前后,密闭系统内物质的总质量不变;
(4)装置气密性良好和使氧气跟铜反应充分,是本实验成功的关键,使实验成功的其他合理操作可以是等到装置冷却后再读数,温度足够高;
答案:
(1)细铜丝由红色变为黑色;铜+氧气$\frac{\underline{\;\;△\;\;}}{\;}$氧化铜;
(2)交替缓慢推动两注射器;
(3)20.3%;<;不变;
(4)等到装置冷却后再读数;温度足够高.
点评 实验的改进中要注意到方法和药品的完善,但是不能改变的是基本的实验原理.另外实验改进要方法更科学、操作更简单、现象更明显、结论更明确.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结 论 |
| 甲:取少量该溶液放入试管中, 滴加几滴酚酞试液 | 溶液变红 | 该溶液没有变质 |
| 乙:取少量该溶液放入试管中加入 一定量澄清石灰水 | 产生白色沉淀 | 该溶液已经变质.产生沉淀 的化学方程式为Na2CO3+Ca(OH)2═2NaOH+CaCO3↓ |
| 丙:取少量该溶液放入试管中加入 一定量稀盐酸 | 产生气泡 | 该溶液已经变质 |
| 实验步骤 | 实验现象 | 结论 |
| 另取少量原溶液放入试管中.加入过量的CaCl2溶液,振荡后再滴加酚酞试液 | ⑦产生白色沉淀 ⑧溶液由无色变为红色 | 该溶液已经部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 该粒子各电子层电子的能量相同 | B. | 该粒子核外电子总数为8 | ||
| C. | 该粒子表示的是原子 | D. | 该粒子属于金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醛是由C、H、O三种元素组成 | |
| B. | 甲醛分子是由C、H、O原子构成 | |
| C. | 一个甲醛分子含有四个原子 | |
| D. | 甲醛是由一个碳原子、2个氢原子、1氧原子构成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com