
 资源、能源、环境与人类的生活和社会发展密切相关.
资源、能源、环境与人类的生活和社会发展密切相关.分析 (1)①根据软化硬水的方法进行分析;②根据过滤后,滤液仍然浑浊的原因进行分析;
(2)①根据常见化石燃料的种类进行分析;
②根据能量的转化方式进行分析;
(3)①根据清洁能源的优点进行分析;
②A、复分解反应是指由两种化合物相互交换成分,生成另外两种新的化合物的反应;B、根据物质的化学式分析;C、在化合物中元素的化合价代数和为零;D、二氧化碳和二氧化硫具有相似的化学性质.
解答 解:(1)①生活中通过加热煮沸可以使硬水中的可溶性钙镁化合物发生反应以水垢的形式析出,形成含较少可溶性钙镁化合物的软水;故答案为:加热煮沸;
②过滤后,滤液仍然浑浊的可能原因有:承接滤液的烧杯不干净,②倾倒液体时液面高于滤纸边缘,③滤纸破损;故答案为:滤纸破损.
(2)①常见的化石燃料包括煤、石油和天然气;故答案为:天然气;
②某同学按如图所示的实验装置进行实验时,发现电流计指针发生了偏转,且铜片上有气泡产生.实验中发生的能量转化方式是化学能转化为电能;故答案为:化学能转化为电能;
(3)①煤燃烧发电会产生大量的污染物二氧化硫和氮氧化合物,利用太阳能、风能等清洁能源替代煤发电可燃有效防止酸雨的形成;故答案为:太阳能;
②A、反应①发生的不是复分解反应,因为反应不是两种化合物简单的交换成分.故选项错误;
B、Na2SO3的名称是亚硫酸钠.故选项错误;
C、Na2SO3中硫元素的化合价是+4.故选项正确;
D、反应说明SO2与CO2有相似的化学性质.故选项正确.
故选CD.
故答案为:
(1)①加热煮沸; ②滤纸破损;(或液面高于滤纸边缘)
(2)①天然气; ②化学能转化为电能;(3)①太阳能(或风能、地热能等);②CD
点评 本题考查知识点较多,基础性强,可依据已有知识进行解答.在平时注意将化学知识与生产生活联系在一起,那么很容易解答出来的;


 名师点拨卷系列答案
名师点拨卷系列答案科目:初中化学 来源: 题型:推断题
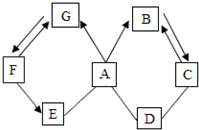 如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同的气体,D是一种红棕色粉末,E常用于改良酸性土壤,F是相对分子质量最小的氧化物.请回答下列问题.
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同的气体,D是一种红棕色粉末,E常用于改良酸性土壤,F是相对分子质量最小的氧化物.请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
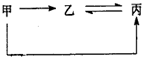
| A. | C CO CO2 | B. | CO2 C6H12O6 H2O | ||
| C. | CaO Ca(OH)2 CaCO3 | D. | Cu CuO Cu(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 取反应后的滤液观察,滤液可能呈蓝色 | |
| B. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 取滤渣滴加稀硫酸,可能有气泡产生 | |
| D. | 滤渣中的物质至少有两种 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 (1)2016年底,沪昆高铁和云贵高铁即将开通,人们的出行将更加方便、快捷.结合所学化学知识,回答下列问题:
(1)2016年底,沪昆高铁和云贵高铁即将开通,人们的出行将更加方便、快捷.结合所学化学知识,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
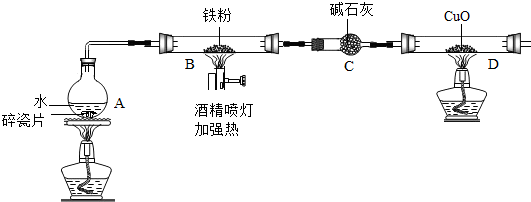
| 实验操作 | 实验现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
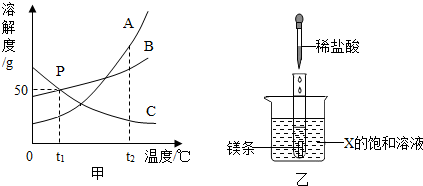
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
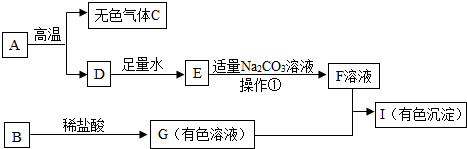
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com