
【题目】向一定量 NaOH 溶液中,滴加稀盐酸,所加盐酸的量与溶液 pH 的变化如图所示:
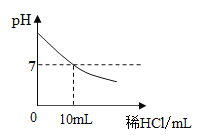
(1)当加入稀盐酸的体积为_____mL 时,稀盐酸与 NaOH 溶液恰好完全反应;
(2)向上述加了 12mL 稀盐酸后的 NaOH 溶液中滴加紫色石蕊试液,溶液显_____色;
(3)当加入 8 mL 稀盐酸时,溶液中的溶质有_____。
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:
【题目】某同学欲利用混有少量CO2的CO气体还原氧化铜。除去CO2后进行还原并验证反应后的气体产物。用下图所示实验装置(可重复使用),按从左到右连接顺序正确的是
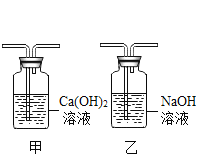
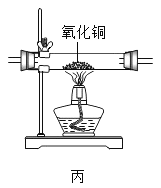
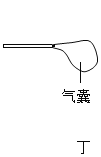
A.甲→乙→丙→丁
B.甲→丙→乙→丁
C.乙→甲→丙→甲→丁
D.乙→甲→丙→乙→丁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一包Na2CO3和NaOH固体样品,为了测定Na2CO3的质量分数,取该样品20g,加水搅拌至全部溶解.然后逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示。请计算:
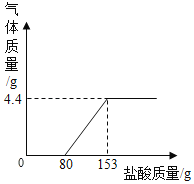
(1)生成气体的质量____;
(2)该样品中Na2CO3的质量分数____;
(3)所用稀盐酸溶质的质量分数____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据统计,我国仅20世纪90年代就发生火灾约89万起,给人民造成重大损失。应用化学知识能有效预防和控制火灾。下面对图中灭火实例的灭火原理解释不正确的是( )

灭火实例 | 灭火原理 | |
A | 住宅失火时,消防队员用水灭火 | 降低可燃物的着火点 |
B | 酒精在桌上着火时,用湿抹布盖灭 | 隔绝空气或氧气 |
C | 炒菜油锅着火时,用锅盖盖熄 | 隔绝空气或氧气 |
D | 扑灭森林火灾时,设置隔离带 | 可燃物与燃烧物隔离 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)自来水属于_____(填“纯净物”或“混合物”);检验自来水是硬水还是软水,可选用的物质是_____; 生活中既能降低水的硬度,又能杀菌消毒的方法是_____。
(2)某同学收集到一杯有臭味的浑浊河水,先用滤纸进行过滤,需用到的玻璃仪器有玻璃棒、_____和_____,其中玻璃棒的作用是_____。
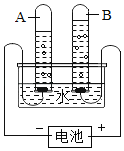
(3)同学们为了探究水的组成,做了电解水实验,如图所示,写出该实验中反应的文字表达式:_____。实验开始后,发现两极都产生气泡,试管A中的气体是_____。该实验证明:_____。
(4)请写出一种生活中的节水方法:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图文对应关系正确的是
A.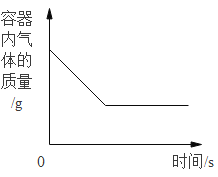 碳在盛有氧气的密闭容器中燃烧
碳在盛有氧气的密闭容器中燃烧
B.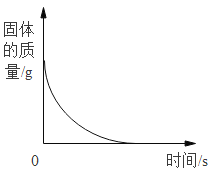 向一定量的铁中加入足量稀盐酸
向一定量的铁中加入足量稀盐酸
C.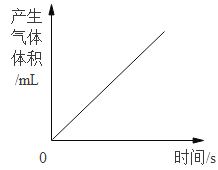 一定量的高锰酸钾受热分解过程
一定量的高锰酸钾受热分解过程
D.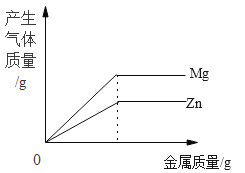 向两份完全相同的稀硫酸中分别加入足量锌、镁粉
向两份完全相同的稀硫酸中分别加入足量锌、镁粉
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】每年的 CES(国际消费类电子产品展览会)都会有一大波“黑科技”产品发布, 而这些产品大多是由金属材料制成,铜是其中重要的金属材料。
I.自然界中的铜主要以化合物形式存在于铜矿石中,从“绿色化学”的理念分析,以下铜矿最适宜炼铜的是_____(填序号)
A 黄铜矿(CuFeS2) B 辉铜矿(Cu2S)
C 蓝铜矿 [Cu(OH)2(CO3)2 ] D 斑铜矿(Cu5FeS4)
II.某化学兴趣小组用如下实验装置制取一氧化碳,再用一氧化碳还原氧化铜模拟炼铜。
(查阅资料)
(1)实验室常用甲酸(H2CO2)和浓硫酸混合加热制备 CO,同时生成 H2O。
(2)浓硫酸具有吸水性。
(进行实验)小组同学组装好下图装置并检查装置气密性之后开始实验,先让 A 装置反应一会儿,然后熄灭 A 中的酒精灯,再点燃 C 装置中的酒精灯。
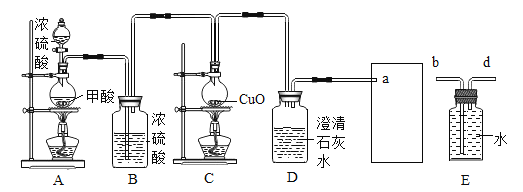
(1)装置 B 的作用是_____;装置 C 中发生反应的化学方程式是_____。
(2)装置 D 的作用是_____;该装置的组装存在的错误是_____; 改正之后,该装置中发生反应的化学方程式是_____。
(3)为避免一氧化碳污染空气,回收利用一氧化碳,方框中应连接装置 E,与 a 导管接口相接的是_____(填“b”或“d”)。
(4)实验结束之后,得到带有金属光泽的砖红色粉末,小组决定对该固体的成分进行探究。
(提出问题)红色的固体是什么?
(查阅资料)氧化亚铜(Cu2O)是红色粉末状固体;
会与稀硫酸反应:Cu2O + H2SO4 == CuSO4 + Cu + H2O。
(提出猜想)猜想一:该固体全部为 Cu;
猜想二:该固体全部为 Cu2O;
猜想三:该固体为 Cu2O 和 Cu 的混合物。
(实验方案)
实验步骤 | 实验现象及实验结论 |
取少量固体粉末于试管中, 加入过量_____溶液。 | 若无明显变化,则猜想一成立; 若溶液变为_____色,则猜想二或猜想三成立。 |
为了进一步确定混合物的组成,另取 m g 固体,重复上述实验,然后将反应后的物质过滤、洗涤、干燥,再次称量得到 n g 固体,若 m 和 n 满足_____的量的关系,则 猜想三成立。
(得出结论)该固体为 Cu2O 和 Cu 的混合物。
(交流讨论)
(1)从实验安全的角度考虑,本实验存在的危险是_____,改进的方法是_____;
(2)从物质的转化程度考虑,小组同学针对如何将氧化铜全部转化为铜单质展开讨论, 查阅了大量资料之后知道,反应条件是影响生成物的重要因素,因此一致认为在下次实验中需要适当加大 CO 的通入量或者_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是在一定条件下,某物质发生化学反应的微观模拟图。请回答下列问题:
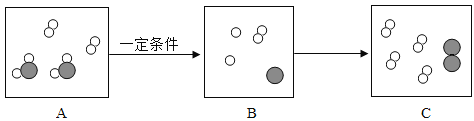

(1)请在B图中补充相关粒子图形,使其表示正确__________。
(2)此变化前后没有发生改变的微观粒子有______________。
(3)从微观角度解释此反应为分解反应的原因_______________。
(4)画出和构成反应物的一个分子质子数相同的原子结构示意图_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表列出了硝酸钾在不同温度时的溶解度.
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
某兴趣小组做了以下实验:

(1)上述溶液中的溶剂是________,上述实验过程中得到的溶液一定属于不饱和溶液的是________(填数字序号),⑤所对应的实验现象是________.
(2)实验过程中,溶质的质量分数一定相等的是________(填数字序号).
(3)为了防止水体污染,小组同学提出了如下方案处理实验后的废液: 步骤I:将⑤继续冷却至0℃,过滤,共可回收得到KNO3固体________g.
步骤II:向滤液中加入________g水稀释,得到溶质的质量分数为1%的KNO3稀溶液,将此溶液做为化肥使用.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com